Węglik aluminium: zastosowania
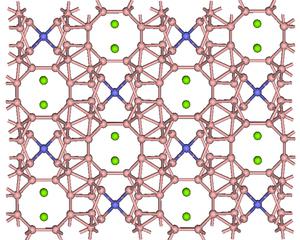
Związek chemiczny o wzorze Al ^ C nazywa się węglikiem glinowym. Jego wygląd jest reprezentowany przez żółtawy krystaloid substancji. Związek jest bardzo odporny na działanie środowiska zewnętrznego, temperatura topnienia alumoksarbku wynosi 1400 ° C, a gęstość względna 2,36 g / cm3. Krata Al₄C₃ jest złożona i zawiera atomy węgla. Występują tam jako aniony. Węglik glinu, podobnie jak inne związki nieorganiczne, ma wiele zastosowań. Ta substancja należy do pierwszej grupy, której różnica polega na niezmiennej wartościowości typowej dla metalu w normie.
Węglik aluminium: substancja

Substancja może być otrzymana przez połączenie metalu z węglem, który musi być umieszczony w piecu łukowym. Złożony węglik wapnia istnieje również niewielka zawartość Al содержаниеC₃. Po otrzymaniu elektrolitów związek jest produktem korozji grafitu. Reakcja tlenku glinu z węglem tworzy Al₄C₃. Następnym sposobem uzyskania tej substancji jest równoczesna kalcynacja koksu i aluminium w temperaturze 1800 stopni. Jest produkowany przez specjalnie wyszkolonych pirotechników i chemików. Nie możesz próbować dostać węglika aluminium w domu, jak również w laboratoriach, które nie są do tego przeznaczone.
Właściwości fizyczne i chemiczne
Główną właściwością substancji jest jej zdolność oddziaływania z wodą, tlenem i wodorotlenek sodu. Ponadto węglik glinu może się topić, załamać i rozpuścić. Ma entalpię formacji ΔH = -209 (S = 88,95), energia Gibbsa = -196 t, molowa pojemność cieplna = 116,8. Współczynnik załamania światła węglik aluminium = 2,7 dla 20 stopni. Al₄C₃ może wchodzić w kontakt z wieloma pierwiastkami chemicznymi, tworząc dobrze znane związki niezbędne w przemyśle. Przykładem jest gaz ziemny - metan. Można go uzyskać przez zmieszanie węglika glinu z wodą. W tym przypadku H20 działa jak rozpuszczalnik metalu, w wyniku czego główny związek ulega rozkładowi.
Zastosowania z węglików spiekanych
 Al₄C₃ jest stosowany w różnych gałęziach przemysłu. Podczas wytwarzania alumokarbidu z cząstkami grafitu powstaje bardzo silny materiał. Narzędzia tworzące ten związek mają taką samą twardość jak topaz. Zazwyczaj alumokarbid dodaje się do cięcia przedmiotów używanych na obrabiarkach, jako sprzęt medyczny itp. Ponadto ten związek jest niezbędnym materiałem w pirotechnice. Był używany w tej dziedzinie przez długi czas i jak dotąd nie zastąpiono go. Tutaj alumokarbid jest niezbędny do wytwarzania iskier. Jego obecność w pracach pirotechnicznych zależy od tego, w jakim stopniu i w jakim stopniu stosuje się proszek. Innym zastosowaniem substancji jest przemysł chemiczny, w którym związek jest niezbędny do tworzenia różnych produktów, w szczególności gazów organicznych.
Al₄C₃ jest stosowany w różnych gałęziach przemysłu. Podczas wytwarzania alumokarbidu z cząstkami grafitu powstaje bardzo silny materiał. Narzędzia tworzące ten związek mają taką samą twardość jak topaz. Zazwyczaj alumokarbid dodaje się do cięcia przedmiotów używanych na obrabiarkach, jako sprzęt medyczny itp. Ponadto ten związek jest niezbędnym materiałem w pirotechnice. Był używany w tej dziedzinie przez długi czas i jak dotąd nie zastąpiono go. Tutaj alumokarbid jest niezbędny do wytwarzania iskier. Jego obecność w pracach pirotechnicznych zależy od tego, w jakim stopniu i w jakim stopniu stosuje się proszek. Innym zastosowaniem substancji jest przemysł chemiczny, w którym związek jest niezbędny do tworzenia różnych produktów, w szczególności gazów organicznych.
Czym jest metan?
Ten związek należy do grupy organicznej, w strukturze jest prostym węglowodorem i ma wzór CH 4 . Metan reaguje niewiele z wodą, jest bezwonny i bezbarwny. Gaz należy do grupy alkanów, jest wystarczająco odporny na działanie różnych reakcje chemiczne. Uważa się, że metan nie jest niebezpieczny dla ludzkiego zdrowia, jednak niektórzy naukowcy twierdzą, że jest odwrotnie. Ludzie, którzy mają stały kontakt z gazem, są zmiany w ośrodkowym układzie nerwowym. Metan jest wybuchowy, dlatego w produkcji przemysłowej konieczne jest uważne monitorowanie jego stężenia w powietrzu. Z uwagi na to, że gaz jest bezwonny, trudno zauważyć wyciek. Z tego powodu w przedsiębiorstwach instalowane są specjalne czujniki rejestrujące jego poziom.
Sposoby na wydobycie metanu
 Z uwagi na to, że gaz jest naturalnym związkiem, nie zawsze jest produkowany przez laboratorium. Metan wytwarzany jest w warunkach beztlenowych, co odbywa się w wyniku procesów fermentacji na bagnach, w jelitach zwierząt i nazbyt mokrej ziemi. Według naukowców jeden z nich Księżyce Saturna zawiera ciekłe mieszaniny zawierające ten gaz na swojej powierzchni. Również metan jest jednym ze składników atmosfery dużych planet. Najwyższą zawartość metanu obserwuje się w gazach naturalnych, kopalnianych i bagiennych. W warunkach przemysłowych gaz wytwarza się przez uwodornienie i koksowanie węgla.
Z uwagi na to, że gaz jest naturalnym związkiem, nie zawsze jest produkowany przez laboratorium. Metan wytwarzany jest w warunkach beztlenowych, co odbywa się w wyniku procesów fermentacji na bagnach, w jelitach zwierząt i nazbyt mokrej ziemi. Według naukowców jeden z nich Księżyce Saturna zawiera ciekłe mieszaniny zawierające ten gaz na swojej powierzchni. Również metan jest jednym ze składników atmosfery dużych planet. Najwyższą zawartość metanu obserwuje się w gazach naturalnych, kopalnianych i bagiennych. W warunkach przemysłowych gaz wytwarza się przez uwodornienie i koksowanie węgla.
Metan jest również produkowany w laboratoriach. Jednym ze sposobów jego uzyskania jest ogrzewanie kwasu octowego i wodorotlenku sodu (lub wapna). Ta ostatnia substancja jest również połączona z octanem w wyniku topienia, w wyniku czego powstaje również metan. Obie metody nie wymagają obecności wody. Trzeci sposób wytwarzania gazu to hydroliza, której podlega węglik glinu. W tym przypadku metan powstaje szybciej. Metoda hydrolizy jest również tańsza, ponieważ nie wymaga ekspozycji na wysokie temperatury.
Zastosowania węglika aluminium w chemii przemysłowej

Oprócz hydrolizy związku można go również stosować jako odczynnik. Takie zastosowanie węglika glinu jest niezbędne do określenia zawartości niektórych substancji. W szczególności możliwe jest wykrycie cennego gazu - trytu, który jest obecny w wodzie. Ponadto sól z kombinacji może być wykonana z węglika glinu. Otrzymuje się go, podobnie jak metan, przez połączenie substancji z wodą. Sól ta jest nazywana tetrahydroksaluminianem sodu. Konieczne jest nadanie koloru tkaninom. Produkcja i stosowanie węglika jest bardzo ważne dla różnych gałęzi przemysłu, więc koszt jego uzyskania jest dość duży. Środki na zakup substancji są przydzielane przez państwo.