Właściwości chemiczne wodoru: cechy i zastosowanie
Zastanów się, co stanowi wodór. Podczas kursu badane są właściwości chemiczne i przygotowanie tego niemetalu. chemia nieorganiczna w szkole. Na czele tego elementu stoi układ okresowy Mendelejewa, dlatego zasługuje on na dokładny opis.

Szczegóły otwarcia przedmiotu
Przed rozważeniem właściwości fizycznych i chemicznych wodoru, dowiedzieliśmy się, jak ten ważny element został znaleziony.
Chemicy, którzy pracowali w XVI i XVII wieku, wielokrotnie wspominali w swoich pismach o gazie palnym, który jest uwalniany, gdy jest wystawiony na działanie aktywnych metali. W drugiej połowie XVIII wieku G. Cavendish był w stanie zebrać i przeanalizować ten gaz, nadając mu nazwę "gaz palny".
W tym czasie nie badano fizycznych i chemicznych właściwości wodoru. Dopiero pod koniec XVIII wieku A. Lavoisier udowodnił przez analizę, że możliwe było uzyskanie tego gazu przez analizę wody. Nieco później zaczął nazywać nowy element hydrogene, co oznacza "rodzenie wody". Wodór zawdzięcza swoje współczesne rosyjskie imię M.F. Solov'ev.
Będąc w naturze
Właściwości chemiczne wodoru można analizować tylko na podstawie jego występowania w przyrodzie. Ten pierwiastek występuje w hydro - i litosferze, a także jest częścią minerałów: gazu naturalnego i związanego, torfu, oleju, węgla, palenisko łupkowe. Trudno wyobrazić sobie dorosłego, który nie wiedziałby, że wodór jest integralną częścią wody.
Ponadto, ten niemetal znajduje się u zwierząt w postaci kwasów nukleinowych, białek, węglowodanów, tłuszczów. Na naszej planecie ten pierwiastek występuje raczej w wolnej postaci, być może tylko w gazie naturalnym i wulkanicznym.
W postaci plazmy wodór odpowiada za około połowę masy gwiazd i słońca, ponadto jest częścią gazu międzygwiezdnego. Na przykład w postaci wolnej, a także w postaci metanu, amoniaku, ten niemetal jest obecny w składzie komet, a nawet niektórych planet.
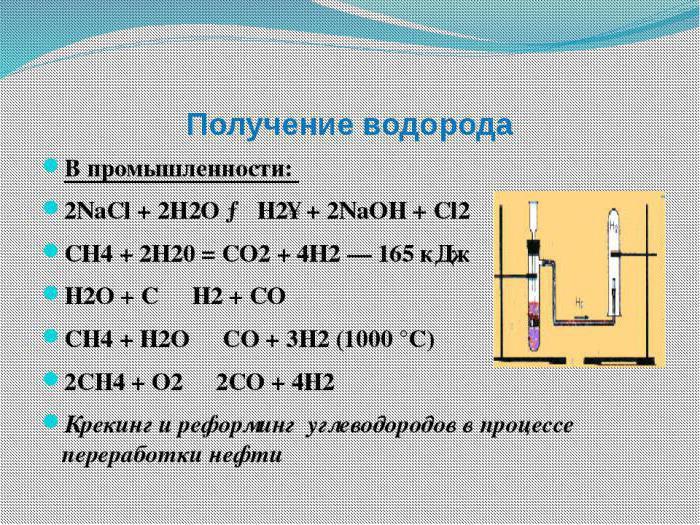
Właściwości fizyczne
Przed rozważeniem chemicznych właściwości wodoru, zauważamy, że w normalnych warunkach jest to substancja gazowa lżejsza od powietrza, mająca kilka postaci izotopowych. Jest prawie nierozpuszczalny w wodzie, ma wysoką przewodność cieplną. Protium, o masie 1, jest uważane za najprostszą formę. Tryt, który ma właściwości radioaktywne, powstaje w przyrodzie z atmosferycznego azotu po wystawieniu na działanie neuronów promieniowania UV.
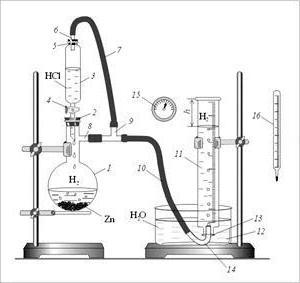
Cechy struktury cząsteczki
Aby rozpatrzyć właściwości chemiczne wodoru, charakterystyczne dla niego reakcje będą dotyczyć osobliwości jego struktury. W tej dwuatomowej cząsteczce kowalencyjny niepolarny wiązanie chemiczne. Tworzenie się atomowego wodoru jest możliwe dzięki oddziaływaniu aktywnych metali z kwasowymi roztworami. Ale w tej formie, ten niemetal jest w stanie istnieć tylko przez nieznaczny okres czasu, niemal natychmiast rekombinuje się w formę molekularną.

Właściwości chemiczne
Rozważ chemiczne właściwości wodoru. W większości związków, które tworzy ten pierwiastek chemiczny, wykazuje on stopień utlenienia +1, co czyni go podobnym do aktywnego (alkaliczne) metale. Główne właściwości chemiczne wodoru, charakteryzujące go jako metal:
- interakcja z tlenem w celu utworzenia wody;
- reakcja z halogenami, której towarzyszy tworzenie halogenowodoru;
- uzyskiwanie siarkowodoru w połączeniu z siarką.
Poniżej znajduje się równanie reakcji charakteryzujących właściwości chemiczne wodoru. Zwracamy uwagę, że jako niemetalowy (ze stanem oksydacyjnym -1) działa on tylko w reakcji z aktywnymi metalami, tworząc z nimi odpowiednie wodorki.
Wodór w normalnej temperaturze nieaktywnie wchodzi w interakcję z innymi substancjami, więc większość reakcji prowadzi się dopiero po wstępnym ogrzaniu.
Przyjrzyjmy się bliżej niektórym interakcjom chemicznym pierwiastka, który przewodzi okresowym tablicom pierwiastków chemicznych Mendelejewa.
Reakcji tworzenia wody towarzyszy wydzielanie 285,937 kJ energii. W podwyższonych temperaturach (ponad 550 stopni Celsjusza) procesowi temu towarzyszy silna eksplozja.
Wśród tych chemicznych właściwości wodoru gazowego, które znalazły znaczące zastosowanie w przemyśle, interesujące jest jego oddziaływanie z tlenkami metali. W wyniku katalitycznego uwodornienia w nowoczesnym przemyśle przetwarzane są tlenki metali, na przykład czysty metal jest ekstrahowany z tlenku żelaza (mieszany tlenek żelaza). Ta metoda pozwala na wydajną obróbkę złomu.
Synteza amoniaku, który obejmuje oddziaływanie wodoru z powietrznym azotem, jest również pożądana w nowoczesnym przemyśle chemicznym. Wśród warunków występowania tego oddziaływania chemicznego, zwracamy uwagę na ciśnienie i temperaturę.

Wniosek
W normalnych warunkach jest to wodór, który jest chemikaliami o niskim poziomie. Wraz ze wzrostem temperatury jego aktywność znacznie wzrasta. Ta substancja jest potrzebna w syntezie organicznej. Na przykład, poprzez uwodornienie, ketony można zredukować do drugorzędowych alkoholi, a aldehydy można przekształcić w pierwszorzędowe alkohole. Ponadto, poprzez uwodornienie, możliwe jest przekształcenie nienasyconych węglowodorów z klasy etylenu i acetylenu w związki graniczne z szeregu metanowego. Wodór słusznie uważany jest za prostą substancję popytową w nowoczesnej produkcji chemicznej.