Chemia. Systemy rozproszone - co to jest?
W naturze dość trudno jest znaleźć czystą substancję. W różnych stanach mogą tworzyć mieszaniny, homogeniczne i niejednorodne - systemy i roztwory zdyspergowane. Jakie są te połączenia? Jakie one są? Rozważ te pytania bardziej szczegółowo. 
Terminologia
Najpierw musisz zrozumieć, czym są systemy rozproszone. Według tej definicji rozumie się struktury heterogeniczne, w których jedna substancja jako najmniejsze cząstki jest równomiernie rozmieszczona w większej części. Składnik obecny w mniejszej ilości nazywany jest fazą rozproszoną. Może zawierać więcej niż jedną substancję. Komponent obecny w większej objętości nazywany jest medium. Pomiędzy cząstkami fazy i nią znajduje się interfejs. Pod tym względem systemy rozproszone są nazywane heterogenicznymi - heterogenicznymi. Zarówno medium, jak i faza mogą być reprezentowane przez substancje w różnych stanach agregacji: ciekłe, gazowe lub stałe.
Systemy rozproszone i ich klasyfikacja
W zależności od wielkości cząstek wchodzących w fazę substancji, rozróżnia się zawiesiny i struktury koloidalne. W pierwszym przypadku wielkość pierwiastków wynosi więcej niż 100 nm, aw drugim - od 100 do 1 nm. Kiedy substancja zostanie zmiażdżona na jony lub cząsteczki, których jasność jest mniejsza niż 1 nm, powstaje roztwór - układ jednorodny. Różni się od innych swoją jednorodnością i brakiem granicy między medium a cząstkami. Układy koloidalne rozpraszające są przedstawione w postaci żeli i zoli. Z kolei zawiesiny są podzielone na zawiesiny, emulsje, aerozole. Istnieją rozwiązania jonowe, molekularne jonowe i molekularne. 
Ważenie
Te zdyspergowane układy obejmują substancje o wielkości cząstek większej niż 100 nm. Struktury te są nieprzejrzyste: ich poszczególne elementy można zobaczyć gołym okiem. Pożywkę i fazę można łatwo oddzielić stojąc. Co to jest zawieszenie? Mogą być ciekłe lub gazowe. Pierwsze są podzielone na zawiesiny i emulsje. Te ostatnie są strukturami, w których medium i faza są cieczami, które są nierozpuszczalne w sobie. Należą do nich na przykład limfa, mleko, farba na bazie wody i inni. Zawiesina jest strukturą, w której podłoże jest cieczą, a faza jest stałą, nierozpuszczalną substancją. Takie rozproszone układy są dobrze znane wielu. Należą do nich w szczególności "mleko wapienne", szlam morski lub rzeczny zawieszony w wodzie, mikroskopijne organizmy żywe rozmieszczone w oceanie (plankton) i inne.
Aerozole
Te zawiesiny są rozprowadzane w gazie drobnymi cząstkami cieczy lub ciała stałego. Są mgły, dym, kurz. Pierwszy typ to dystrybucja małych kropelek cieczy w gazie. Pył i dym są zawieszonymi ciałami stałymi. W tym przypadku pierwsze cząstki są nieco większe. Do naturalnych aerozoli niesie się burzowa chmura, właściwa mgła. Smog zawisł nad dużymi miastami przemysłowymi, składającymi się z stałych i płynnych składników rozprowadzanych w gazie. Należy zauważyć, że aerozole, jako systemy rozproszone, mają duże znaczenie praktyczne, wykonują ważne zadania w działalności przemysłowej i domowej. Przykłady pozytywnego wyniku ich zastosowania obejmują leczenie układu oddechowego (inhalacja), chemiczne traktowanie pól, natryskiwanie farby pistoletem natryskowym. 
Struktury koloidalne
Są to systemy zdyspergowane, w których faza składa się z cząstek w zakresie od 100 do 1 nm. Takie elementy nie są widoczne gołym okiem. Faza i medium w tych strukturach za pomocą sedymentacji są oddzielone z trudnościami. Sols (roztwory koloidalne) znajdują się w żywej komórce iw ciele jako całości. Płyny te obejmują soki jądrowe, cytoplazmę, limfę, krew i inne. Te systemy dyspergujące tworzą skrobię, kleje, niektóre polimery, białka. Struktury te można uzyskać poprzez reakcje chemiczne. Na przykład podczas interakcji rozwiązań krzemian sodu lub potas z kwasowymi związkami tworzą związek kwasu krzemowego. Zewnętrznie struktura koloidalna jest podobna do tej prawdziwej. Jednak te pierwsze odróżniają się od tych drugich obecnością "świetlistej ścieżki" - stożka, gdy przechodzi przez nie wiązka światła. Sols zawierają większe cząstki fazy niż w prawdziwych roztworach. Ich powierzchnia odbija światło - aw naczyniu obserwator może zobaczyć świetlisty stożek. W prawdziwym rozwiązaniem tego zjawiska nie jest. Podobny efekt można zaobserwować także w kinie. W tym przypadku wiązka światła przechodzi nie przez ciecz, ale koloid w aerozolu - powietrze w pomieszczeniu. 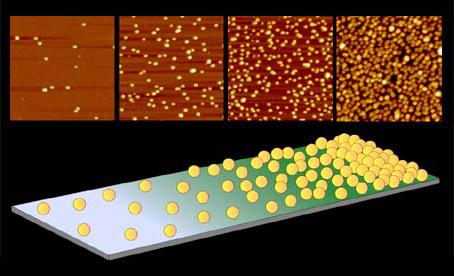
Odkładanie cząstek
W roztworach koloidalnych cząstki fazy często nie osiadają nawet podczas długotrwałego przechowywania, co jest związane z ciągłymi zderzeniami z cząsteczkami rozpuszczalnika pod wpływem ruchu termicznego. Zbliżając się do siebie, nie trzymają się razem, ponieważ na ich powierzchniach są takie same ładunki elektryczne. Jednak w pewnych okolicznościach może wystąpić proces koagulacji. Jest to efekt sklejania i wytrącania cząstek koloidalnych. Proces ten obserwuje się, gdy ładunki są neutralizowane na powierzchni elementów mikroskopowych po dodaniu elektrolitu. W takim przypadku roztwór zamienia się w żel lub zawiesinę. W niektórych przypadkach obserwuje się proces koagulacji podczas ogrzewania lub w przypadku zmiany równowagi kwasowo-zasadowej.
Żele
Te koloidalne układy dyspersyjne są galaretowatymi osadami. Powstają podczas koagulacji zolu. Struktury te obejmują liczne żele polimerowe, kosmetyki, wyroby cukiernicze, substancje medyczne (ciasto "Ptasie mleko", marmolada, galaretka, galaretka, żelatyna). Obejmują one również naturalne struktury: opal, korpusy meduzy, włosy, ścięgna, tkankę nerwową i mięśniową, chrząstkę. Rozwój życia na Ziemi może być w rzeczywistości uważany za historię ewolucji układu koloidalnego. Z czasem dochodzi do naruszenia struktury żelu, a woda zaczyna się od niego odróżniać. Zjawisko to nazywane jest synerezą. 
Systemy homogeniczne
Roztwory obejmują dwie lub więcej substancji. Są zawsze jednofazowe, to znaczy są stałe, gazowe lub płynne. W każdym razie ich struktura jest jednorodna. Efekt ten tłumaczy się tym, że w jednej substancji inny jest rozprowadzany w postaci jonów, atomów lub cząsteczek, których wielkość jest mniejsza niż 1 nm. W przypadku, gdy konieczne jest podkreślenie różnicy między roztworem a koloidalną strukturą, nazywa się to prawdą. W procesie krystalizacji ciekłego stopu złota i srebra uzyskuje się stałe mieszane struktury. 
Klasyfikacja
Mieszaniny jonowe to struktury o silnych elektrolitach (kwasy, sole, zasady - NaOH, HC104 i inne). Innym rodzajem są układy rozpraszania molekularno-jonowego. Zawierają silny elektrolit (siarkowodór, kwas azotowy i inne). Ostatnim typem są roztwory molekularne. Struktury te obejmują nieelektrolity - substancje organiczne (sacharoza, glukoza, alkohol itp.). Rozpuszczalnik jest składnikiem, którego stan skupienia nie zmienia się po utworzeniu roztworu. Takim elementem może być na przykład woda. W roztworze soli, dwutlenku węgla, cukru działa jako rozpuszczalnik. W przypadku mieszania gazów, cieczy lub ciał stałych, rozpuszczalnik będzie składnikiem, który będzie większy w związku.