Chromatograficzne metody analizy: zalety i wady
Analiza chromatograficzna jest dziś najszerzej stosowaną metodą badania różnych obiektów. Mogą to być próbki pobrane w środowisku, w pracy, w laboratorium i tak dalej. Metodę tę zaproponował w 1903 r. Rosyjski naukowiec M. S. Tsvet. Jego badania stały się podstawą rozwoju wszystkich istniejących dziś technik chromatografii i służą do oddzielania nie tylko barwnych, ale także nie wybarwionych związków we wszystkich środowiskach. Przeprowadzenie analizy chromatograficznej jest możliwe na różne sposoby, z wykorzystaniem w każdym przypadku własnych technik i metod obliczeniowych. Opiera się na różnicach w adsorpcji lub innych właściwościach związków, co przyczynia się do ich dystrybucji między stałym sorbentem a przechodzącym przez niego płynem (lub gazem).
Ad

Podstawowe pojęcia
Chromatograficzna metoda analizy odnosi się do takiej metody separacji i oznaczania substancji, która opiera się na rozkładzie kilku składników próbki między dwiema fazami, z których jedna jest ruchoma, a druga jest ustalona.
Faza stacjonarna (stacjonarna) jest zwykle porowatą substancją stałą (zwykle określaną jako sorbent) lub folią cieczy, która osadza się na stałej substancji.
Faza ruchoma jest ciekłą lub gazową substancją przepływającą przez fazę stacjonarną, czasami pod ciśnieniem. Wszystkie składniki analizowanej mieszaniny (zwane sorbatami) wraz z fazą ruchomą poruszają się wzdłuż fazy stacjonarnej. Z reguły umieszcza się go w szklanej (metalowej) tubie - kolumnie.
Ad
Szybkość ruchu składników wzdłuż kolumny zależy od stopnia ich interakcji z powierzchnią sorbentu. Prowadzi to do tego, że niektóre składniki pozostaną w górnej części kolumny, rozproszone w objętości sorbentu, inne w dolnej części, a niektóre nie zostaną w nim całkowicie i odejdą wraz z fazą ruchomą.
Klasyfikacja chromatograficznych metod analizy
Te metody badań substancji są tak różnorodne, że nie ma jednej ich klasyfikacji. Zwykle są one podzielone przez następujące cechy:
- stan skupienia sorbentu i fazy ruchomej;
- mechanizm substancji wiążących i sorbentu;
- technika analizy;
- sposób przemieszczania próbki przez kolumnę;
- cel analizy.
Zgodnie z zagregowanym stanem faz
Zgodnie z tą cechą metody analizy chromatograficznej dzieli się na:
- chromatografia gazowa, jeśli fazą ruchomą jest para lub gaz;
- chromatografia cieczowa, gdy faza ruchoma znajduje się w stanie ciekłym.
Pierwszy jest zwykle używany do oddzielania lotnych termicznie stabilnych związków o ciężarze cząsteczkowym do 300. Drugi jest odpowiedni do oddzielania składników organicznych i nieorganicznych, które mają ciężar cząsteczkowy do 2000, nawet jeśli są niestabilne termicznie.
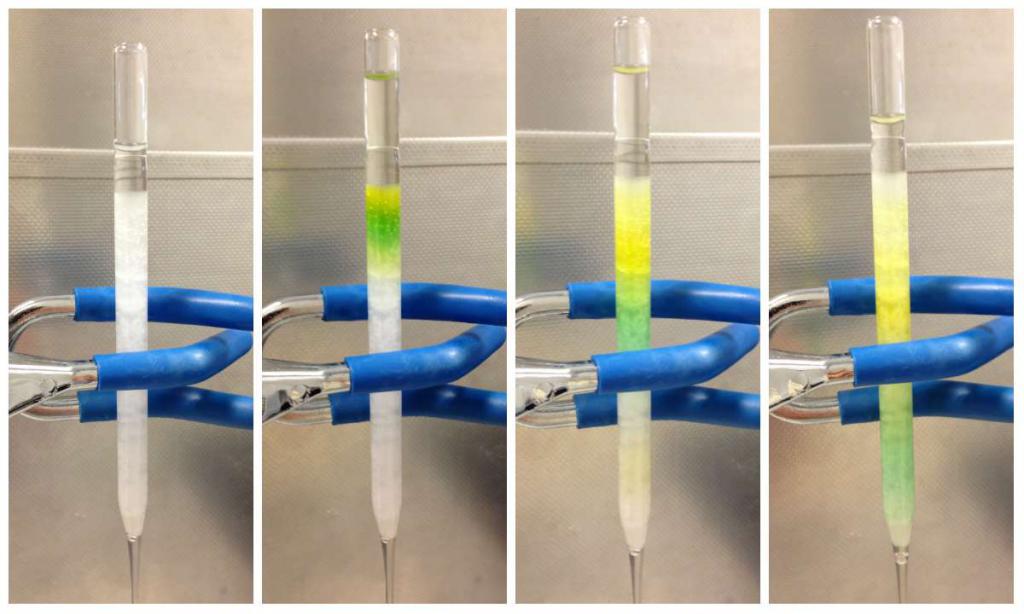
Z natury interakcji substancji z fazą stacjonarną
Zgodnie z mechanizmem działania sorbentu z substancją chromatograficzne metody analizy mogą być następujące:
- adsorpcja, jeżeli rozdział jest oparty na różnicach w powinowactwie składników próbki do powierzchni adsorbentu;
- rozdzielcze, jeżeli rozdzielanie substancji oparte jest na różnicach w ich rozpuszczalności w fazie ruchomej i sorbencie;
- wymiana jonowa, jeśli separacja jest oparta na różnicach w zdolności składników do przeprowadzenia wymiany jonowej;
- penetrujące, jeśli nastąpi rozdzielenie substancji z powodu różnic w wielkości i kształcie cząsteczek, a także ładunków.
Ponadto, metody chromatograficzne analizy są klasyfikowane według tej metody do sedymentacji, redox, tworzenia kompleksów i innych.
Zgodnie z techniką eksperymentu
Zgodnie z metodą przetwarzania chromatografia procesowa to:
- kolumnę, w której rozdzielanie prowadzi się w kolumnach wypełnionych sorbentem.
- płaski, który można przeprowadzić na papierze lub na płytkach (chromatografia cienkowarstwowa).
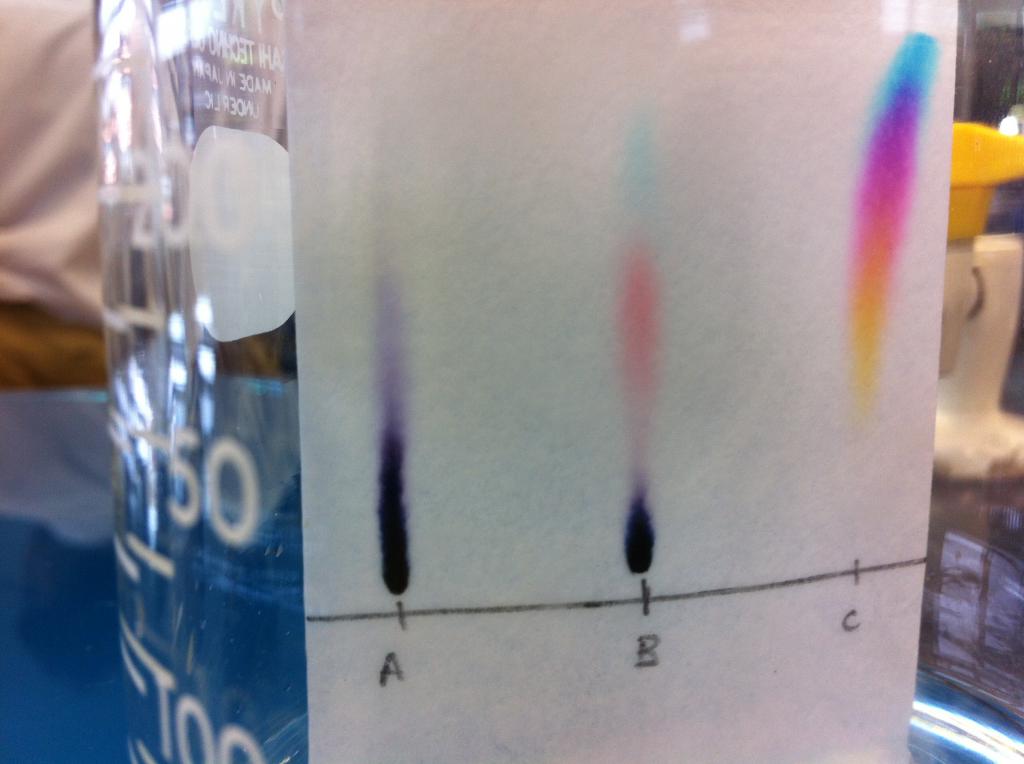
Do tej listy można również dodać metody analizy chromatograficznej przeprowadzonej przy użyciu kapilar. Wewnętrzna średnica takich rur nie jest większa niż 1 mm. W porównaniu z innymi rodzajami chromatografii pozwala to na zwiększenie szybkości analizy i umożliwia badanie drogich gazów lub sorbentów. Ponadto niewielki rozmiar kolumny umożliwia połączenie tego badania ze spektrometrią mas. Jednak istotną wadą chromatograficznej metody analizy tego rodzaju jest trudność wprowadzenia próbki do kapilary.
O ruchu materii
Ta cecha jest również nazywana metodą chromatografii. Istnieją:
- Eluent Chromatografia. Najlepiej nadaje się do rozwiązywania problemów analitycznych. Polega ona na tym, że mieszanina substancji wprowadzana do ciągle poruszającego się strumienia eluentu jest sorbowana lepiej niż faza ruchoma. Podczas postępu eluentu wzdłuż kolumny ze składnikami sorbowanymi, zaczynają one przemieszczać się wzdłuż sorbentu z różnymi prędkościami i opuszczają kolumnę w oddzielnych frakcjach (strefach). Zaletami metody rozwojowej są bardziej kompletne oddzielenie substancji, ciągła regeneracja sorbentu i dobra powtarzalność parametrów retencji.
- Chromatografia dysymetryczna. Polega ona na tym, że podzielona próbka jest wprowadzana do fazy ruchomej, a następnie propelent, który ma pojemność sorpcyjną większą niż wszystkie pozostałe, zaczyna przechodzić. W trakcie postępu wzdłuż kolumny wypiera wcześniej sorbenty z sorbentu w celu zwiększenia ich pojemności sorpcyjnej.
- Czołowa chromatografia. Podczas badania analizowana mieszanina jest również przepuszczana przez warstwę sorbentu. A podczas wypełniania kolumny komponentami stopniowo wychodzą, aby zwiększyć ich zdolność sorpcji.
Przez cel pracy
Klasyfikacja chromatograficznych metod analizy w zależności od celu procesu jest następująca:
- chromatografia analityczna - jest osobną metodą, obejmującą rozdzielenie próbki na składniki, a także ich analizę jakościową i ilościową;
- Chromatografia preparatywna służy wyłącznie do rozdzielania mieszaniny substancji.
Zalety metody
Analiza chromatograficzna ma następujące zalety w stosunku do innych metod separacji i badań substancji:
- Ze względu na fakt, że ta metoda separacji ma charakter dynamiczny, charakteryzujący się powtarzalnym powtarzaniem sorpcji-desorpcji, jej wydajność jest znacznie wyższa niż w przypadku sorpcji statycznej lub ekstrakcji.
- Zastosowanie różnych rodzajów oddziaływań sorbinianów i sorbentów (fizycznej i chemisorpcji) pozwala rozszerzyć zakres substancji do selektywnej separacji.
- Niektóre techniki przewidują nakładanie pól grawitacyjnych, magnetycznych i innych na emitowane substancje, co rozszerza możliwości chromatografii poprzez zmianę warunków rozdziału składników.
- Ta metoda jest hybrydowa, ponieważ łączy separację i definicję kilku składników naraz.
- Chromatografia umożliwia jednoczesne rozwiązywanie kilku problemów. Zadania analityczne obejmują zatem separację, identyfikację i oznaczanie substancji, a preparatywne - ich oczyszczanie, izolację i zatężanie.

Funkcje chromatograficzne
Wysokosprawna i wysoce selektywna chromatografia preparatywna jest niezbędna do rozdzielenia złożonych próbek zawierających dużą liczbę pojedynczych związków o podobnych parametrach fizykochemicznych (olej, wszystkie rodzaje leków, ekstrakty z roślin, płyny biologiczne i inne). Zatem metody gazowe do analizy chromatograficznej są szeroko stosowane do oczyszczania substancji chemicznych lub izolowania poszczególnych związków w chemii preparatywnej. Do ekstrakcji jonowej odpowiednia jest chromatografia jonowymienna w oparciu o różnice w zdolności jonów z roztworu do wymiany procesów z wymieniaczem jonowym.
Nowoczesne metody chromatograficzne umożliwiają oznaczanie substancji gazowych, ciekłych i stałych. Wybór warunków analizy koncentruje się na charakterze i składzie analizowanej próbki. Adsorpcja gazu i chromatografia gazowo-cieczowa umożliwiają badanie substancji lotnych odpornych na ciepło. Zatem chromatografia adsorpcyjna jest szeroko stosowana do analizy mieszanin gazów i niskowrzących węglowodorów, które nie mają aktywnych grup funkcyjnych. Chromatografia gazowo-cieczowa jest ważna w petrochemii, analizie pestycydów i nawozów, leków.
Ad
Analiza chromatograficzna oleju transformatorowego pozwala na szybkie wykrycie wad lub charakteru i stopnia uszkodzenia transformatora. Jego stan ocenia się przez porównanie danych uzyskanych podczas analizy z wartościami dopuszczalnymi, a także szybkości zmiany zawartości gazu w oleju. Zatem wysoka zawartość CO i CO 2 zwykle sygnalizuje naruszenia izolacji celulozowej. Ale obecność pochodnych furanu sugeruje starzenie się izolacji papierowej. Analiza chromatograficzna gazów przyczynia się do bezpiecznej i długotrwałej pracy urządzenia.
Chromatografia gazowa
Jest to jedna z najczęstszych odmian tej metody, ze względu na to, że opracowano dla niej różne techniki z pełnym teoretycznym uzasadnieniem, a także istnieje niezawodne i stosunkowo niedrogie oprzyrządowanie. Faza ruchoma (gaz nośny) to gazy lub ich mieszaniny, a także substancje, które są gazami w warunkach, w których przeprowadzana jest analiza. Faza stacjonarna to stałe sorbenty (metoda adsorpcji gazu) lub ciecz na powierzchni obojętnego nośnika (metoda gaz-ciecz).
Ad
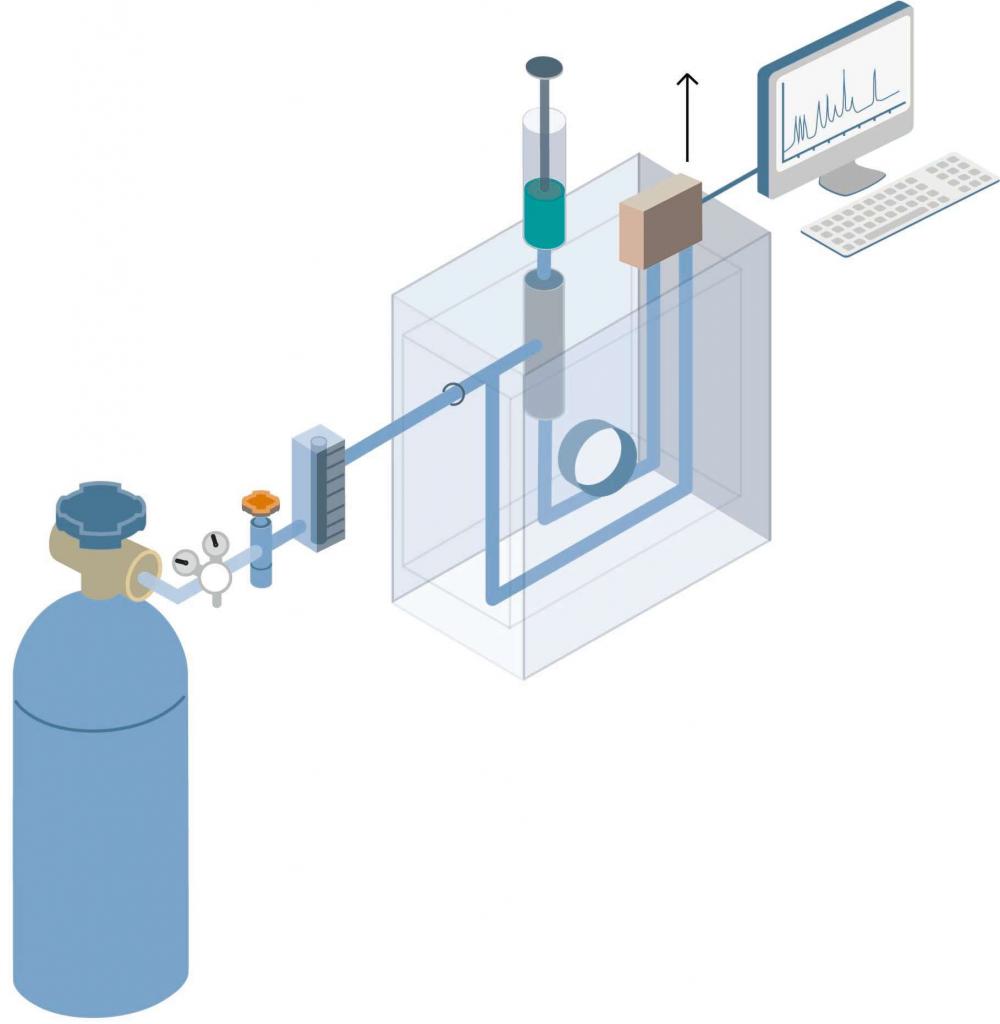
Do chromatografii gazowej można dodatkowo wymienić szereg zalet:
- duża prędkość procesu;
- zdolność do analizy mikroplastrów;
- automatyczne rejestrowanie wyników wraz z dostępnością odpowiedniego sprzętu;
- możliwość izolowania komponentów nie tylko w laboratorium, ale także na skalę przemysłową.
Chromatografia papierowa
Jako fazę stacjonarną stosuje się filtr lub specjalny papier chromatograficzny. Ta ostatnia jest papierową bibułką celulozową o wysokiej czystości i pewnych szczególnych właściwościach. Absorbuje rozpuszczalnik przy różnych prędkościach podnoszenia kapilarnego, w zależności od gęstości papieru.
Głównym wyposażeniem są specjalne komory lub naczynia, tace umieszczone na stojakach, pipety, rozpylacze, lampy do chromatogramów, urządzenia pomiarowe, a także planimetry i densytometry stosowane do oznaczeń ilościowych.
Ad
Metoda ta najlepiej nadaje się do analizy różnych substancji organicznych zawierających różne grupy funkcyjne, od alkoholi po sterydy, od amin do indoli, od witamin po antybiotyki.
Chromatografia jonowymienna
Ta metoda opiera się na wymianie jonów między spęcznionym wymieniaczem jonowym a fazą ruchomą. Wymiana jonowymienna mieszaniny jonów charakteryzuje się różnicą w ich ładunkach i siłą jonową roztworu. W objętości ziaren jonitu proces rozdzielania zależy również od szybkości dyfuzji jonów, która jest określona przez gęstość wymieniacza jonowego.
Jonit jest wybierany za pomocą parametru o nazwie powinowactwo, który jest proporcjonalny do ładunku jonu i odwrotnie proporcjonalny do promienia uwodnionego jonu. Wybór wymieniacza jonowego przeprowadza się przy użyciu tablic o zadanej charakterystyce typów wytwarzanych wymieniaczy jonowych. Ich głównymi cechami są wielkość i kształt ziarna, pojemność wymiany, właściwości kwasowo-zasadowe, pęcznienie, gęstość.
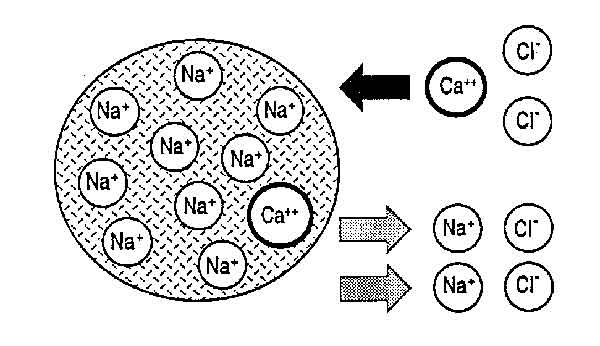
Rozdzielanie nieorganicznych substancji odbywa się na nieorganicznych wymieniaczach jonowych (zeolitach, wodorotlenkach glinu) lub żywicach (styren z diwinylobenzenem). Dlatego chromatograficzna metoda analizy wody pod kątem obecności w niej różnych jonów jest często stosowana, na przykład, do określenia jej twardości.
Chromatografia żelowa
Istotą metody jest to, że analizowany roztwór jest powoli filtrowany przez kolumny wypełnione żelem. Czasami nazywa się to filtracją żelową. Poszczególne cząstki żelu składają się z plastycznych liniowych cząsteczek substancji o najwyższej masie cząsteczkowej, połączonych wiązaniami poprzecznymi. Taka struktura siatkowa przyczynia się do pęcznienia żelu w wodzie i pojawiania się w nim porów o różnych średnicach. Wielkość porów zależy od rodzaju polimeru, temperatury medium i rodzaju rozpuszczalnika.
Separacja opiera się na zdolności mniejszych cząsteczek do penetracji głębiej w pory i pozostania tam przez dłuższy czas. Dlatego na początku większe cząsteczki opuszczają kolumnę, a następnie te, które są mniejsze.

Metoda ta wykonuje dwa rodzaje separacji: grupowanie i frakcjonowanie. Pierwszy charakteryzuje się oddzieleniem mieszaniny składników zgodnie z ich masą cząsteczkową. Po drugie, pod względem szybkości i intensywności dyfuzji cząstek wewnątrz żelu. Najczęściej stosowana chromatografia żelowa w biochemii, w syntezie organicznej i chemii polimerów do oznaczania mas cząsteczkowych. Przykładowo możliwa jest chromatograficzna analiza białek i peptydów w osoczu. W porównaniu ze sposobami spektrometrii masowej, śledząca homeostaza białkowo-peptydowa w dystrybucji białek i ich produktów degradacji za pomocą chromatografii żelowej jest znacznie bardziej dostępna.