Jak określić stopień utlenienia atomu pierwiastka chemicznego
Formalny ładunek atomu w związkach jest wartością pomocniczą, używaną zwykle w opisach właściwości pierwiastków w chemii. To warunkowe ładunek elektryczny i istnieje stan utlenienia. Jego wartość zmienia się w wyniku wielu procesów chemicznych. Chociaż ładunek jest formalny, żywo opisuje właściwości i zachowanie atomów w reakcje redoks (OVR).
Utlenianie i redukcja
W przeszłości chemicy używali określenia "utlenianie", aby opisać interakcję tlenu z innymi pierwiastkami. Nazwa reakcji pochodzi od łacińskiej nazwy tlenu - Oxygenium. Później okazało się, że inne pierwiastki również są utlenione. W tym przypadku zostają przywrócone - dołączają elektrony. Każdy atom w tworzeniu cząsteczki zmienia strukturę jej powłoki elektronowej walencyjnego. W tym przypadku pojawia się opłata formalna, której wartość zależy od liczby warunkowo podanych lub otrzymanych elektronów. W celu scharakteryzowania tej wartości wykorzystano wcześniej angielski chemiczny termin "numer utleniania", co oznacza "liczbę utleniającą". Podczas jego stosowania zakłada się, że elektrony wiążące w cząsteczkach lub jonach należą do atomu o wyższej wartości elektroujemności (EO). Zdolność do trzymania swoich elektronów i przyciągania ich z innych atomów dobrze wyraża się w silnych niemetaliach (halogenach, w tlenie). Właściwości przeciwne mają silne metale (sód, potas, lit, wapń, inne pierwiastki alkaliczne i pierwiastki ziem alkalicznych).
Ad
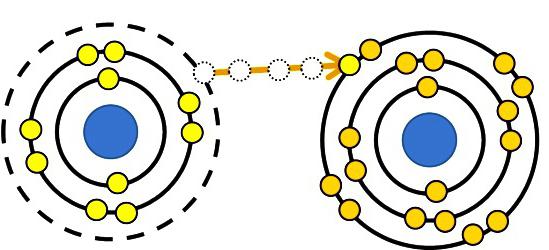
Oznaczenie stopnia utlenienia
Stan utleniania odnosi się do ładunku, który uzyskałby atom, gdyby elektrony biorące udział w tworzeniu wiązania zostały całkowicie przesunięte do bardziej elektroujemnego elementu. Istnieją substancje, które nie mają struktury molekularnej (halogenki metale alkaliczne i inne związki). W tych przypadkach stopień utlenienia pokrywa się z ładunkiem jonów. Opłata warunkowa lub rzeczywista wskazuje, który proces nastąpił, zanim atomy uzyskały swój obecny stan. Dodatnią wartością stopnia utlenienia jest całkowita liczba elektronów, które zostały usunięte z atomów. Ujemna wartość stopnia utlenienia to liczba nabytych elektronów. Zmieniając stan utleniania pierwiastka chemicznego, ocenia się, co dzieje się z jego atomami podczas reakcji (i na odwrót). Kolor substancji określa, jakie zmiany zaszły w stanie utlenienia. Związki chromu, żelaza i wielu innych pierwiastków, w których wykazują różne walencyjności, są inaczej zabarwione.
Ad
Ujemne, zerowe i dodatnie wartości stopnia utlenienia

Proste substancje są tworzone przez pierwiastki chemiczne o tej samej wartości EO. W tym przypadku elektrony wiążące należą jednakowo do wszystkich cząstek strukturalnych. Dlatego w przypadku substancji prostych stan utlenienia (H 0 2 , O 0 2 , C 0 ) jest niezwykły dla pierwiastków. Kiedy atomy akceptują elektrony lub powszechna chmura przesuwa się w ich kierunku, zwykle zapisuje się ładunki ze znakiem minus. Na przykład F -1 , O -2 , C- 4 . Poprzez darowanie elektronów atomy nabywają rzeczywisty lub formalny ładunek dodatni. W tlenku OF 2 atom tlenu daje jeden elektron do dwóch atomów fluoru i znajduje się w stanie utlenienia O + 2 . Uważa się, że w cząsteczce lub jonie wieloatomowym więcej atomów elektroujemnych przyjmuje wszystkie elektrony wiążące.
Ad
Siarka - pierwiastek wykazujący różne wartościowości i stany utleniania
Pierwiastki chemiczne głównych podgrup często wykazują niższą wartościowość równą VIII. Na przykład wartość siarki w siarkowodorze i siarczkach metali - II. Element charakteryzuje się pośrednią i wyższą wartościowością w stanie wzbudzonym, gdy atom oddaje jeden, dwa, cztery lub wszystkie sześć elektronów i wykazuje odpowiednio wartościowości I, II, IV, VI. Te same wartości, tylko ze znakiem "minus" lub "plus", mają stopień utlenienia siarki:
- jeden elektron w siarczku fluoru daje: -1;
- w siarkowodorze najniższa wartość: -2;
- Dwutlenkowy stan przejściowy: +4;
- w trójtlenku, kwas siarkowy i siarczany: +6.
W najwyższym stopniu utlenienia siarka akceptuje tylko elektrony, w najniższym stopniu wykazuje silne właściwości redukujące. Atomy S + 4 mogą manifestować funkcje redukujące lub utleniające w związkach, w zależności od warunków.
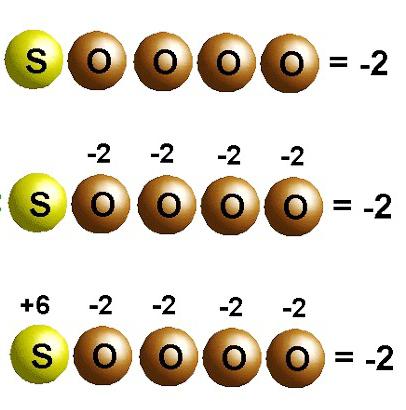
Przejście elektronów w reakcjach chemicznych
Gdy powstaje chlorek sodu, sód oddaje elektrony do bardziej elektroujemnego chloru. Stany utlenienia pierwiastków pokrywają się z ładunkami jonowymi: Na +1 Cl -1 . W przypadku cząsteczek utworzonych przez uspołecznienie i przemieszczenie par elektronów do bardziej elektroujemnego atomu, zastosowanie mają tylko pojęcia opłaty formalnej. Można jednak założyć, że wszystkie związki składają się z jonów. Następnie atomy, przyciągające elektrony, nabywają warunkowy ładunek ujemny i dają pozytyw. W reakcjach zaznacz, ile elektronów zostało przesuniętych. Na przykład w cząsteczce dwutlenku węgla С +4 О - 2 2 indeks w górnym prawym rogu z symbolem chemicznym węgla pokazuje liczbę elektronów usuniętych z atomu. Dla tlenu w tej substancji charakteryzuje się stan utlenienia -2. Odpowiedni indeks na znaku chemicznym O to liczba dodanych elektronów w atomie.
Ad
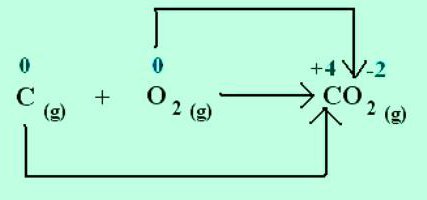
Jak obliczyć stopień utlenienia
Zliczanie liczby elektronów oddanych i przyłączonych przez atomy może być czasochłonne. Poniższe reguły ułatwiają to zadanie:
- W przypadku substancji prostych stany utleniania wynoszą zero.
- Suma utleniania wszystkich atomów lub jonów w substancji neutralnej wynosi zero.
- W złożonym jonie suma stanów utlenienia wszystkich pierwiastków musi odpowiadać ładunkowi całej cząstki.
- Bardziej elektroujemny atom uzyskuje stan ujemnego utleniania, który jest zapisany ze znakiem minus.
- Mniej elektroujemnych elementów otrzymuje pozytywne stany utleniania, są one oznaczone znakiem plus.
- Tlen ogólnie wykazuje stan utlenienia -2.
- Dla wodoru, wartość charakterystyczna: +1, w wodorkach metali występuje: H - 1.
- Fluor jest najbardziej elektroujemny ze wszystkich pierwiastków, a jego stan utleniania wynosi zawsze -4.
- W przypadku większości metali liczby utleniające i wartościowości są takie same.
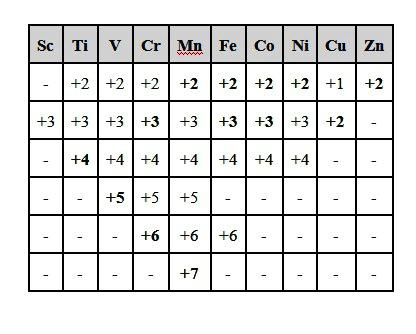
Stan utleniania i wartościowości
Większość związków powstaje w wyniku procesów redoks. Przejście lub przesunięcie elektronów z jednego elementu do drugiego prowadzi do zmiany ich stanu utlenienia i wartościowości. Często te wartości są takie same. Jako synonim terminu "stopień utlenienia" można użyć zwrotu "wartość elektrochemiczna". Są jednak wyjątki, na przykład w jonie amonowym azot jest czterowartościowy. W tym samym czasie atom tego pierwiastka znajduje się w stanie utlenienia -3. W materia organiczna węgiel jest zawsze czterowartościowy, ale stany utleniania atomu C w metanie CH 4 , alkoholu mrówkowym CH3OH i kwasie HCOOH mają różne wartości: -4, -2 i +2.
Ad
Reakcje redoks

Redox obejmuje wiele najważniejszych procesów w przemyśle, technologii, faunie i florze oraz nieożywionej przyrodzie: spalanie, korozję, fermentację, oddychanie wewnątrzkomórkowe, fotosyntezę i inne zjawiska.
Przy opracowywaniu równań OVR wybierają współczynniki za pomocą metody bilansu elektronicznego, które działają w następujących kategoriach:
- stany utleniania;
- środek redukujący przekazuje elektrony i jest utleniany;
- utleniacz przyjmuje elektrony i jest zredukowany;
- liczba emitowanych elektronów musi być równa liczbie dołączonych.
Pozyskiwanie elektronów przez atom prowadzi do zmniejszenia jego stopnia utlenienia (redukcji). Utracie jednego lub więcej elektronów przez atom towarzyszy wzrost liczby utleniania pierwiastka w wyniku reakcji. W przypadku OVR przepływający pomiędzy jonami silnych elektrolitów w roztworach wodnych, a nie w równowadze elektronowej, częściej stosuje się metodę połowicznego przereagowania.