Dwutlenek siarki - właściwości fizyczne, przygotowanie i zastosowanie
Dwutlenek siarki ma strukturę molekularną podobną do ozonu. Atom siarki znajdujący się w centrum cząsteczki wiąże się z dwoma atomami tlenu. Ten gazowy produkt utleniania siarki nie ma barwy, wytwarza silny zapach, a gdy zmieniają się warunki łatwo ulega kondensacji w klarowny płyn. Substancja dobrze rozpuszcza się w wodzie, ma właściwości antyseptyczne. SO 2 produkowany jest w dużych ilościach w przemyśle chemicznym, a mianowicie w cyklu produkcji kwasu siarkowego. Gaz jest szeroko stosowany do przetwarzania produktów rolnych i spożywczych, tkanin wybielających w przemyśle włókienniczym.
Systematyczne i banalne nazwy substancji
Konieczne jest zrozumienie różnorodności terminów związanych z tym samym związkiem. Oficjalna nazwa związku, którego skład chemiczny odzwierciedla wzór SO 2 , to dwutlenek siarki. IUPAC zaleca stosowanie tego terminu i jego odpowiednika w języku angielskim - dwutlenek siarki. Podręczniki dla szkół i uniwersytetów częściej wymieniają taką nazwę - tlenek siarki (IV). Cyfra rzymska w nawiasach wskazuje wartościowość atomu S. Tlen w tym tlenku jest dwuwartościowy, a liczba utleniająca siarki wynosi +4. Literatura techniczna używa takich nieaktualnych pojęć, jak dwutlenek siarki, bezwodnik kwasu siarkowego (produkt jego odwodnienia).
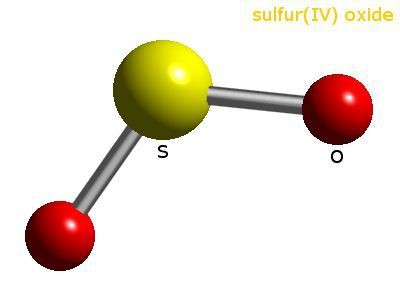
Skład i struktura cząsteczkowa SO 2
Cząsteczka SO2 jest utworzona przez jeden atom siarki i dwa atomy tlenu. Pomiędzy wiązaniami kowalencyjnymi występuje kąt 120 °. Hybrydyzacja sp2 występuje w atomie siarki - są one ułożone w formę i energię chmury jednego s oraz dwóch p-elektronów. Angażują się w edukację. wiązanie kowalencyjne między siarką i tlenem. W parze O-S odległość między atomami wynosi 0,143 nm. Tlen jest bardziej elektroujemnym elementem niż siarka, co oznacza, że pary wiążące elektronów są przesuwane ze środka na zewnętrzne naroża. Cała cząsteczka jest również spolaryzowana, biegun ujemny to atom O, dodatni to atom S.
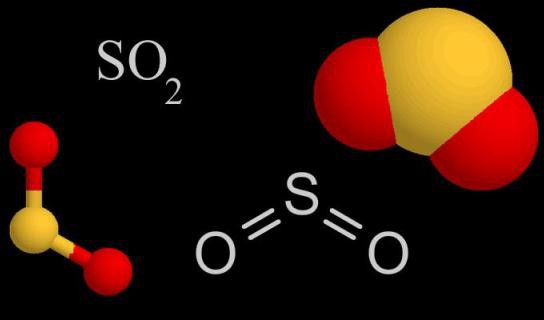
Niektóre parametry fizyczne dwutlenku siarki
Tlenek czterowartościowej siarki w normalnych warunkach środowiskowych zachowuje gazowy stan agregacji. Wzór dwutlenku siarki pozwala na określenie jego względnej masy cząsteczkowej i molowej: Mr (SO 2 ) = 64,066, M = 64,066 g / mol (można zaokrąglić do 64 g / mol). Gaz ten jest prawie 2,3 razy cięższy od powietrza (M (powietrze) = 29 g / mol). Dwutlenek ma ostry, specyficzny zapach płonącej siarki, który trudno jest pomylić z każdym innym. Jest nieprzyjemny, podrażnia błony śluzowe oczu, powoduje kaszel. Ale tlenek siarki (IV) nie jest tak toksyczny jak siarkowodór.
Pod ciśnieniem w temperaturze pokojowej gazowy dwutlenek siarki upłynnia się. W niskich temperaturach substancja jest w stanie stałym, topi się w temperaturze -72 ... -75,5 ° C Wraz z dalszym wzrostem temperatury pojawia się ciecz, aw temperaturze -10,1 ° C następuje ponowne przekształcenie gazu. Cząsteczki SO 2 są stabilne termicznie, rozkład na atomową siarkę i tlen cząsteczkowy występuje w bardzo wysokich temperaturach (około 2800 ºС).

Rozpuszczalność i interakcja z wodą
Dwutlenek siarki po rozpuszczeniu w wodzie częściowo reaguje z nim tworząc bardzo słaby kwas siarkowy. W momencie jego otrzymania natychmiast ulega rozkładowi do bezwodnika i wody: SO2 + H2O ↔ H2SO4. W rzeczywistości rozwiązanie nie jest obecne kwas siarkowy i uwodnione cząsteczki SO2. Dwutlenek lotny lepiej oddziałuje z zimną wodą, a jego rozpuszczalność zmniejsza się wraz ze wzrostem temperatury. W normalnych warunkach może rozpuścić się w 1 objętości wody do 40 objętości gazu.
Dwutlenek siarki w przyrodzie
Znaczne ilości dwutlenku siarki uwalniają się wraz z gazami wulkanicznymi i lawą podczas erupcji. Wiele rodzajów działań antropogenicznych prowadzi również do wzrostu stężenia SO 2 w atmosferze.

Bezwodnik kwasu siarkowego jest dostarczany do powietrza przez zakłady metalurgiczne, w których spaliny nie są uwięzione podczas spalania rudy. Wiele rodzajów paliw kopalnych zawiera siarkę, w wyniku czego znaczne ilości ditlenku siarki są uwalniane do powietrza atmosferycznego, gdy spalany jest węgiel, ropa naftowa i gaz pochodzący z nich. Dwutlenek siarki staje się toksyczny dla ludzi przy stężeniach w powietrzu przekraczających 0,03%. U osoby początkowo występuje duszność, mogą wystąpić objawy, takie jak zapalenie oskrzeli i zapalenie płuc. Bardzo wysokie stężenia dwutlenku siarki w atmosferze mogą prowadzić do poważnych zatruć lub śmierci.
Dwutlenek siarki - produkcja w laboratorium i przemyśle
Metody laboratoryjne:
- Gdy siarkę spala się w kolbie tlenem lub powietrzem, ditlenek otrzymuje się według wzoru: S + O2 = SO2.
- Możliwe jest działanie na sole kwasu siarkowego z mocniejszymi kwasami nieorganicznymi, lepiej jest brać kwas solny, ale możliwe jest rozcieńczenie siarki:
- Na 2SO 3 + 2HCI = 2NaCl + H2SO4;
- Na 2 SO 3 + H 2 SO 4 (d). = Na 2 SO 4 + H 2SO 3 ;
- H 2 SO 3 = H 2 O + SO 2 .
3 Kiedy miedź oddziałuje ze stężonym kwasem siarkowym, to nie uwalnia się wodoru, ale dwutlenek siarki:
2H 2SO 4 (stęż.) + Cu = CuSO 4 + 2H 2O + SO 2 .
Nowoczesne metody przemysłowej produkcji dwutlenku siarki:
- Utlenianie naturalnej siarki, gdy jest spalana w specjalnych piecach: S + O 2 = SO 2 .
- Wypalanie pirytu żelaznego (pirytu).
Podstawowe właściwości chemiczne ditlenku siarki
Dwutlenek siarki jest chemicznie aktywnym związkiem. W procesach redoks substancja ta często działa jako środek redukujący. Na przykład, w oddziaływaniu bromu cząsteczkowego z dwutlenkiem siarki, produkty reakcji są kwas siarkowy i bromowodór. Utleniające właściwości SO 2 pojawiają się, gdy gaz ten przepuszczany jest przez wodę siarkowodoru. W rezultacie następuje uwolnienie siarki, następuje samo-utlenienie-samodestrukcja: SO 2 + 2H 2 S = 3S + 2H 2 O.
Dwutlenek siarki wykazuje właściwości kwasowe. Odpowiada jednemu z najsłabszych i najbardziej niestabilnych kwasów - siarkowym. Ten związek nie istnieje w czystej postaci, możliwe jest wykrycie kwaśnych właściwości roztworu ditlenku siarki za pomocą wskaźników (lakmus jest różowawieniem). Kwas siarkowy daje średnie sole - siarczyny i kwaśne - wodorosiarczyny. Wśród nich są związki stabilne.
Proces utleniania siarki w ditlenku do stanu sześciowartościowego w bezwodniku kwasu siarkowego jest katalityczny. Otrzymana substancja energicznie rozpuszcza się w wodzie, reaguje z cząsteczkami H 2 O. Reakcja jest egzotermiczna, powstaje kwas siarkowy, a raczej jego uwodniona postać.
Praktyczne zastosowanie dwutlenku siarki
Główna metoda produkcji przemysłowej kwasu siarkowego, która wymaga dwutlenku pierwiastka, ma cztery etapy:
- Pozyskiwanie dwutlenku siarki poprzez spalanie siarki w specjalnych piecach.
- Oczyszczanie powstałego dwutlenku siarki ze wszystkich rodzajów zanieczyszczeń.
- Dalsze utlenianie do sześciowartościowej siarki w obecności katalizatora.
- Wchłanianie trójtlenku siarki przez wodę.
Wcześniej prawie cały dwutlenek siarki wymagany do produkcji kwasu siarkowego na skalę przemysłową uzyskiwano przez prażenie pirytu jako produktu ubocznego produkcji stali. Nowe rodzaje przetwarzania surowców metalurgicznych zużywają mniej spalania rudy. Dlatego w ostatnich latach naturalna siarka stała się głównym źródłem materiału do produkcji kwasu siarkowego. Znaczące globalne rezerwy tego surowca, jego dostępność pozwala nam organizować przetwarzanie na dużą skalę.

Dwutlenek siarki jest szeroko stosowany nie tylko w przemyśle chemicznym, ale także w innych przemysł. Młyny tekstylne wykorzystują tę substancję i produkty jej chemicznej interakcji do wybielania jedwabiu i tkaniny wełniane. Jest to jeden z rodzajów bielenia bezchlorowego, w którym włókna nie są niszczone.
Dwutlenek siarki ma doskonałe właściwości dezynfekujące, które stosuje się w walce z grzybami i bakteriami. Bezwodnik siarkowy jest poddawany fumigacji przy przechowywaniu produktów rolnych, beczek z winem i piwnic. Używano SO 2 w przemyśle spożywczym jako środek konserwujący i przeciwbakteryjny. Dodaj do syropów, zanurz w nim świeże owoce. Sulfitization
sok z buraków cukrowych odbarwia i dezynfekuje surowce. Puszki i soki roślinne zawierają również dwutlenek siarki jako przeciwutleniacz i środek konserwujący.
