Ogólny wzór amin. Właściwości i struktura amin
Zasady organiczne - ta nazwa jest często używana w chemii dla związków pochodzących z amoniaku. Atomy wodoru w jego cząsteczce są zastąpione przez rodniki węglowodorowe. Mówimy o aminach - związkach, które powtarzają chemiczne właściwości amoniaku. W naszym artykule zapoznamy się z ogólną formułą amin i ich właściwości.
Struktura molekularna
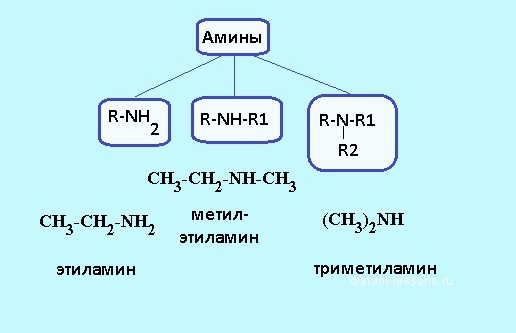
W zależności od tego, ile atomów wodoru zastąpiono rodnikami węglowodorowymi, rozróżnia się pierwszorzędowe, drugorzędowe i trzeciorzędowe aminy. Na przykład, metyloamina jest pierwszorzędową aminą, w której cząstkę wodoru zastąpiono grupą -CH3. Wzór strukturalny amin to R-NH 2 , można go użyć do określenia składu materii organicznej. Przykładem drugorzędowej aminy może być dimetyloamina, która ma następującą postać: NH2-NH-NH2. W cząsteczkach związków trzeciorzędowych wszystkie trzy atomy wodoru amoniaku są zastąpione przez rodniki węglowodorowe, na przykład trimetyloamina ma wzór (NH2) 3 N. Struktura amin wpływa na ich właściwości fizyczne i chemiczne.
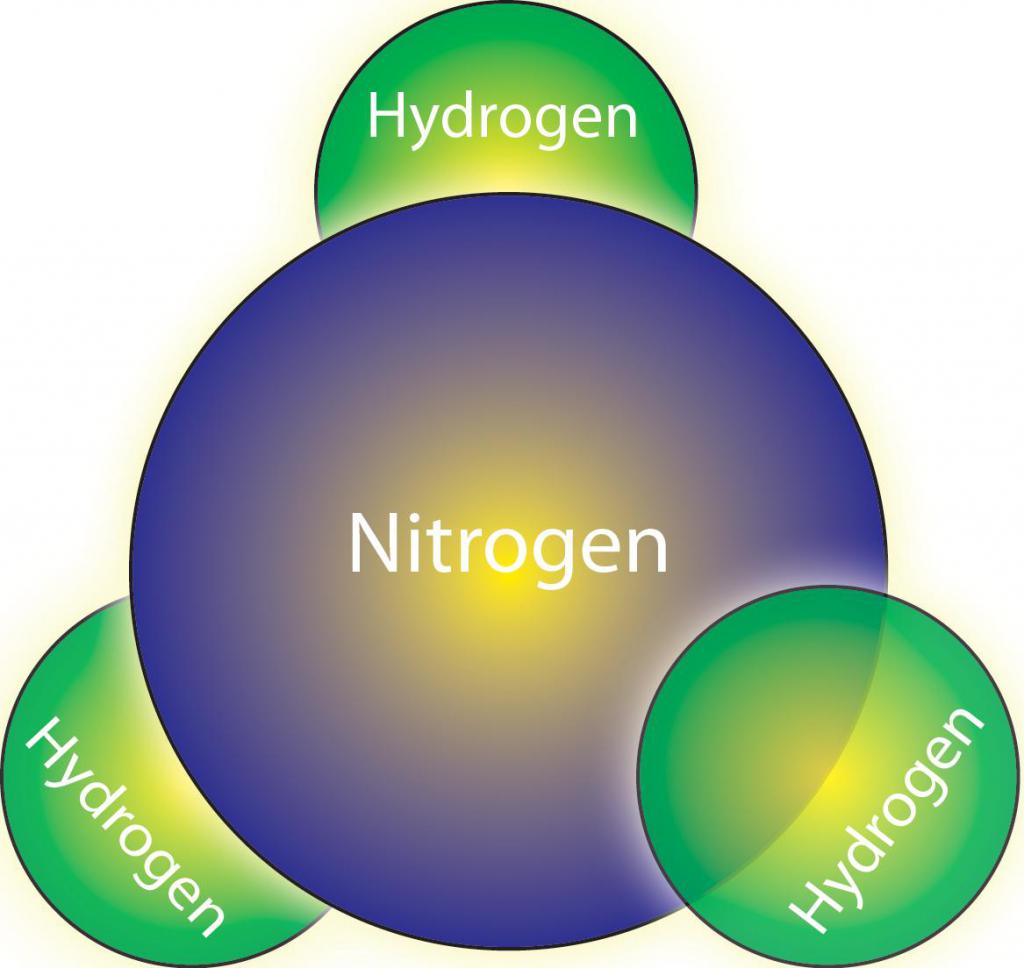
Charakterystyka fizyczna
Stan skupienia amin zależy od tego, co masa molowa radykałów. Im jest on mniejszy, tym niższa jest ciężar właściwy substancji. Aminy niższej klasy są reprezentowane przez gazy (na przykład metyloamina). Mają wyraźny zapach amoniaku. Średnie aminy to łagodnie pachnące ciecze, a związki o dużej masie rodników węglowodorowych są bezwonnymi ciałami stałymi. Rozpuszczalność amin zależy również od masy rodnika: im jest on większy, tym gorsza substancja rozpuszcza się w wodzie. Tak więc struktura amin determinuje ich stan fizyczny i właściwości.
Właściwości chemiczne
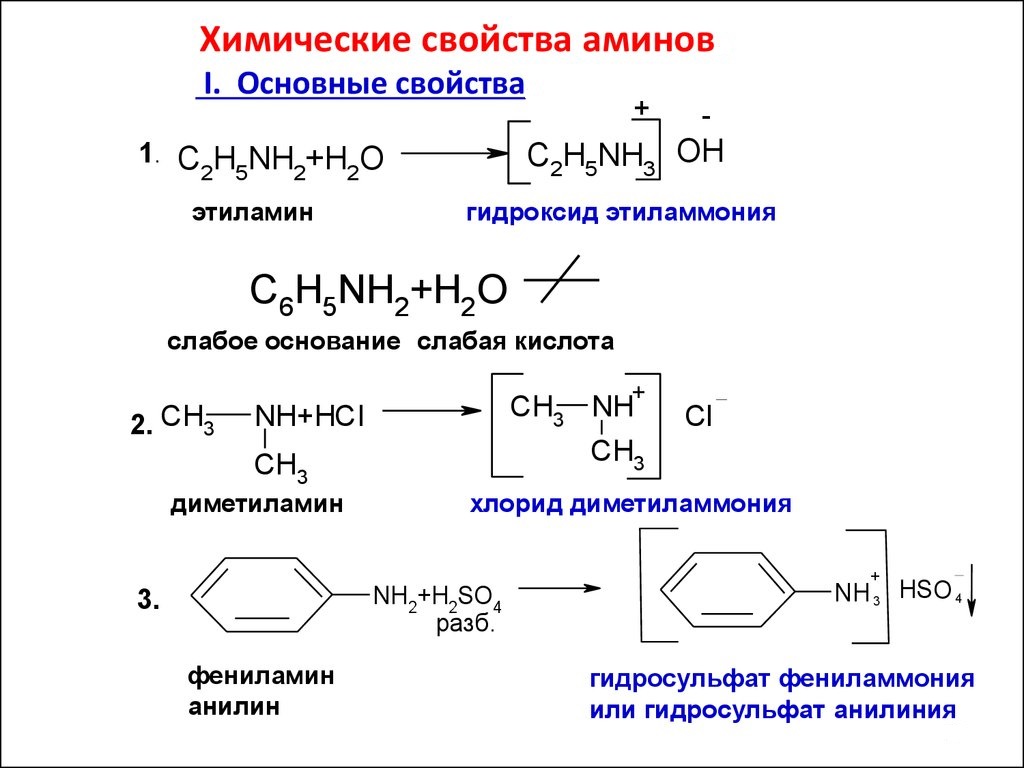
Charakterystyka substancji zależy głównie od transformacji grupy aminowej, w której wiodącą rolę przypisuje się jej samotnej parze elektronów. Więc jak materia organiczna Aminy klasyczne są pochodnymi amoniaku, są zdolne do reakcji charakterystycznych dla NH3. Na przykład związki rozpuszczają się w wodzie. Produktami tej reakcji będą substancje wykazujące właściwości wodorotlenków. Na przykład, metyloamina, której skład atomowy jest zgodny z ogólnym wzorem nasyconych amin R - NH 2 , z wodą tworzy związek, wodorotlenek metyloamoniowy:
CH3 - NH2 + H20 = [CH3-NH3] OH
Zasady organiczne wchodzą w interakcję z kwasami nieorganicznymi, aw produktach wykrywa się sól. Tak więc, metyloamina z kwasem chlorowodorowym daje chlorek metyloamoniowy:
CH 3- NH 2 HCl -> [CH 3 NH 3 ] Cl
Reakcje amin, których ogólny wzór to R-NH2, z kwasy organiczne zastępowane są przez zastąpienie atomu wodoru grupy aminowej kompleksem anionowym reszt kwasowych. Nazywa się je reakcjami alkilowania. Podobnie jak w reakcji z kwasem azotynowym, pochodne acylowe mogą tworzyć tylko pierwszorzędowe i drugorzędowe aminy. Trimetyloamina i inne trzeciorzędowe aminy nie są zdolne do takich interakcji. Dodajemy również, że alkilowanie w chemii analitycznej służy do oddzielania mieszanin amin, służy również odpowiedź jakościowa na pierwszorzędowych i drugorzędowych aminach. Wśród amin cyklicznych istotna jest anilina. Jest ekstrahowany z nitrobenzenu przez redukcję tego ostatniego wodorem w obecności katalizatora. Anilina jest surowcem do produkcji tworzyw sztucznych, barwników, materiałów wybuchowych i leków.

Trzeciorzędowe właściwości amin
Trzeciorzędowe pochodne amoniaku różnią się właściwościami chemicznymi od jedno- lub dwupodstawionych związków. Na przykład mogą wchodzić w interakcje z pochodnymi halogenowymi nasyconych węglowodorów. W wyniku tego powstają sole tetraalkiloamoniowe. Tlenek srebra reaguje z trzeciorzędowymi aminami, a aminy są przekształcane w wodorotlenki tetraalkiloamoniowe, które są mocnymi zasadami. Mogą tworzyć się kwasy aprotonowe, takie jak trifluorek boru, z trimetyloaminą związki złożone.
Test jakościowy dla amin pierwszorzędowych
Kwas azotowy może służyć jako odczynnik do wykrywania jedno- lub dwupodstawionych amin. Ponieważ nie istnieje w stanie wolnym, aby otrzymać go w roztworze, najpierw przeprowadzić reakcję między rozcieńczonym kwasem chlorkowym i azotynem sodu. Następnie dodaj rozpuszczoną pierwszorzędową aminę. Skład jego cząsteczek można wyrazić za pomocą ogólnego wzoru amin: R-NH 2. Procesowi temu towarzyszy pojawianie się cząsteczek nienasyconych węglowodorów, które można oznaczyć w reakcji z wodą bromową lub roztworem nadmanganianu potasu. Reakcję izonitrylu można uznać za jakościową. W nim pierwszorzędowe aminy oddziałują z chloroformem w środowisku z nadmiernym stężeniem anionów hydroksylowych. Rezultatem jest powstawanie izonitrilu o nieprzyjemnym specyficznym zapachu.

Cechy reakcji amin drugorzędowych z kwasem azotynowym
Technologia wytwarzania odczynnika HNO 2 jest opisana przez nas powyżej. Następnie do roztworu zawierającego odczynnik dodaje się organiczną pochodną amoniaku zawierającą dwie grupy węglowodorowe, na przykład dietyloaminę, której cząsteczka odpowiada ogólnemu wzorowi amin drugorzędowych NH2-R-NH2. W produktach reakcji znajduje się związek nitrowy: N-nitrozodietyloamina. Jeśli działa na kwas chlorowy, związek rozkłada się na sól chlorkową wyjściowej aminy i chlorek nitrozylu. Dodajemy również, że trzeciorzędowe aminy nie są zdolne do reakcji z kwasem azotawym. Wyjaśnia to następujący fakt: kwas azotowy należy do słabych kwasów, a jego sole, w interakcji z aminami zawierającymi trzy rodniki węglowodorowe, są całkowicie hydrolizowane w roztworach wodnych.
Sposoby na zdobycie
Aminy, których ogólny wzór stanowi R-NH2, można otrzymać przez redukcję związków zawierających azot. Na przykład może to być redukcja nitroalkanów w obecności katalizatora - metalicznego niklu - po podgrzaniu do +50 ° C i przy ciśnieniu do 100 atm. Nitroetan, nitropropan lub nitrometan są przekształcane w aminy w wyniku tego procesu. Substancje tej klasy można również otrzymać przez redukcję wodoru związków grup nitrylowych. Ta reakcja zachodzi w rozpuszczalnikach organicznych, z obecnością katalizatora niklowego. Jeśli jako środek redukujący stosuje się metaliczny sód, w tym przypadku proces przeprowadza się w roztworze alkoholowym. Przytoczmy przykłady dwóch innych metod: aminowania halogenoalkanów i alkoholi.
W pierwszym przypadku powstaje mieszanina amin. Aminowanie alkoholi przeprowadza się w następujący sposób: mieszaninę oparów metanolu lub etanolu z amoniakiem przepuszcza się przez tlenek wapnia, który działa jak katalizator. Otrzymane pierwszorzędowe, drugorzędowe i trzeciorzędowe aminy można zazwyczaj oddzielić przez destylację.
W naszym artykule badaliśmy strukturę i właściwości azotowych związków organicznych - amin.