Rodzaje reakcji chemicznych. Klasyfikacja chemiczna
Pojęcie, jakie rodzaje reakcji chemicznych są, jest nierozerwalnie związane z podstawową wiedzą na temat, który koniecznie jest nauczany w szkole. W przeciwieństwie do fizycznej metamorfozy, w chemii następuje przemiana substancji z jednej lub kilku w inną lub kilku innych. Na tym opierają się prawie wszystkie rodzaje reakcji chemicznych.
Czynniki reakcji chemicznych
Do chwili obecnej zidentyfikowano wystarczająco dużą liczbę reakcji, które w taki czy inny sposób należą do dziedziny chemii i fizyki. Jednak klasyfikacja reakcji chemicznych jest taka, że można je ocenić za pomocą pewnych podstawowych cech. Najczęściej są to oznaki o charakterze wizualnym.

Na przykład najłatwiejszym sposobem określenia, czy miała miejsce reakcja chemiczna, jest zmiana koloru substancji lub roztworu, wydzielanie się, wydzielanie gazu itp. Wszystko to nie jest trudne do zauważenia, jak mówią, nawet na oko. W niektórych przypadkach ta metoda nie działa. W szczególności dotyczy to odczynników ciekłych, takich jak kwasy i zasady, po rozpuszczeniu w wodzie. Chociaż proces ten jest ściśle związany z procesami fizycznymi, to jednak hydratację lub hydrolizę uważa się właśnie z punktu widzenia nauki, takiej jak chemia. Reakcje chemiczne określane za pomocą dodatkowych środków. Na przykład, jeśli zdecydujesz się na pH roztworu, tutaj nic nie zobaczysz wizualnie. Rozwiązania są używane do wskazania papierek lakmusowy który jest malowany w określonym kolorze w zależności od kwasowości medium.

Jednak definicja nie ogranicza się tylko do efektów wizualnych. Może to być potwierdzone przez inne nie mniej zauważalne czynniki, które pojawiają się w trakcie lub na końcu procesu. A jest ich całkiem sporo.
Równie interesującą cechą jest wzrost temperatury lub pożar stawu. Wystarczy przypomnieć szkolne doświadczenia, gdy kawałek potasu wrzuca się do wody, po czym uwalniany jest wodór. Jeśli weźmiesz wystarczająco duży kawałek tego metalu i odpowiednią ilość wody, możesz nawet osiągnąć fakt, że eksplozja niesamowitej siły właśnie się wydarzy. Pamiętaj, że takie przypadki w historii niestety nie są unikalne.

Główne rodzaje reakcji chemicznych
Jeśli chodzi o to, jakie typy reakcji chemicznych można odróżnić na obecnym etapie rozwoju nauki chemii, tutaj można na wstępie wspomnieć, że procesy można początkowo i warunkowo podzielić na jednorodne i niejednorodne. Procesy jednorodne zachodzą w tej samej fazie (np. Ciecz), a reakcje heterogeniczne wykorzystują kilka stanów substancji (ciekły, stały, gazowy itd.) Jako główne reagenty.
Jednak taki podział na typy procesów chemicznych jest daleka od unikalności, ponieważ w tym przypadku konieczne jest dokładne uwzględnienie konwersji substancji biorących udział w reakcji między sobą.
Ci sami alchemicy próbowali kiedyś zdobyć złoto z ołowiu. W rzeczywistości proces ten można przypisać raczej chemii raczej pośrednio.

W rzeczywistości przekształcenie jednego elementu w drugi należy raczej do dziedziny fizyki jądrowej. Obecnie możliwe jest wytwarzanie takiego procesu, jednak uzyskane w ten sposób złoto staje się bardzo wysoko radioaktywne, niewiarygodnie drogie i po prostu nie nadaje się do użytku.
Jednak w podstawowej wiedzy na temat podziału na klasy reakcji chemicznych należy wyróżnić najbardziej powszechne typy. Podstawę przyjęto w czterech głównych klasach: reakcji związku, rozkładu, podstawienia i wymiany jonowej. Istnieje również piąty rodzaj, który w swej istocie nie pasuje do żadnej z wyżej wymienionych klas. Są to reakcje redoks, w których z reguły nadmanganian potasu (KMnO 4 ) działa jako główny odczynnik, który wraz z kwasami jest uważany za jeden z najsilniejszych środków utleniających znanych ludzkości.

Reakcje złożone
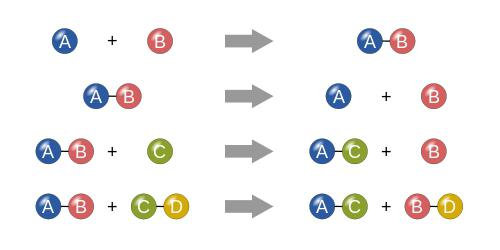
Jeśli mówimy o tym, jakie są warunki reakcji chemicznych tego typu, warunkowo sam proces można przedstawić jako rodzaj wyrażenia matematycznego. Załóżmy, że mamy dwie substancje. Konwencjonalnie oznaczamy je jako "A" i "B". W takim przypadku reakcja będzie miała następujący wzór:
A + B = AB
Jak już wiadomo, istnieje po prostu połączenie tych dwóch składników (czy są to substancje proste, czy złożone, które są związkami).
Najprostszym przykładem jest tworzenie tlenków. Na przykład:
S + O2 = SO2
Reakcje rozkładu
W rzeczywistości klasyfikacja reakcji chemicznych jest niemożliwa bez zrozumienia procesów rozkładu. Na podstawie powyższego przykładu sam proces może być przedstawiony jako formuła:
X = AB - A - B ,
gdzie AB jest substancją wyjściową, a A i B są składnikami, do których zostanie on rozłożony. Odpowiednio, X jest wynikiem, reprezentującym dwa składniki A i B, które pod koniec reakcji nie reagują ze sobą.
Reakcje substytucji
Warunki reakcji chemicznych z podstawieniem również mają swoje własne cechy. Opierając się na prostej matematyce, ten typ procesu można opisać za pomocą następującego przykładu:
Załóżmy, że mamy pewien związek w postaci dwóch składników "AB" i pewnej substancji "C". W tym widoku reakcja substytucji będzie następująca:
AB + C = AC + B lub AB + C = BC + A.
Innymi słowy, zwykle następuje zastąpienie jednego lub kilku składników innym.
Reakcje jonowymienne
Szybkość reakcji chemicznej najlepiej ilustruje przykład reakcji jonowymiennych, gdy reagenty są wymieniane na jony (naładowane cząstki). W tym przypadku może być maksymalna, ponieważ konwersja jednej substancji na drugą zachodzi na poziomie molekularnym. W wyrażeniu matematycznym wzór ten ma postać:
AB + CD = AD + CB (lub w innych odmianach).
W istocie reakcje wymiany jonowej są nieco podobne do reakcji podstawienia, chociaż należą do oddzielnej klasy.
Reakcje redoks
Jeśli chodzi o reakcje tego typu, są one wśród wszystkich znanych najbardziej złożonych (nie wspominając o reakcjach syntezy). Faktem jest, że nawet zwykłe równanie chemiczne z nadmanganianem potasu bez specjalnej wiedzy po prostu nie zadziała. W tym przypadku należy wziąć pod uwagę nie tylko wartościowość każdego początkowego składnika, ale także wartościowość, którą składniki nabywają po zakończeniu procesu. W większości przypadków wartościowość może się wahać w dość szerokich granicach, a wynikiem reakcji dwóch początkowych składników może być utworzenie trzech lub czterech związków.
Czynniki wpływające na szybkość reakcji chemicznych
Szybkość samej reakcji chemicznej zależy od zdolności reagentów do wejścia w proces, a także od pewnych dodatkowych warunków, takich jak temperatura. Najprostszym przykładem jest zastosowanie katalizatora - substancji zdolnej do przyspieszania reakcji chemicznej. Na przykład, aby zwolnić go w niektórych przypadkach, można użyć substancji takich jak inhibitory, adsorbenty, absorbenty itp. Każda taka substancja może mieć znaczący wpływ na cały proces chemiczny i szybkość jego przepływu.
Spośród substancji tego typu, zwykły człowiek zna węgiel aktywny, który jest w stanie wchłonąć kwasy lub zasady, w zależności od środowiska, w którym się znajduje.

Wniosek
Jak widać, rodzaje reakcji chemicznych, które zwykły człowiek może zrozumieć, są dość proste. Najważniejszą kwestią w tej kwestii jest wyraźne wyjaśnienie, czym jest proces. Zauważmy, że w tym przypadku rozważaliśmy procesy chemiczne oparte na prostej matematyce, bez wchodzenia w szczegóły chemii. Wydaje się, że takie podejście pomoże wyjaśnić istotę głównych procesów chemicznych, że tak powiem, "na palcach". Co więcej, z punktu widzenia matematyki każdy będzie w stanie zrozumieć, czym naprawdę jest dany proces.
W takim przypadku reakcje chemiczne i układy, w których więcej niż dwa reagenty wchodzą w interakcje, nie są uwzględniane. Aby je zrozumieć, musisz mieć pewną wiedzę. Tylko z nimi możliwe będzie dokonanie tego samego równania opisującego ten proces, nie wspominając o chemii organicznej, gdzie aby zrozumieć, czym jest substancja, trzeba nawet zastosować wzory strukturalne, powiedzmy, na podstawie pierścienia benzenowego lub przyłączonych rodników.
W takim przypadku musisz odejść od zwykłych podstaw chemia nieorganiczna który opisuje większość procesów najprościej i zwięźle. To prawda, ponieważ na początku rozwoju nauki o organicznej sobie, nikt nie miał pojęcia, jednak wyniki odkryć i wiele badań po prostu zadziwia.