Kwas octowy: wzór chemiczny, właściwości i zastosowanie
Kwas etanowy jest lepiej znany jako kwas octowy. Ona reprezentuje związek organiczny o wzorze CH3 COOH. Należy on do klasy kwasów karboksylowych, których cząsteczki zawierają funkcjonalne jednowartościowe grupy karboksylowe COOH (jedno lub kilka). O tym można zapewnić wiele informacji, ale teraz należy zwrócić uwagę tylko na najciekawsze fakty.
Formuła
Jak to wygląda, można zrozumieć na podstawie poniższego obrazu. Wzór chemiczny kwasu octowego jest nieskomplikowany. Wynika to z wielu: sam związek jest monozasadowy i należy do grupy karboksylowej, która charakteryzuje się łatwym rozkładem protonów (stabilna cząstka elementarna). Ten związek jest typowym przedstawicielem kwasów karboksylowych, ponieważ ma wszystkie ich właściwości.
Ad
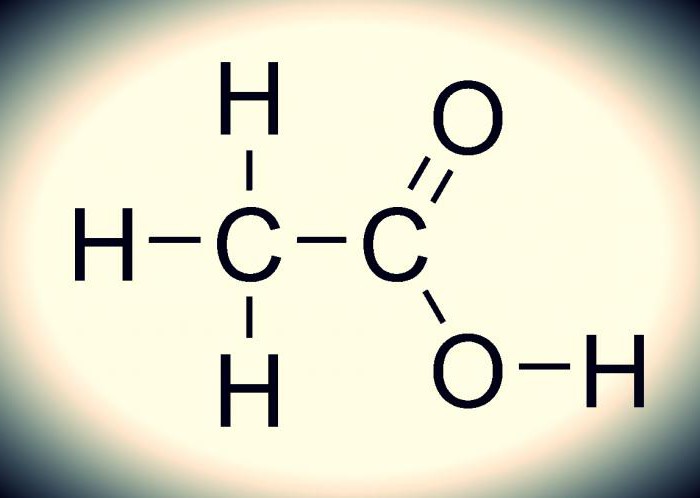
Wiązanie między tlenem i wodorem (-COOH) jest wysoce polarne. Powoduje to łatwy proces dysocjacji (rozpuszczania, rozkładu) tych związków i przejaw ich kwaśnych właściwości.
W wyniku tego powstaje proton H + i jon octanu CH3COO. Jakie są te substancje? Jon octanowy jest ligandem związanym z konkretnym akceptorem (obiektem, który otrzymuje coś od związku donorowego), tworząc stabilne kompleksy octanowe z kationami wielu metali. Proton jest, jak wspomniano powyżej, cząstką zdolną do wychwytywania elektronu z powłok elektronowych M-, K- lub L- atomu.
Analiza jakościowa
Opiera się dokładnie na dysocjacji kwasu octowego. Analiza jakościowa, zwana również reakcją, jest kombinacją metod fizycznych i chemicznych, które są wykorzystywane do wykrywania związków, rodników (niezależnych cząsteczek i atomów) i elementów (połączenie cząstek), które tworzą analit.
Ad
Za pomocą tej metody można wykryć sole kwasu octowego. Wszystko wygląda nie tak trudne, jak mogłoby się wydawać. Mocny jest dodawany do rozwiązania kwas. siarkowy, na przykład. A jeśli jest zapach kwasu octowego, to jego sól jest obecna w roztworze. Jak to działa? Pozostałości kwasu octowego, które powstają z soli, są związane w tym momencie z kationami wodoru z kwasu siarkowego. Jaki jest wynik? Pojawienie się większej liczby cząsteczek kwasu octowego. Dysocjacja się dzieje.
Reakcje
Należy zauważyć, że omawiany związek może oddziaływać z aktywnymi metalami. Należą do nich lit, sód, potas, rubid, francium, magnez, cez. Ten ostatni, nawiasem mówiąc, jest najbardziej aktywny. Co dzieje się w czasie takich reakcji? Wydzielił się wodór i powstaje octan osławiony. Oto wzór chemiczny kwasu octowego, który reaguje z magnezem: Mg + 2CH 3 COOH → (CH 3 COO) 2 Mg + H 2 ↑.

Istnieją sposoby uzyskiwania kwasów dichlorooctowego (CHCI2COOH) i trichlorooctowego (CCI3COOH). W nich atomy wodoru grupy metylowej są zastąpione przez chlor. Są tylko dwa sposoby, aby je zdobyć. Jedną z nich jest hydroliza trichloroetylenu. I to jest mniej powszechne niż inne, w oparciu o zdolność kwasu octowego do chlorowania w wyniku działania chloru gazowego. Ta metoda jest prostsza i bardziej wydajna.
Ad
Oto jak ten proces wygląda jak wzór chemiczny kwasu octowego wchodzącego w interakcje z chlorem: CH 3 COOH + Cl 2 → CH 2 CLCOOH + HCL. Tylko warto jedno wyjaśnić: jest to po prostu kwas chlorooctowy, dwa wyżej wymienione powstają przy udziale czerwonego fosforu w małych ilościach.
Inne transformacje
Warto zauważyć, że kwas octowy (CH3COOH) może wchodzić we wszystkie reakcje charakterystyczne dla notorycznej grupy karboksylowej. Można go przywrócić do etanolu, alkoholu jednowodorotlenowego. Aby to zrobić, konieczne jest działanie na nim wodorkiem litowo-glinowym, związkiem nieorganicznym, który jest silnym środkiem redukującym często stosowanym w syntezie organicznej. Jego formuła to Li (AlH 4 ).

Kwas octowy można również przekształcić w chlorek kwasowy, aktywny środek acylujący. Dzieje się to pod wpływem chlorku tionylu. Nawiasem mówiąc, jest to chlorek kwasu siarkowego. Jego formuła to H2S03. Warto również zauważyć, że sól sodowa dekarboksyluje kwas octowy po ogrzaniu alkaliami (z wyłączeniem cząsteczki dwutlenku węgla), w wyniku czego powstaje metan (CH₄). A on, jak wiadomo, jest najprostszym węglowodorem, który jest lżejszy od powietrza.
Krystalizacja
Lodowaty kwas octowy - często ten związek nazywany jest w ten sposób. Faktem jest, że gdy schładza się do zaledwie 15-16 ° C, przechodzi w stan krystaliczny, jakby zamarzł. Wizualnie jest to bardzo podobne do lodu. Jeśli istnieje kilka składników, można przeprowadzić eksperyment, którego wynikiem będzie przekształcenie kwasu octowego w lód. To proste. Z wody i lodu należy przygotować mieszaninę chłodzącą, a następnie opuścić wcześniej przygotowaną probówkę z kwasem octowym. Po kilku minutach krystalizuje. Oprócz związku wymaga zlewki, statywu, termometru i probówki.
Ad
Substancja szkodliwa
Kwas octowy, którego wzór chemiczny i właściwości zostały wymienione powyżej, jest niebezpieczny. Jej pary podrażniają błony śluzowe górnych dróg oddechowych. Próg odczuwania zapachu tego związku w powietrzu wynosi około 0,4 mg / l. Ale istnieje również pojęcie maksymalnego dopuszczalnego stężenia - normy sanitarnej i higienicznej, zatwierdzonej przez prawo. Według niego, w powietrzu może wynosić do 0,06 mg / m³ tej substancji. A jeśli chodzi o pomieszczenia robocze, limit wzrasta do 5 mg / m 3 .

Destrukcyjny wpływ kwasu na tkanki biologiczne zależy bezpośrednio od jego rozcieńczenia wodą. Najbardziej niebezpieczne rozwiązania z zawartością tej substancji ponad 30%. A jeśli dana osoba przypadkowo wejdzie w kontakt ze stężonym związkiem, nie będzie w stanie uniknąć poparzeń chemicznych. Tego kategorycznie nie można dopuścić, ponieważ po tej koagulacji zaczyna się rozwijać martwica - śmierć tkanek biologicznych. Dawka śmiertelna wynosi tylko 20 ml.
Ad
Konsekwencje
Logiczne jest, że im wyższe stężenie kwasu octowego, tym więcej szkód będzie mieć w przypadku kontaktu ze skórą lub do organizmu. Typowe objawy zatrucia obejmują:
- Kwasica Równowaga kwasowo-zasadowa jest przesunięta w kierunku zwiększenia kwasowości.
- Skrzepy krwi i jej krzepnięcie.
- Hemoliza erytrocytów, ich niszczenie.
- Uszkodzenie wątroby.
- Hemoglobinuria. W moczu pojawia się hemoglobina.
- Ostra niewydolność nerek.
- Toksyczny szok palący.
Stopnie nasilenia
Zwyczajowo wyróżnia się trzy:
- Łatwo Charakteryzuje się niewielkimi oparzeniami przełyku i jamy ustnej. Ale nie ma krzepnięcia krwi, a narządy wewnętrzne nadal działają normalnie.
- Średnia. Jest odurzenie, szok i pogrubienie krwi. Dotknięty jest żołądek.
- Ciężki Górne drogi oddechowe, ściany przewodu pokarmowego są poważnie uszkodzone i rozwija się niewydolność nerek. Maksymalny szok bólowy. Być może rozwój choroby oparzeń.

Możliwe jest również zatrucie parami octowymi. Towarzyszy mu silny katar, kaszel i łzawienie.
Pomoc
Jeśli dana osoba jest zatruta kwasem octowym, bardzo ważne jest, aby działać szybko, aby zminimalizować konsekwencje tego, co się wydarzyło. Zastanów się, co zrobić:
- Opłucz usta. Nie połykaj wody.
- Wykonaj płukanie żołądka z sondą. Zajmuje 8-10 litrów zimnej wody. Nawet domieszka krwi nie jest przeciwwskazaniem. Ponieważ w pierwszych godzinach zatruwania duże naczynia pozostają nienaruszone. Więc nie będzie niebezpiecznego krwawienia. Przed płukaniem środki przeciwbólowe powinny działać przeciwbólowo. Sonda jest smarowana olejem wazelinowym.
- Nie wywoływać wymiotów! Neutralizować substancję można spalić magnezji lub narkotyków "Almagel".
- Żadne z powyższych? Następnie ofiara otrzymuje lód i olej słonecznikowy - musisz wziąć kilka łyków.
- Pozwolono na użycie dotkniętej mieszanki mleka i jaj.
Ważne jest udzielenie pierwszej pomocy w ciągu dwóch godzin po incydencie. Po tym okresie błony śluzowe puchną i trudno będzie zmniejszyć ból człowieka. I tak, w żadnym wypadku nie można użyć sody. Połączenie kwasu i alkaliów wywoła reakcję, podczas której będzie się rozwijać dwutlenek węgla i woda. A taka formacja wewnątrz żołądka może być śmiertelna.
Aplikacja
Wodne roztwory kwasu etanowego są szeroko stosowane w przemyśle spożywczym. To są octy. Aby je uzyskać, kwas rozcieńcza się wodą, otrzymując 3-15% roztwór. Jako dodatek są oznaczone jako E260. Octy są częścią różnych sosów i są również wykorzystywane do produkcji konserw, marynowania mięsa i ryb. W życiu codziennym są one szeroko stosowane do usuwania kamienia, plam z ubrań i przyborów. Ocet jest doskonałym środkiem dezynfekcyjnym. Mogą poradzić sobie z każdą powierzchnią. Czasami dodaje się ją do prania w celu zmiękczenia ubrań.

Ocet można stosować również przy przygotowywaniu substancji zapachowych, leków, rozpuszczalników, np. Do produkcji acetonu i octanu celulozy. Tak, a kwas octowy jest bezpośrednio zaangażowany w barwienie i typografię.
Ponadto jest on stosowany jako medium reakcyjne do utleniania różnych substancji organicznych. Przykładem przemysłowym jest utlenianie para-ksylenu (aromatycznego węglowodoru) przez atmosferyczny tlen do tereftalowego kwasu aromatycznego. Nawiasem mówiąc, ponieważ opary tej substancji mają ostry, drażniący zapach, może być stosowany jako substytut amoniaku do usuwania osoby z omdlenia.
Syntetyczny kwas octowy
Jest to palny płyn, który należy do substancji trzeciej klasy niebezpieczeństwa. Jest stosowany w przemyśle. Podczas pracy z nim stosuje się osobiste wyposażenie ochronne. Przechowywać tę substancję w specjalnych warunkach i tylko w określonym pojemniku. Zazwyczaj jest to:
- czyste cysterny kolejowe;
- pojemniki;
- cysterny, beczki, zbiorniki ze stali nierdzewnej (pojemność do 275 dm 3 );
- szklane butelki;
- beczki z polietylenu o pojemności do 50 dm 3 ;
- szczelne zbiorniki ze stali nierdzewnej.

Jeśli ciecz jest przechowywana w pojemniku z polimerem, to wynosi najwyżej miesiąc. Ponadto kategorycznie zabronione jest przechowywanie tej substancji razem z takimi silnymi środkami utleniającymi, takimi jak nadmanganian potasu, siarka i kwas azotowy.
Skład octu
O nim też powinien powiedzieć kilka słów. Skład tradycyjnego, zwykłego octu obejmuje następujące kwasy:
- Apple Wzór: NOORSN₂CH (HE) COOH. Jest to powszechny dodatek do żywności (E296) pochodzenia naturalnego. Zawarte w niedojrzałych jabłek, malin, jarzębiny, berberysu i winogron. W tytoniu i tytoniu występuje w postaci soli nikotyny.
- Nabiał. Wzór: CH₃CH (OH) COOH. Powstały podczas rozkładu glukozy. Dodatek do żywności (E270), który otrzymuje się w drodze fermentacji mlekowej.
- Ascorbic Wzór: C = H203. Dodatek do żywności (E300), stosowany jako przeciwutleniacz, który zapobiega utlenianiu produktu.
I oczywiście związek etanu jest również zawarty w occie - to jest podstawa tego produktu.
Jak rozcieńczyć?
To jest często zadawane pytanie. Wszyscy widzieli sprzedaż kwasu octowego 70%. Jest kupowany w celu przygotowania mieszanek do popularnego zabiegu lub do zastosowania jako przyprawa, marynata, dodatek w sosie lub do roll-inu. Ale nie możesz użyć tak potężnego koncentratu. Dlatego powstaje pytanie, jak rozcieńczyć kwas octowy do octu. Najpierw musisz się zabezpieczyć - załóż rękawiczki. Następnie należy przygotować czystą wodę. Dla roztworów o różnych stężeniach potrzebna jest pewna ilość płynu. Który Spójrz na tabelę poniżej i rozcieńczyć kwas octowy w świetle danych.
Koncentracja octu | Początkowe stężenie octu 70% |
30 | 1: 1,5 (stosunek jest częścią octu do n-tej części wody) |
10 | 1: 6 |
9 | 1: 7 |
8 | 1: 8 |
7 | 1: 9 |
6 | 1:11 |
5 | 1:13 |
4 | 1:17 |
3 | 1:22 |
W zasadzie nic nie jest skomplikowane. Aby uzyskać 9% roztworu, musisz pobrać taką ilość wody w mililitrach za pomocą tej formuły: 100 gram octu pomnożone przez stawkę początkową (70%) i podzielone przez 9. Co się dzieje? Liczba ta wynosi 778. Od tej pory zabrano 100, ponieważ pierwotnie pobrano 100 gramów kwasu. Okazuje się, że 668 mililitrów wody. Ta ilość jest mieszana ze 100 g octu. Rezultatem jest cała butelka 9 procent roztworu.
Chociaż możesz działać jeszcze łatwiej. Wiele osób interesuje się wytwarzaniem octu z kwasu octowego. Łatwo! Najważniejsze jest, aby pamiętać, że dla jednej części 70% roztworu konieczne jest zabranie 7 części wody.