Sól bertoletowa: właściwości chemiczne, przygotowanie i zastosowanie
 Wprowadzenie
Wprowadzenie
Studiując tlen w chemii, dotarłeś do działu "Uzyskiwanie tlenu w laboratorium przez rozkład substancji nieorganicznych". "Dekompozycja wody, nadmanganianu potasu, nadtlenku wodoru, ciężkich tlenków i azotanów aktywnych metali ... wszystko wydaje się jasne: pobieranie tlenu z chlorku potasu Czy to jest bestia?!" - standardowy ciąg myśli każdego ucznia przeglądający ten akapit w podręczniku. Szkoła nie uczy soli Bertoletova, więc sam musisz o nią zapytać. Dzisiaj w tym artykule postaram się odpowiedzieć jak najwięcej na pytanie, czym jest sól bertoletowa.
Pochodzenie nazwy
Najpierw porozmawiajmy o jego nazwie. Sól jest odrębną klasą substancji nieorganicznych, w formule chemicznej, której następujący układ elementów to: Me-n to kwas kwasowy, gdzie Me to metal, kwas kwasowy to kwasowa pozostałość, n to liczba atomów (może nie być obecna, jeśli wartościowość metalu jest a kwasowa pozostałość jest taka sama). Kwasowe pozostałości są pobierane z dowolnego kwasu nieorganicznego. Wzór chemiczny tej soli to KClO 3 . Obecny w nim metal to potas, co oznacza, że jest to potas. Źródłem reszty ClO3 jest kwas chlorowodorowy HClO3. Całkowita sól bertoletowa jest solą potasową kwasu chlorowego. Nazywany jest również chloranem potasu, a przymiotnik "bertoletov" przypisuje się mu z powodu nazwy jego odkrywcy.
Historia odnajdywania
Po raz pierwszy uzyskał ją w 1786 r. Francuski chemik Claude Berthollet. Brakowało mu chloru przez gorący stężony roztwór wodorotlenku potasu (zdjęcie). 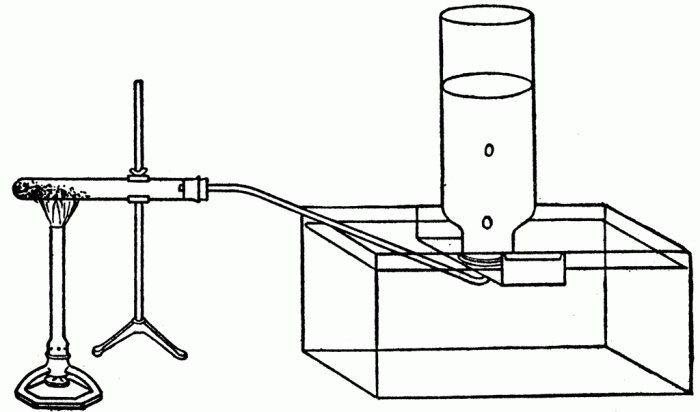
Sól Bertoletova: uzyskiwanie
Przemysłowa produkcja chloranów (w tym soli bertoletowej) opiera się na dysproporcjonowaniu podchlorynów, które uzyskuje się w wyniku oddziaływania chloru z roztworami alkalicznymi. Projekt procesu może być inny: ze względu na to, że najbardziej duży produkt - podchloryn wapnia, z którego wydziela się wybielacz, najczęstszym procesem jest realizacja reakcji wymiany między chloranem wapnia (jest otrzymywana przez ogrzewanie podchlorynu wapnia) i chlorku potasu (krystalizuje z ługu macierzystego). Kolejny chloran potasu można uzyskać dzięki zmodyfikowanemu metodzie Bertholleta przy użyciu elektrolizy membranowej chlorku potasu. Powstały chlor i wodorotlenek potasu oddziałują bezpośrednio. Produktem ich reakcji jest podchloryn potasu, który dodatkowo dysproporcjonuje do początkowego chlorek potasu i chloran potasu.
Właściwości chemiczne 
Jeżeli temperatura ogrzewania osiąga 400 ° C, następuje rozkład soli potasowej, w której uwalniany jest tlen i powstaje pośrednio nadchloran potasu. Z katalizatorami (tlenek manganu (4), tlenek żelaza (3), tlenek miedzi itp.) temperatura, w której odbywa się ten proces, staje się znacznie niższa. Sól bertoletowa i siarczan amonowy mogą reagować w roztworze woda-alkohol i tworzyć z chloranem amonu.
Aplikacja
Mieszaniny czynników redukujących (fosfor, siarka, związki organiczne) i chloran potasu są wybuchowe i wrażliwe na wstrząsy i tarcie (zdjęcie powyżej). Czułość jest zwiększona, jeśli obecne są bromiany i sole amonowe. Ze względu na wysoką czułość, kompozycje, w których występuje sól bertoletowa, prawie nigdy nie są wykorzystywane do produkcji wojskowych i przemysłowych materiałów wybuchowych. Czasami jest on używany w pirotechnice jako źródło chloru do preparatów z kolorowym płomieniem.  Jest również zawarty w główkach meczów i bardzo rzadko może być inicjującym materiałem wybuchowym (proszek chloranowy zdetonował przewód i był grubszą kompozycją granatów ręcznych Wehrmachtu). A w ZSRR chloran potasu jest częścią lontu koktajlu Mołotowa, przygotowanego według specjalnej receptury. Roztwory soli bertoletowej były niekiedy stosowane jako słaby antyseptyk, zewnętrzny lek do płukania gardła. Na początku XX w. Do produkcji tlenu w laboratorium użyto soli bertoletowowej. Jednak ze względu na wysokie ryzyko przestało obowiązywać. Ponadto, stosując go w warunkach laboratoryjnych, otrzymuje się dwutlenek chloru (prowadzi się reakcję redukcji chloranu szczawianu potasu i kwas siarkowy).
Jest również zawarty w główkach meczów i bardzo rzadko może być inicjującym materiałem wybuchowym (proszek chloranowy zdetonował przewód i był grubszą kompozycją granatów ręcznych Wehrmachtu). A w ZSRR chloran potasu jest częścią lontu koktajlu Mołotowa, przygotowanego według specjalnej receptury. Roztwory soli bertoletowej były niekiedy stosowane jako słaby antyseptyk, zewnętrzny lek do płukania gardła. Na początku XX w. Do produkcji tlenu w laboratorium użyto soli bertoletowowej. Jednak ze względu na wysokie ryzyko przestało obowiązywać. Ponadto, stosując go w warunkach laboratoryjnych, otrzymuje się dwutlenek chloru (prowadzi się reakcję redukcji chloranu szczawianu potasu i kwas siarkowy).
Wniosek
Teraz wiesz o soli bertoletowej wszystko. Może być zarówno korzystne, jak i niezwykle niebezpieczne dla ludzi. Jeśli masz mecze w domu, codziennie obserwujesz jedną z gałęzi stosowania soli bertoletowej w życiu codziennym.