Właściwości chemiczne i fizyczne aluminium. Właściwości fizyczne wodorotlenku glinu
Ten lekki metal o srebrno-białym odcieniu znajduje się niemal wszędzie we współczesnym życiu. Fizyczne i chemiczne właściwości aluminium sprawiają, że jest on szeroko stosowany w przemyśle. Najbardziej znane złoża znajdują się w Afryce, Ameryce Południowej i na Karaibach. W Rosji miejsca wydobycia boksytu znajdują się na Uralu. Światowymi liderami w produkcji aluminium są Chiny, Rosja, Kanada, USA. 
Wydobywanie węgla
W naturze ten metal srebra, ze względu na jego wysoką aktywność chemiczną, występuje tylko w postaci związków. Najbardziej znane skały geologiczne zawierające aluminium to boksyt, tlenek glinu, korund, skalenie. Boksyt i tlenek glinu mają znaczenie przemysłowe, a złoża tych rud umożliwiają wydobywanie aluminium w czystej postaci.
Ad
Właściwości
Fizyczne właściwości aluminium ułatwiają wciągnięcie sztabki tego metalu do drutu i przetoczenie go na cienkie arkusze. Metal ten nie jest trwały, aby zwiększyć ten wskaźnik podczas wytapiania, jest on stopowany różnymi dodatkami: miedzią, krzemem, magnezem, manganem, cynkiem. Dla celów przemysłowych ważne jest, aby inną fizyczną właściwością substancji aluminiowej była jej zdolność do szybkiego utleniania się w powietrzu. W warunkach naturalnych powierzchnia produktu aluminiowego jest zwykle pokryta cienką warstwą tlenku, która skutecznie chroni metal i zapobiega jego korozji. Kiedy ten film zostaje zniszczony, srebrzysty metal szybko się utlenia, a jego temperatura znacznie wzrasta.
Wewnętrzna struktura aluminium
Fizyczne i chemiczne właściwości aluminium są w dużej mierze zależne od jego wewnętrznej struktury. Kryształowa krata Ten element jest typem sześcianu skoncentrowanego na twarzy. 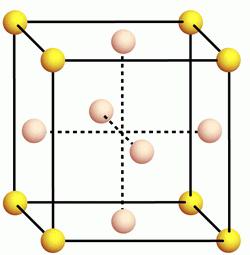 Ten rodzaj siatki jest nieodłączny dla wielu metali, takich jak miedź, brom, srebro, złoto, kobalt i inne. Wysoka przewodność cieplna i zdolność przewodzenia prądu sprawiły, że ten metal jest jednym z najbardziej poszukiwanych na świecie. Pozostałe właściwości fizyczne aluminium, którego tabela przedstawiona jest poniżej, w pełni ujawniają jego właściwości i pokazują zakres ich zastosowania.
Ten rodzaj siatki jest nieodłączny dla wielu metali, takich jak miedź, brom, srebro, złoto, kobalt i inne. Wysoka przewodność cieplna i zdolność przewodzenia prądu sprawiły, że ten metal jest jednym z najbardziej poszukiwanych na świecie. Pozostałe właściwości fizyczne aluminium, którego tabela przedstawiona jest poniżej, w pełni ujawniają jego właściwości i pokazują zakres ich zastosowania. 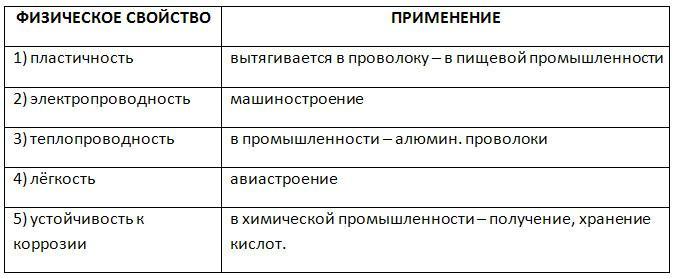
Stop aluminium
Fizyczne właściwości miedzi i aluminium są takie, że gdy pewna ilość miedzi jest dodawana do stopu aluminium, jej sieć krystaliczna jest zginana, a wytrzymałość samego stopu wzrasta. Al opiera się na tej właściwości stopowych stopów lekkich, aby zwiększyć ich wytrzymałość i odporność na agresywne środowiska.
Ad
Wyjaśnienie procesu hartowania polega na zachowaniu atomów miedzi w sieci krystalicznej aluminium. Cząsteczki miedzi mają tendencję do wypadania z sieci krystalicznej Al, są zgrupowane w jej specjalnych obszarach. 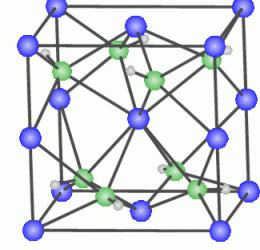 Gdzie atomy miedzi tworzą skupiska, powstaje mieszana sieć krystaliczna CuAl2, w której cząsteczki srebra tworzą jednocześnie część wspólnej sieci krystalicznej aluminium i mieszanej siatki typu CuAl 2. Siła połączeń wewnętrznych w zniekształconej sieci jest znacznie większa niż w zwykłym. Oznacza to, że wytrzymałość nowo powstałej substancji jest znacznie wyższa.
Gdzie atomy miedzi tworzą skupiska, powstaje mieszana sieć krystaliczna CuAl2, w której cząsteczki srebra tworzą jednocześnie część wspólnej sieci krystalicznej aluminium i mieszanej siatki typu CuAl 2. Siła połączeń wewnętrznych w zniekształconej sieci jest znacznie większa niż w zwykłym. Oznacza to, że wytrzymałość nowo powstałej substancji jest znacznie wyższa.
Właściwości chemiczne
Interakcja glinu z rozcieńczonym kwasem siarkowym i kwas chlorowodorowy. Po podgrzaniu metal łatwo się w nim rozpuszcza. Zimno jest stężone lub bardzo rozcieńczone kwas azotowy nie rozpuszcza tego elementu. Wodne roztwory alkaliów aktywnie wpływają na substancję, w trakcie reakcji tworzą się gliniany - sole zawierające jony glinu. Na przykład:
Ad
Al 2 O 3 + 3H 2O + 2NaOH = 2Na [Al (OH) 4 ]
Otrzymany związek nazywa się tetrahydroksaluminianem sodu.
Cienki film na powierzchni produktów aluminiowych chroni ten metal nie tylko przed powietrzem, ale także przed wodą. Jeśli ta cienka bariera zostanie usunięta, element będzie energicznie oddziaływać z wodą, uwalniając z niej wodór.
2AL + 6H20 = 2 AL (OH) 3 + 3H2
Utworzona substancja jest nazywana wodorotlenek glinu.
AL (OH) 3 reaguje z alkaliami, tworząc kryształy hydroksyaluminianu:
Al (OH) 2 + NaOH = 2Na [Al (OH) 4 ]
Jeśli to równanie chemiczne zostanie dodane do poprzedniego, otrzymamy wzór na rozpuszczenie pierwiastka w roztworze alkalicznym.
Al (OH) 3 + 2NaOH + 6H20 = 2Na [Al (OH) 4 ] + 3H2
Spalanie aluminium
Fizyczne właściwości aluminium pozwalają mu reagować z tlenem. Jeśli proszek tej metalowej lub aluminiowej folii zostanie podgrzany, zacznie błyskać i płonie białym, oślepiającym płomieniem. Pod koniec reakcji powstaje tlenek glinu Al 2 O 3.
Tlenek glinu
Powstały tlenek glinu ma nazwę geologiczną tlenek glinu. W warunkach naturalnych występuje w postaci korundu - stałych przezroczystych kryształów. Korund wyróżnia się wysoką twardością, jego wskaźnikiem w skali ciał stałych jest 9. Sam korund jest bezbarwny, ale różne zanieczyszczenia mogą go zabarwić na czerwono i niebiesko, dzięki czemu uzyskuje się klejnoty, które w biżuterii nazywane są rubinami i szafirami.
Ad
Fizyczne właściwości tlenku glinu umożliwiają hodowlę tych kamieni szlachetnych w sztucznych warunkach. Klejnoty techniczne są wykorzystywane nie tylko do produkcji biżuterii, ale również do precyzyjnego wytwarzania instrumentów, wykonywania zegarków i innych rzeczy. Sztuczne kryształy ruby są również szeroko stosowane w urządzeniach laserowych. 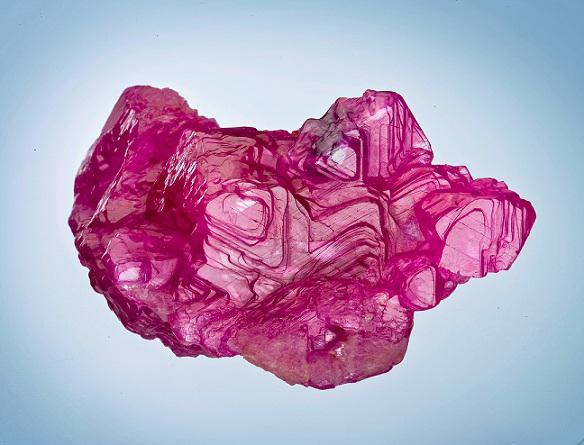
Drobnoziarniste odmiany korundu z dużą ilością zanieczyszczeń osadzonych na specjalnej powierzchni, znanej wszystkim jako szmergiel. Fizyczne właściwości tlenku glinu wyjaśniają wysokie właściwości ścierne korundu, a także jego twardość i odporność na tarcie.
Wodorotlenek glinu
Al 2 (OH) 3 to typowy wodorotlenek amfoteryczny. W połączeniu z kwasem substancja ta tworzy sól zawierającą dodatnio naładowane jony glinu, w alkaliach tworzy gliniany. Substancja amfoteryczna przejawia się w tym, że może zachowywać się zarówno jako kwas, jak i alkalia. Ten związek może istnieć w postaci galaretowatej lub stałej.  Praktycznie nierozpuszczalny w wodzie, ale reaguje z najbardziej aktywnymi kwasami i zasadami. Fizyczne właściwości wodorotlenku glinu są stosowane w medycynie, jest popularnym i bezpiecznym środkiem zmniejszania kwasowości w organizmie, jest stosowany w zapaleniu żołądka, dwunastnicy, wrzodach. W przemyśle Al 2 (OH) 3 jest stosowany jako adsorbent, doskonale oczyszcza wodę i wytrąca szkodliwe pierwiastki rozpuszczone w niej.
Praktycznie nierozpuszczalny w wodzie, ale reaguje z najbardziej aktywnymi kwasami i zasadami. Fizyczne właściwości wodorotlenku glinu są stosowane w medycynie, jest popularnym i bezpiecznym środkiem zmniejszania kwasowości w organizmie, jest stosowany w zapaleniu żołądka, dwunastnicy, wrzodach. W przemyśle Al 2 (OH) 3 jest stosowany jako adsorbent, doskonale oczyszcza wodę i wytrąca szkodliwe pierwiastki rozpuszczone w niej.
Zastosowanie przemysłowe
Aluminium odkryto w 1825 roku. Początkowo ten metal był ceniony ponad złoto i srebro. Było to spowodowane złożonością wydobycia z rudy. Fizyczne właściwości aluminium i jego zdolność do szybkiego tworzenia filmu ochronnego na jego powierzchni sprawiły, że badanie tego elementu było trudne. Dopiero pod koniec XIX wieku powstała wygodna metoda topienia czystego elementu nadającego się do zastosowania na skalę przemysłową. 
Lekkość i odporność na korozję to wyjątkowe właściwości fizyczne aluminium. Stopy tego srebrnego metalu są wykorzystywane w technologii rakietowej, w produkcji samochodów, statków, samolotów i przyrządów, w produkcji sztućców i naczyń.
Ad
Jako czysty metal Al jest wykorzystywany do produkcji części do sprzętu chemicznego, przewodów elektrycznych i kondensatorów. Fizyczne właściwości aluminium są takie, że jego przewodność elektryczna nie jest tak wysoka, jak miedzi, ale ta wada jest kompensowana łatwością metalu, co umożliwia wytwarzanie drutów z aluminium grubszego. Tak więc, przy tej samej przewodności elektrycznej, drut aluminiowy waży dwa razy mniej niż miedź.
Równie ważne jest zastosowanie Al w procesie aluminizacji. Jest to tak zwana reakcja nasycania powierzchni żeliwa lub produktu stalowego z aluminium w celu ochrony metalu podstawowego przed korozją podczas ogrzewania.
Obecnie sprawdzone rezerwy rud aluminium są dość porównywalne do potrzeb ludzi w tym srebrnym metalu. Fizyczne właściwości aluminium mogą stanowić dla naukowców znacznie więcej niespodzianek, a zakres zastosowania tego metalu jest znacznie szerszy, niż można sobie wyobrazić.