Właściwości chemiczne metali ziem alkalicznych. Lista metali ziem alkalicznych
Druga grupa układu okresowego DI Mendelejewa zawiera grupę elementów, które są bardzo podobne w swoich właściwościach metale alkaliczne są one jednak gorsze w działaniu. Zawiera beryl i magnez, a także wapń, stront, bar i rad. Są one znane pod ogólną nazwą - pierwiastki ziem alkalicznych. W naszym artykule zapoznamy się z ich rozmieszczeniem w naturze i zastosowaniach w przemyśle, a także będziemy badać główne właściwości chemiczne metali ziem alkalicznych.

Ogólna charakterystyka
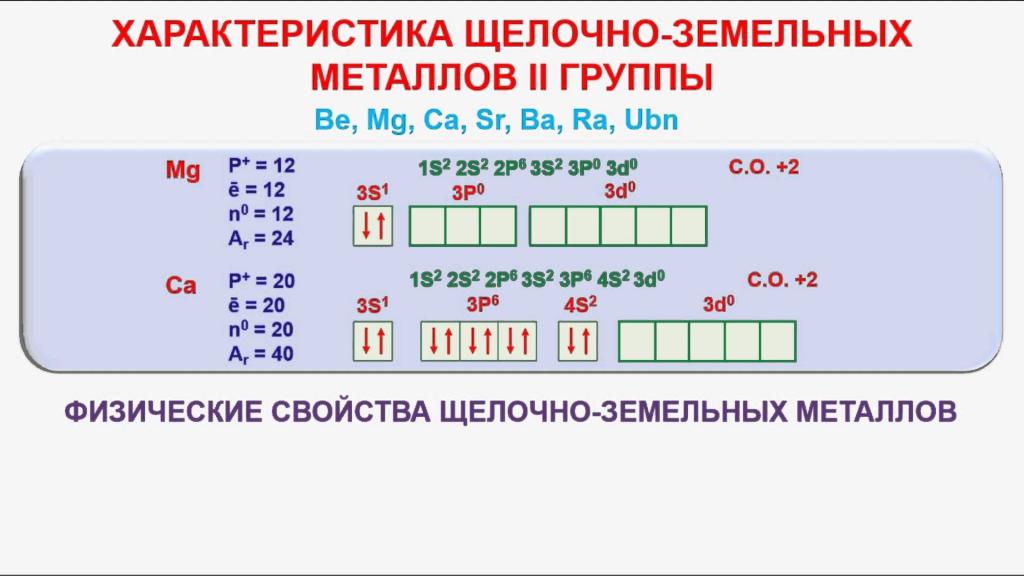
Wszystkie atomy powyżej wymienionych elementów zawierają dwa elektrony w zewnętrznej warstwie energetycznej. Oddziaływając z innymi substancjami, zawsze oddają swoje ujemne cząstki, przechodząc w stan kationów o ładunku 2+. W reakcjach redoks pierwiastki zachowują się jak silne środki redukujące. Wraz ze wzrostem ładunku jądrowego wzrastają właściwości chemiczne metali ziem alkalicznych i ich aktywność. Szybko utleniają się w powietrzu, tworząc na ich powierzchni warstwę tlenkową. Ogólna formuła dla wszystkich tlenków to RO. Odpowiadają wodorotlenkom o wzorze R (OH) 2 . Ich podstawowe właściwości i rozpuszczalność w wodzie zwiększają się wraz ze wzrostem numeru seryjnego elementu.
Szczególne właściwości berylu i magnezu
W niektórych swoich właściwościach pierwsi dwaj przedstawiciele głównej podgrupy drugiej grupy różnią się nieco od innych pierwiastków ziem alkalicznych. Przejawia się to w szczególności podczas ich interakcji z wodą. Na przykład chemiczne właściwości berylu są takie, że nie reagują w ogóle z H 2 O. Magnez oddziałuje z wodą tylko po ogrzaniu. Ale wszystkie pierwiastki ziem alkalicznych z łatwością reagują z nią w zwykłej temperaturze. Jakie substancje powstają w tym samym czasie?

Podstawy metali ziem alkalicznych
Wapń, bar i inni członkowie grupy szybko zastępują wodór z wody, tworząc wodorotlenki. Interakcja metali ziem alkalicznych z wodą przepływa szybko, wraz z wydzielaniem ciepła. Roztwory baz wapnia, baru, strontu, kojące w dotyku, gdy wejdą w kontakt ze skórą i błoną śluzową oczu, powodują poważne oparzenia. Pierwszą pomocą w takich przypadkach będzie obróbka powierzchni rany słabym roztworem kwasu octowego. Neutralizuje alkalia i zmniejsza ryzyko martwicy uszkodzonych tkanek.
Właściwości chemiczne metali ziem alkalicznych
Interakcja z tlenem, wodą i niemetalami jest główną listą właściwości metali zawartych w drugiej grupie okresowego układu pierwiastków chemicznych. Na przykład wapń nawet w normalnych warunkach reaguje z halogenami: fluorem, chlorem, bromem i jodem. Po podgrzaniu łączy się z siarką, węglem i azotem. Twarde utlenianie - spalanie, kończy się formacją tlenek wapnia: 2Ca + O2 = 2 CaO. Interakcja metali z wodorem prowadzi do pojawienia się wodorków. Są to białe substancje ogniotrwałe z jonowymi sieciami krystalicznymi. Ważne właściwości chemiczne metali ziem alkalicznych obejmują ich oddziaływanie z wodą. Jak wspomniano wcześniej, produktem tej reakcji podstawienia jest wodorotlenek metalu. Należy również zauważyć, że w głównej podgrupie drugiej grupy wapń zajmuje najważniejsze miejsce. Dlatego bardziej szczegółowo analizujemy jego cechy.
Wapń i jego związki
Zawartość pierwiastka w skorupie wynosi do 3,5%, co wskazuje na jego szeroki rozkład w składzie takich minerałów jak wapień, kreda, marmur i kalcyt. Skład naturalnego wapnia obejmuje sześć rodzajów izotopów. Występuje również w naturalnych źródłach wody. Związki metali alkalicznych są szczegółowo badane w trakcie chemii nieorganicznej. Na przykład w klasie 9 uczniowie dowiedzą się, że wapń jest lekkim, ale mocnym srebrno-białym metalem. Jego temperatura topnienia i wrzenia są wyższe niż w przypadku pierwiastków alkalicznych. Podstawowa metoda otrzymywania - elektroliza mieszaniny stopionych soli chlorku i fluorku wapnia. Główne właściwości chemiczne to reakcje z tlenem, wodą i niemetalami. Spośród związków metali alkalicznych tlenek i wapń są najważniejsze dla przemysłu. Pierwszy związek otrzymuje się z kredy lub wapienia poprzez ich spalanie.

Ponadto wodorotlenek wapnia powstaje z tlenku wapnia i wody. Jego mieszanka z piaskiem i wodą nazywa się zaprawą budowlaną. W dalszym ciągu jest stosowany jako tynk i do łączenia cegieł podczas układania ścian. Roztwór wodorotlenku wapnia, nazywany wodą wapniową, stosuje się jako odczynnik do wykrywania dwutlenku węgla. Podczas przepuszczania dwutlenku węgla przez klarowny wodny roztwór Ca (OH) 2 , jego zmętnienie obserwuje się z powodu powstawania nierozpuszczalnego osadu. węglan wapnia.
Magnez i jego charakterystyka
Chemia metali ziem alkalicznych bada właściwości magnezu, koncentrując się na niektórych jego cechach. Jest to bardzo lekki, srebrzystobiały metal. Magnez stopiony w atmosferze o wysokiej wilgotności aktywnie pochłania cząsteczki wodoru z pary wodnej. Chłodzenie powoduje, że metal niemal całkowicie uwalnia je z powrotem w powietrze. Reaguje bardzo wolno z wodą z powodu tworzenia słabo rozpuszczalnego związku, wodorotlenku magnezu. Alkalis w ogóle nie działa na magnez. Metal nie reaguje z niektórymi kwasami: stężonym siarczanem i fluorowodorkiem, ze względu na pasywację i tworzenie warstwy ochronnej na powierzchni. Większość kwasów mineralnych rozpuszcza metal, czemu towarzyszy szybkie uwalnianie wodoru. Magnez jest silnym czynnikiem redukującym, zastępuje wiele metali z ich tlenków lub soli:
BeO + Mg = MgO + Be.
Metal wraz z berylem, manganem, aluminium jest stosowany jako środek stopowy do stali. Szczególnie cenne właściwości to stopy zawierające magnez - elektrony. Są wykorzystywane w produkcji samolotów i samochodów, a także w szczegółach technologii optycznej.
Rola elementów w życiowej aktywności organizmów
Podajmy przykłady metali ziem alkalicznych, których związki są powszechne w dzikiej przyrodzie. Magnez jest centralnym atomem w cząsteczkach chlorofilu w roślinach. Bierze udział w procesie fotosyntezy i jest częścią aktywnych centrów zielonego pigmentu. Atomy magnezu wiążą energię świetlną, przekształcając ją w energię wiązań chemicznych związków organicznych: glukozy, aminokwasów, gliceryny i kwasów tłuszczowych. Ważną rolę odgrywa element jako niezbędny składnik enzymów regulujących metabolizm w ludzkim ciele. Wapń jest makroelementem, który zapewnia efektywne przejście impulsów elektrycznych przez tkankę nerwową. Obecność soli fosforanowych w składzie kości i szkliwie zębów nadaje im twardość i wytrzymałość.
Beryl i jego właściwości
Metale ziem alkalicznych obejmują także beryl, bar i stront. Rozważ beryl. Pierwiastek ten nie jest szeroko rozpowszechniony w naturze, głównie w składzie minerałów, na przykład, beryl. Jego odmiany zawierające wielobarwne zanieczyszczenia tworzą klejnoty: szmaragdy i akwamaryny. Cechą właściwości fizycznych jest kruchość i wysoka twardość. Charakterystyczną cechą atomu pierwiastka jest obecność na drugim zewnętrznym poziomie energii nie osiem, jak we wszystkich innych metalach ziem alkalicznych, ale tylko dwa elektrony.

Dlatego promień atomu i jonu jest nieproporcjonalnie mały, energia jonizacji jest duża. Powoduje dużą wytrzymałość. sieć krystaliczna metal. Właściwości chemiczne berylu odróżniają go także od innych elementów z drugiej grupy. Reaguje nie tylko z kwasami, ale także z roztworami alkalicznymi, wypierając wodór i tworząc hydroksyleryniany:
Be + 2NaOH + 2H20 = Na2 [Be (OH) 4 ] + H2.
Metal ma wiele unikalnych cech. Ze względu na możliwość pomijania promieni X, służy on do produkcji lamp rentgenowskich. W przemyśle jądrowym pierwiastek uważany jest za najlepszego moderatora i reflektor neutronów. W hutnictwie stosowany jest jako cenny dodatek stopowy, który zwiększa właściwości antykorozyjne stopów.
Stront i bar
Elementy są dość powszechne w naturze i podobnie jak magnez ziem alkalicznych stanowią część minerałów. Nazwijmy je: jest to baryt, celestyna, stront. Bar ma wygląd metalu z tworzywa sztucznego w srebrno-białym kolorze. Podobnie jak wapń, jest reprezentowany przez kilka izotopów. W powietrzu aktywnie współdziała z jego składnikami - tlenem i azotem - tworząc tlenek baru i azotek. Z tego powodu metal jest przechowywany pod warstwą parafiny lub oleju mineralnego, unikając kontaktu z powietrzem. Oba metale tworzą nadtlenki po podgrzaniu do 500 ° C.

Spośród nich nadtlenek baru, stosowany jako wybielacz do tkanek, ma praktyczne zastosowanie. Właściwości chemiczne metali ziem alkalicznych, baru i strontu są podobne do właściwości wapnia. Ich oddziaływanie z wodą jest jednak znacznie bardziej aktywne, a powstałe zasady są silniejsze niż wodorotlenek wapnia. Bar jest stosowany jako dodatek do ciekłych chłodziw metalowych, zmniejszając korozję, w optyce, w produkcji próżniowych urządzeń elektronicznych. Stront jest poszukiwany w produkcji ogniw fotowoltaicznych i luminoforów.
Jakościowe reakcje z użyciem jonów metali ziem alkalicznych
Związki baru i strontu są przykładami metali ziem alkalicznych szeroko stosowanych w pirotechnice ze względu na ich jasny kolor płomienia z jonami. Tak więc, siarczan lub węglan strontu daje czerwoną karminową poświatę płomienia, a odpowiednie związki baru dają żółtozielone. W celu wykrycia jonów wapnia w laboratorium, kilka peletek chlorku wapnia wlewa się na płomień palnika, płomień jest malowany w kolorze ceglastoczerwonym.

Roztwór chlorku baru stosuje się w chemii analitycznej do wykrywania kwaśnej pozostałości kwasu siarczanowego w roztworze. Jeśli powstaje biały osad siarczanu baru po odlaniu roztworów, oznacza to, że znajdują się w nim cząstki SO4 2- .
W naszym artykule zbadaliśmy właściwości metali ziem alkalicznych i podaliśmy przykłady ich zastosowania w różnych gałęziach przemysłu.