Wiązanie jonowe. Metoda formowania i właściwości
W reakcje chemiczne elektrony z jednego atomu mogą przejść całkowicie do innego. Taka redystrybucja ładunków prowadzi do tworzenia dodatnio i ujemnie naładowanych jonów (kationów i anionów). Powstaje między nimi szczególny rodzaj interakcji - wiązanie jonowe. Rozważmy bardziej szczegółowo metodę jej powstawania, strukturę i właściwości substancji.
Elektroujemność
Atomy różnią się elektroujemnością (EO) - zdolnością do przyciągania elektronów ze skorup walencyjnych innych cząstek. Do określenia ilościowego zastosowano skalę względnej elektroujemności zaproponowaną przez L. Polling (wielkość bezwymiarowa). Silniejszy niż inne pierwiastki, zdolność do przyciągania elektronów z atomów fluoru jest wyrażona, jego EO wynosi 4. W skali odpytywania tlen, azot i chlor natychmiast podążają za fluorem. Wartości EO wodoru i innych typowych niemetali są równe lub zbliżone do 2. Większość metali ma elektroujemność od 0,7 (Fr) do 1,7. Istnieje zależność jonowości wiązania od różnicy między TE pierwiastków chemicznych. Im większe, tym większe prawdopodobieństwo powstania wiązania jonowego. Ten rodzaj interakcji jest bardziej powszechny, gdy różnica EO wynosi 1,7 i więcej. Jeśli wartość jest mniejsza, związki są kowalencyjne.
Ad
Energia jonizacji
Aby odłączyć zewnętrzne elektrony słabo związane z jądrem, niezbędna jest energia jonizacji (EI). Jednostką zmiany tej wielkości fizycznej jest 1 wolt elektronowy. Istnieją regularności w zmianie EI w rzędach i kolumnach układu okresowego, w zależności od wzrostu ładunku jądrowego. W okresach od lewej do prawej energia jonizacji rośnie i osiąga najwyższe wartości dla niemetali. W grupach zmniejsza się z góry na dół. Głównym powodem jest wzrost promienia atomu i odległość od jądra do zewnętrznych elektronów, które łatwo się odrywają. Powstaje dodatnio naładowana cząstka - odpowiedni kation. Wielkość EI można ocenić na podstawie tego, czy występuje wiązanie jonowe. Właściwości zależą również od energii jonizacji. Na przykład metale alkaliczne a metale ziem alkalicznych mają małe wartości EI. Mają wyraźne właściwości odbudowujące (metal). Gazy obojętne są chemicznie nieaktywne ze względu na wysoką energię jonizacji.
Ad
Powinowactwo elektronowe
W interakcjach chemicznych atomy mogą łączyć się z elektronami tworząc ujemną cząsteczkę, anion, procesowi towarzyszy uwalnianie energii. Odpowiednia wielkość fizyczna to powinowactwo do elektronu. Jednostka miary jest taka sama jak energia jonizacji (1 elektronowolt). Ale jego dokładne wartości nie są znane dla wszystkich elementów. Halogeny mają najwyższe powinowactwo elektronowe. Na zewnętrznym poziomie atomów pierwiastków - 7 elektronów, bez jednego tylko do oktetu. Powinowactwo elektronowe do halogenów jest wysokie, mają silne właściwości utleniające (niemetaliczne).
Interakcja atomów w tworzeniu wiązań jonowych
Atomy z niepełnym poziomem zewnętrznym znajdują się w niestabilnym stanie energii. Chęć uzyskania stabilnej konfiguracji elektronicznej jest główną przyczyną, która prowadzi do powstawania związków chemicznych. Procesowi zwykle towarzyszy wydzielanie energii i może prowadzić do cząsteczek i kryształów, które różnią się strukturą i właściwościami. Silne metale i niemetale różnią się znacznie między sobą pod względem wielu wskaźników (EO, EI i powinowactwa elektronów). Dla nich bardziej odpowiedni jest rodzaj interakcji, taki jak jonowe wiązanie chemiczne, w którym porusza się jednoczący orbitalny molekularny (wspólna para elektronów). Uważa się, że gdy tworzą się jony, metale całkowicie przenoszą elektrony do niemetali. Siła powstałego wiązania zależy od pracy wymaganej do zniszczenia cząsteczek tworzących 1 mol badanej substancji. Ta fizyczna ilość znana jest jako energia wiążąca. W przypadku związków jonowych jego wartości wahają się od kilkudziesięciu do setek kJ / mol.
Ad
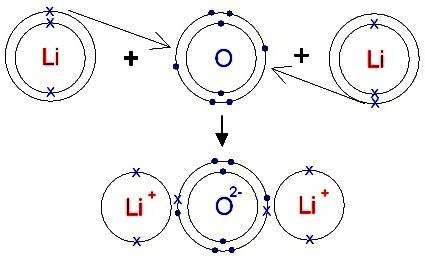
Tworzenie jonów
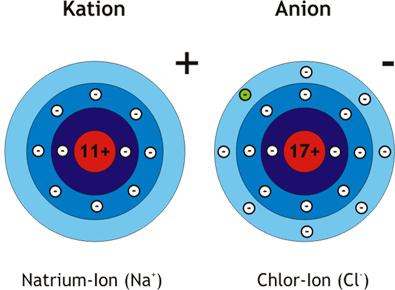
Atom, który przekazuje swoje elektrony podczas interakcji chemicznych, przekształca się w kation (+). Cząstką macierzystą jest anion (-). Aby dowiedzieć się, jak zachowują się atomy, czy pojawią się jony, należy ustalić różnicę między ich TE. Najprostszym sposobem przeprowadzenia takich obliczeń jest dla związku dwóch pierwiastków, na przykład chlorek sodu.
- EO (Cl) = 3,16;
- EO (Na) = 0,99;
- 3,16 - 0,99 = 2,17.
- 2,17 więcej niż 1,7, występuje wiązanie jonowe.
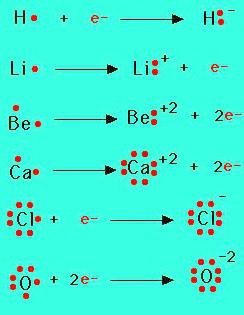
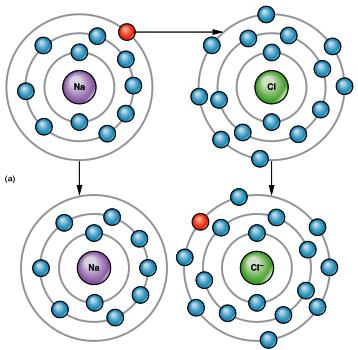
Sód ma w sumie 11 elektronów, konfiguracja warstwy zewnętrznej to 3s 1 . Aby go dokończyć, atom łatwiej jest oddać 1 elektron niż przyczepić 7. Struktura warstwy walencyjnej chloru jest opisana wzorem 3s 2 3p 5 . Atom ma łącznie 17 elektronów, 7 - zewnętrznych. Nie wystarczy, aby osiągnąć oktet i stabilną strukturę. Właściwości chemiczne potwierdzają założenie, że atom sodu daje, a chlor akceptuje elektrony. Są jony: dodatnie (kation sodu) i ujemne (anion chloru).
Wiązanie jonowe
Po utracie elektronu, sód otrzymuje ładunek dodatni i stabilną powłokę z neonu w gazie obojętnym (1s 2 2s 2 2p 6 ). Chlor w wyniku oddziaływania z sodą otrzymuje dodatkowy ładunek ujemny, a jon powtarza strukturę powłoki atomowej gazu szlachetnego argonu (1s 2 2s 2 2p 6 3s 2 3p 6 ). Nabyte ładunki elektryczne nazywane są ładunkiem jonów. Na przykład Na + , Ca 2+ , Cl - , F - . Jony mogą zawierać atomy kilku pierwiastków: NH 4 + , SO 4 2- . Wewnątrz takich złożonych jonów cząstki są wiązane przez donor - akceptor lub mechanizm kowalencyjny. Elektrostatyczne przyciąganie występuje pomiędzy przeciwnie naładowanymi cząstkami. Jego wartość w przypadku wiązania jonowego jest proporcjonalna do ładunków, a wraz ze wzrostem odległości między atomami słabnie. Charakterystyczne cechy wiązania jonowego:
Ad
- silne metale reagują z aktywnymi pierwiastkami niemetalicznymi;
- elektrony przenoszą się z jednego atomu do drugiego;
- Powstałe jony mają stabilną konfigurację zewnętrznych powłok;
- przyciąganie elektrostatyczne występuje między przeciwnie naładowanymi cząstkami.
Kraty kryształowe związki jonowe
W reakcjach chemicznych metale z 1., 2. i 3. grupy układu okresowego zwykle tracą elektrony. Tworzenie jedno-, dwu- i potrójnych dodatnich jonów. Niemetale z 6 i 7 grupy zwykle przyczepiają elektrony (z wyjątkiem reakcji z fluorem). Pojawiają się pojedyncze i podwójnie naładowane jony ujemne. Koszty energii dla tych procesów są z reguły rekompensowane, gdy tworzy się kryształ. Związki jonowe są zwykle w stanie stałym, tworzą struktury składające się z przeciwnie naładowanych kationów i anionów. Cząstki te przyciągają i tworzą gigantyczne sieci krystaliczne, w których jony dodatnie są otoczone przez cząstki ujemne (i vice versa). Całkowity ładunek materii wynosi zero, ponieważ całkowita liczba protonów jest zrównoważona przez liczbę elektronów wszystkich atomów.
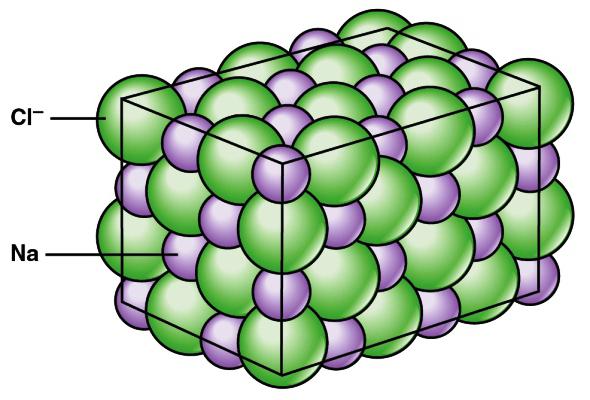
Właściwości substancji z wiązaniem jonowym
Jonowe substancje krystaliczne charakteryzują się wysoką temperaturą wrzenia i temperaturami topnienia. Zwykle związki te są odporne na ciepło. Następującą cechę można wykryć przez rozpuszczenie takich substancji w polarnym rozpuszczalniku (wodzie). Kryształy są łatwo niszczone, a jony przechodzą w roztwór o przewodności elektrycznej. Związki jonowe są również niszczone przez topienie. Pojawiają się swobodnie naładowane cząstki, a więc topi się prąd elektryczny. Substancje z wiązaniem jonowym to elektrolity - przewodniki drugiego rodzaju.
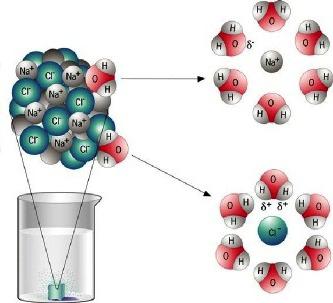
Tlenki i halogenki metali alkalicznych i metali ziem alkalicznych należą do grupy związków jonowych. Prawie wszystkie z nich są szeroko stosowane w nauce, technologii, produkcji chemicznej, metalurgii.