Izomeria: klasa klasyczna
Czym jest izomeria? Interklas, strukturalny, izomeria, pozycja grup funkcyjnych i izomeria wielu wiązań to wszystkie jego odmiany. Przeanalizujmy definicję tego terminu, biorąc pod uwagę konkretne przykłady jego tworzenia i przynależności do pewnych klas materia organiczna.
Definicja
Interferencyjna izomeria alkenów jest zjawiskiem, w którym mogą istnieć substancje o zupełnie różnych klasach substancji organicznych o tym samym składzie jakościowym i ilościowym.
Przedstawiciele seria homologiczna alkeny mają ogólny wzór postaci CnH2n. Wśród głównych parametrów wyróżniających tej klasy, zwracamy uwagę na obecność podwójnych wiązań w cząsteczkach. Ta sama formuła w chemii organicznej opisuje klasę cykloalkanów, które mają pojedyncze wiązania i strukturę cykliczną.
Ad
Przykłady izomerii węglowodorów
Na przykład izomeria klasyczna jest charakterystyczna dla wzoru cząsteczkowego C4H8, to znaczy, że istnieje kilka różnych węglowodorów jednocześnie. Wśród substancji cyklicznych zauważamy cyklobutan i metylocyklopropan.
Jeśli przeanalizuje się węglowodory o otwartej strukturze o ogólnym wzorze C4H8, można dokonać wzory strukturalne buten-1, buten-2 i metylopropen. Biorąc pod uwagę, że przedstawiciele cyklicznych i nienasyconych węglowodorów należą do różnych klas, obserwuje się izomerię międzyklasową.
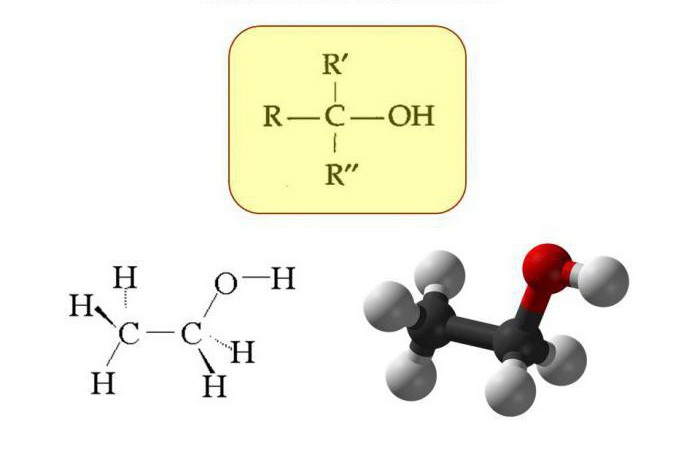
Związki zawierające tlen
Czy istnieje izomeria klasyczna? Aby znaleźć odpowiedź na to pytanie, rozważamy ich ogólną formułę. Limit jednowodorotlenowe alkohole są związkami o ogólnym wzorze CnH2n + 1OH, które zawierają grupę hydroksylową. Izomer międzyklasowy to etery. Skład jakościowy i ilościowy tych związków zawierających tlen są do siebie absolutnie podobne. W tym przypadku izomeria międzyklasowa wyjaśnia istnienie substancji o różnych właściwościach fizycznych i chemicznych. Na przykład dla składu C2H6O można sformułować wzór etanolu C2H5OH lub zapisać wzór eteru dimetylowego (CH3) 2-O.
Ad
W zależności od tego, ile atomów węgla znajduje się w głównym łańcuchu, liczba izomerów międzyklasowych będzie się znacznie różnić.
Zadania kompilacji formuł izomerycznych klasy klasowej są z powodzeniem rozwiązywane przez uczniów szkół średnich. Aby poradzić sobie z takimi problemami i określić liczbę izomerów, podajemy konkretny przykład.
Dla formuły kompozycji C5H10 można wykonać następujące warianty związków:
- penten-1;
- penten-2;
- 2 metylobuten-1;
- 2 metylo-buten-2;
- cyklopentan;
- metylocyklobutan.
Wartość izomerii
Estry monosacharydów i kwasu fosforowego mają ważne znaczenie biologiczne. Biorą czynny udział w biosyntezie cukrowych substancji i wysokowartościowego metabolizmu węglowodanów, który występuje w organizmie istot żywych. Aminokwasy są końcowymi produktami hydrolizy cząsteczek białka. Podczas tworzenia pojedynczych polimerów składających się z sekwencji aminokwasów ważna jest wyraźna powtarzalność struktury, ponieważ zależy od tego specyficzność uzyskanego polimeru biologicznego.
Charakterystyczny dla nich izomeria optyczna wyjaśnia wiele procesów zachodzących w świecie żywym. Na przykład, w zależności od tego, do której serii należą monosacharydy, charakteryzują się one różnymi funkcjami biologicznymi.
Zdolność do formułowania izomerów międzyklasowych jest uważana za jedną z ich głównych umiejętności, którą muszą opanować uczniowie szkoły średniej.