Reakcja Lebiediewa: formuła, mechanizm reakcji. Produkcja butadienu
Reakcja Siergieja Wasiljewicza Lebiediewa stała się punktem wyjścia do badań nad metodami wytwarzania nienasyconych węglowodorów dienowych, które są nadal dobrze wykorzystywane do wytwarzania kauczuków syntetycznych. Odkrycie to umożliwiło zastosowanie względnie taniej i opłacalnej metody syntezy sztucznej gumy do celów wojskowych i technicznych, która zapewniła uwalnianie wysokiej jakości i trwałej wymiany naturalnych gum w czasach sowieckich.

Zasada reakcji
Zgodnie z zasadą przepływu, syntezę tę przypisuje się pirolizie katalitycznej (rozkładowi termicznemu), która zachodzi w obecności katalizatorów tlenek glinowo-cynkowy w temperaturze około 450 ° C.
W chemii reakcja Lebiediewa jest niezwykła, ponieważ odbywa się w jednym etapie, ale jednocześnie pojawiają się w niej trzy zmiany:
- woda pęka;
- wodór się zrywa;
- łączenie zachodzi między resztami alkilowymi.
Syntezę wielokrotnie ulepszano, stosowano nowe katalizatory aluminiowe z dodatkiem soli manganu i innych metali, a warunki zmieniały się, co pozwoliło na zmniejszenie zużycia energii przy utrzymaniu temperatury (360-370 ° C) i zwiększenie stopnia konwersji alkoholu podczas reakcji (do 50%, wydajność butadien - 1,3 wynosi 42%).

Odczynniki i produkty
We wczesnych badaniach S. V. Lebiediew odwołał się do tworzenia butadienu z frakcji ropy naftowej. Jednak później zaczął otrzymywać ten dien z alkoholu etylowego uzyskanego przez fermentację ziemniaków. Aby uzyskać tylko jedną oponę samochodową, konieczne było przetworzenie do 500 kg ziemniaków, co oczywiście było nieopłacalne ekonomicznie.
Później, w latach 1926-928, S.V. Lebiediew wraz ze swoim zespołem studentów i wolnymi słuchaczami poprawił metodę otrzymywania butadienu z alkoholu etylowego. Wydajność dienu w momencie demonstracji wynosiła 22%. Dzięki staraniom naukowcy wygrali konkurs zorganizowany przez I.V. Stalin pośród krajów byłego Związku Radzieckiego, w sprawie propozycji metod produkcji kauczuków syntetycznych.
Ad
Tak więc, w ostatecznej wersji syntezy, w głównych produktach otrzymuje się butadien - 1,3 CH 2 = CH - CH = CH2, woda H 2 O i wolny wodór H2. Ponadto mogą powstawać pewne związki aromatyczne, etylen, propylen, butyleny, wyższe alkohole i aldehyd octowy, ale formuły tych substancji nie są określone w podstawowym równaniu reakcji Lebiediewa. Ponieważ ten dien jest substancją gazową, nierozpuszczalną w wodzie, jest oddzielany od wszystkich innych węglowodorów przez kondensację, adsorpcję przez alkohol, przemywanie H20 lub rektyfikację.
Mechanizm reakcji
W syntezie podczas rozszczepiania (rozkładu) 2 cząsteczek alkoholu etylowego, dzięki odwadniającym odwadniającym katalizatorom oddziela się 2 cząsteczki wody i 1 cząsteczkę wodoru wodorowego. Zgodnie z mechanizmem reakcji Lebiedieja, reszty alkilowe łączą się, tworząc dwa nienasycone skoniugowane wiązania podwójne w pozycjach 1,3 (przykład 1).
Ad
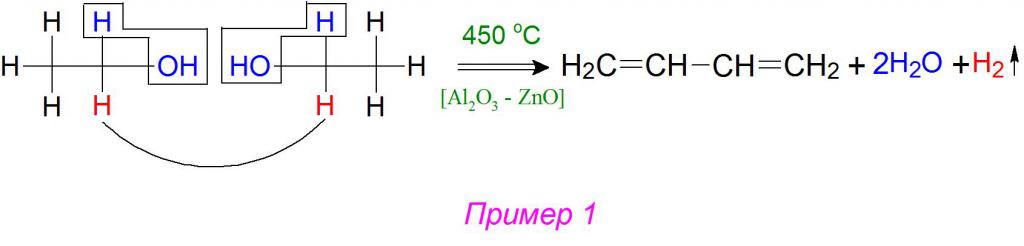
Użyj w przemyśle
Po triumfalnym zwycięstwie w międzynarodowym konkursie naukowiec otrzymał możliwość przeprowadzenia produkcji kauczuku syntetycznego na skalę przemysłową. Ponieważ odbiór butadienu w reakcji Lebiediewa uznano za bardzo cenny, został on sfinansowany, aw 1930 r. Zbudowano eksperymentalną fabrykę Litera B w Leningradzie, która do 1990 r. Zajmowała pierwsze miejsce na świecie w produkcji sztucznej gumy. Na bazie tego przedsiębiorstwa powstał później Ogólnounijny Instytut Badań nad Kauczukiem Syntetycznym, który kontynuuje badania związków polimerowych.

Dalsze badania
Odkrycia S. V. Lebiediewa były początkiem badań właściwości węglowodorów dienowych, dzięki czemu odkryto tak zwaną "syntezę dienową". Istnieją trzy wersje, w których badał reakcję dimeryzacji dienów w trakcie swojej pracy naukowej. Pierwszy zakłada, że w wyniku syntezy naukowiec uzyskał dimer cyklopentadienowy. Druga wersja mówi o dimeryzacji izoprenu, dając dipenten. Trzeci opisuje wytwarzanie winylo-cykloheksenu z dwóch cząsteczek butadienu - 1,3. W każdym razie synteza ta stanowiła podstawę do dalszych badań nad właściwościami skoniugowanych dienów, które zostały opracowane przez Otto Dielsa i Kurta Adlera, którzy zostali nagrodzeni Nagrodą Nobla w 1950 roku.
Synteza dienowa
Reakcja Dielsa-Adlera pozwoliła nam uzyskać związki cykliczne za pomocą dość prostych mechanizmów, bez uciekania się do złożonych reakcji wieloetapowych. Istotą reakcji jest oddziaływanie sprzężonego dienu i dienofilu, które mogą być reprezentowane przez alkeny i alkiny z podstawnikami elektroakceptorowymi, jak również związki zawierające wiązania podwójne z heteroatomem, na przykład -C = O, -C = N, itp. W wyniku tego powstaje cykliczny węglowodór, dlatego ta reakcja jest również nazywana "cykloaddycją".
Ad
Synteza Dielsa-Adlera może zachodzić w obecności kwasów Lewisa, które znacznie przyspieszają przebieg reakcji i najczęściej przyczyniają się do dobrej wydajności głównego produktu, jak również wpływają na tworzenie się enancjomerów i izomerii cis / trans.
Przykładem takiej reakcji bez katalizatora jest dodanie butadienu-1,3 do para-benzochinonu w benzenie w temperaturze 35 ° C, w wyniku czego wydajność produktu osiąga 100%. Synteza przebiega z przeniesieniem protonów wodoru pomiędzy atomami węgla, tworząc drugi cykl i tworząc silny związek. Pod koniec reakcji powstaje pochodna 1,4-naftochinonu, która może dalej reagować z butadienem-1,3 w 100 ° С z utworzeniem cyklu po przeciwnej stronie. Antrachinon można otrzymać z końcowego produktu reakcji przez odwodornienie, którego pochodne stosuje się jako barwniki, na przykład alizarynę.
Ad
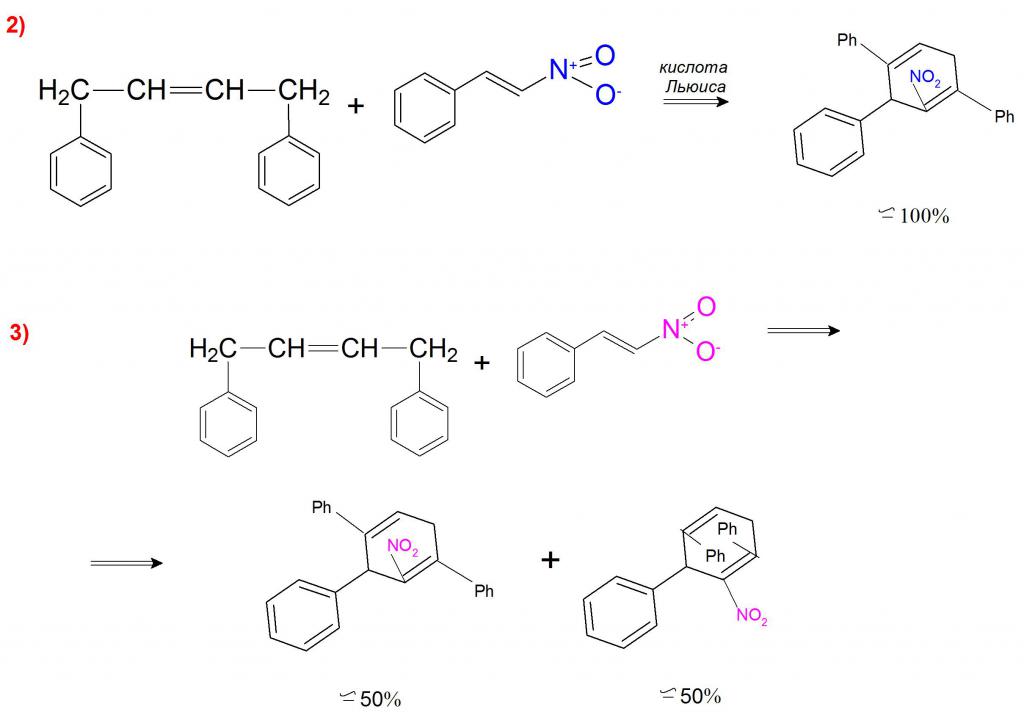
Przykładem syntezy katalitycznej może być reakcja 1,4-difenylobutadienu z β-nitrostyrenem, gdzie w obecności kwasu Lewisa powstaje tylko addukt endo-nitrowy (przykład 2). Bez udziału katalizatora reakcja zachodzi z wytworzeniem związków endonitro i produktów endo-difenylowych w stosunku 1: 1 (Przykład 3).
Takie reakcje potwierdzają celowość stosowania substancji aktywnych katalitycznie w syntezie dienowej, ponieważ znacznie przyspieszają proces i znacząco wpływają na pozycje regio- (orto-, para- i meta) i stereoselektywność (pozycje optyczne i endo- / egzo podstawników).