Teoria dysocjacji elektrolitycznej - jedna z głównych w chemii
Po rozpuszczeniu w wodzie substancje elektrolitowe rozkładają się na naładowane cząstki - jony. Przeciwieństwem jest molaryzacja lub powiązanie. Tworzenie się jonów wyjaśnia teorię dysocjacji elektrolitycznej (Arrheniusz, 1887). Na mechanizm rozkładu związków chemicznych podczas topienia i rozpuszczania mają wpływ charakterystyki rodzajów wiązań chemicznych, struktura i charakter rozpuszczalnika.
Elektrolity i nieprzewodniki
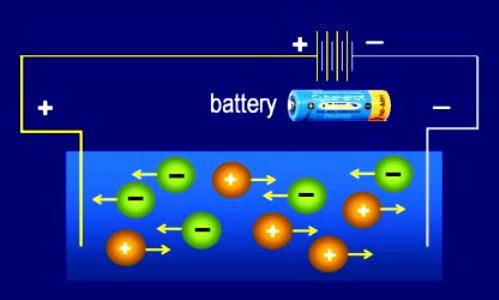
Destrukcja występuje w roztworach i topi się siatki krystaliczne i cząsteczki - dysocjacja elektrolityczna (ED). Rozkładowi substancji towarzyszy tworzenie się jonów, pojawianie się takich właściwości jak przewodnictwo elektryczne. Nie każdy związek jest w stanie dysocjować, ale tylko substancje, które początkowo składają się z jonów lub silnie polarnych cząstek. Obecność wolnych jonów wyjaśnia właściwości elektrolitów do przewodzenia prądu. Baza, sól, wiele nieorganicznych i niektórych kwasów organicznych posiada tę zdolność. Nieprzewodniki składają się z cząsteczek o niskiej polarności lub niepolarnych. Nie rozkładają się na jony, będąc nieelektrolitami (wieloma związkami organicznymi). Nośnikami ładunku są jony dodatnie i ujemne (kationy i aniony).
Rola S. Arrhenius i innych chemików w badaniu dysocjacji
Teorię dysocjacji elektrolitycznej potwierdził w 1887 r. Naukowiec ze Szwecji S. Arrhenius. Ale pierwsze obszerne badania właściwości roztworów przeprowadził rosyjski naukowiec M. Łomonosow. Przyczynił się do badania naładowanych cząstek powstałych w wyniku rozpuszczania substancji T. Grotgus i M. Faraday, R. Lenz. Arrhenius udowodnił, że wiele nieorganicznych elektrolitów i niektóre związki organiczne. Szwedzki naukowiec wyjaśnił przewodność elektryczną roztworów poprzez rozpad substancji w jony. Teoria dysocjacji elektrolitycznej Arrhenius nie przywiązywała wagi do bezpośredniego udziału cząsteczek wody w tym procesie. Rosyjscy naukowcy Mendelejew, Kablukow, Konovalov i inni wierzyli, że ma miejsce solwat - interakcja rozpuszczalnika i substancji rozpuszczonej. Jeśli chodzi o systemy wodne, używa się nazwy "hydratacja". Jest to złożony proces fizyczno-chemiczny, o czym świadczy tworzenie się hydratów, zjawisk cieplnych, odbarwianie materii i pojawianie się osadów.

Główne postanowienia teorii dysocjacji elektrolitycznej (TED)
Wielu naukowców pracowało nad wyjaśnieniem teorii S. Arrheniusa. Trzeba ją było poprawić, biorąc pod uwagę nowoczesne dane o strukturze atomu, wiązanie chemiczne. Zostały sformułowane główne postanowienia TED, które różnią się od klasycznych tez końca XIX wieku:
- Procesowi topnienia lub rozpuszczania towarzyszy dysocjacja elektrolitu w jony. Tak więc (na sugestię Faradaya) nazywane są cząstki o ładunku ("+" lub "-"), różnią się od neutralnych atomów w strukturze powłok walencyjnych i stabilności, są kolorowe i bezbarwne. Jony mogą być proste: Na + , Cl - , S 2- , Al 3+ . Są naładowane cząstki składające się z grup atomów: CO 2 , NH 4+ . Z języka greckiego nazwa "jon" jest tłumaczona jako "wędrowanie", co wskazuje na losowość propagacji tych cząstek.
- Uderzenie zewnętrznego pola elektrycznego powoduje, że jony przemieszczają się w uporządkowany sposób w przestrzeni elektrolitu. Każda ujemna cząstka jest kierowana do anody (elektrody dodatniej). Jony ze znakiem "+" zaczynają przesuwać się w kierunku katody (elektrody ujemnej).
- W tym samym czasie rozkład w jony i połączenie tych cząstek występują w roztworach, dlatego dysocjacja odnosi się do odwracalnych procesów fizykochemicznych.
Występujące zjawiska należy wziąć pod uwagę przy opracowywaniu równań: zastosować znak specjalny procesu odwracalnego, obliczyć ładunki ujemne i dodatnie: muszą pokrywać się w sumie.
Mechanizm substancji jonowych ED
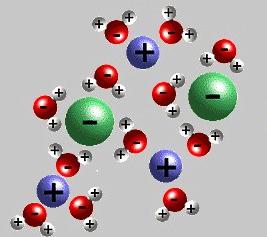
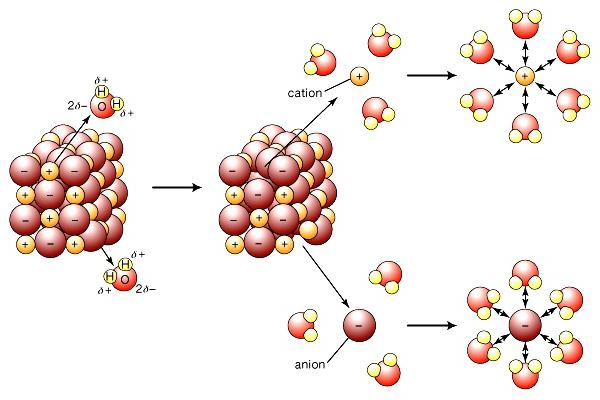
Współczesna teoria dysocjacji elektrolitycznej uwzględnia strukturę substancji elektrolitowych i rozpuszczalników. Po rozpuszczeniu wiązania między przeciwnie naładowanymi cząstkami w kryształach jonowych zostają zniszczone przez działanie cząsteczek wody polarnej. Dosłownie "wyciągają" jony z masy do roztworu. Rozpadowi towarzyszy tworzenie się powłoki solwatacyjnej (w wodzie - hydratacji) wokół jonów. Oprócz wody, ketonów, niższych alkoholi, mają wyższą stałą dielektryczną. Podczas dysocjacji chlorek sodu Jony Na + i Cl - rejestrują początkowy etap, któremu towarzyszy orientacja dipoli wodnych w stosunku do jonów powierzchniowych w krysztale. W końcowym etapie uwodnione jony są uwalniane i dyfundują do cieczy.
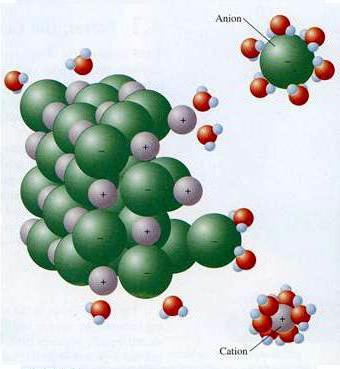
Mechanizm związków ED z wiązaniem kowalencyjnym silnie polarnym
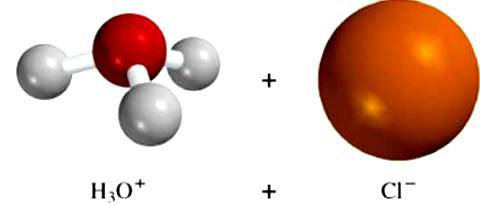
Cząsteczki rozpuszczalnika wpływają na strukturę krystaliczną niejonowych substancji. Na przykład wpływ dipoli wodnych na kwas chlorowodorowy prowadzi do zmiany typu wiązania w kowalencyjnej polarnej cząsteczce na jonową. Substancja dysocjuje, uwodniony wodór i jony chloru wchodzą do roztworu. Ten przykład dowodzi znaczenia procesów zachodzących pomiędzy cząstkami rozpuszczalnika i rozpuszczonym związkiem. To właśnie ta interakcja prowadzi do tworzenia się jonów elektrolitowych.
Teoria dysocjacji elektrolitycznej i główne klasy związków nieorganicznych
W świetle głównych przepisów TED, kwas można nazwać elektrolitem, podczas którego zaniku jonów dodatnich można wykryć jedynie proton H + . Dysocjacji zasady towarzyszy tworzenie lub uwalnianie z sieci krystalicznej tylko anionu OH i kationu metalu. Normalna sól po rozpuszczeniu daje dodatni jon metalu, a ujemny - pozostałość kwasu. Sól główna charakteryzuje się obecnością dwóch rodzajów anionów: grupy OH i reszty kwasowej. W kwaśnej soli kationów obecny jest tylko wodór i metal.
Wytrzymałość elektrolitu
Aby scharakteryzować stan substancji w roztworze, stosuje się wielkość fizyczną - stopień dysocjacji (α). Znajdź jego wartość ze stosunku liczby zepsutych cząsteczek do ich całkowitej liczby w roztworze. Głębokość dysocjacji zależy od różnych warunków. Ważne wskaźniki dielektryczne rozpuszczalnika, struktura rozpuszczonych związków. Zazwyczaj stopień dysocjacji zmniejsza się wraz ze wzrostem stężenia i wzrasta wraz ze wzrostem temperatury. Często stopień dysocjacji danej substancji wyraża się we frakcjach jednostki.
Klasyfikacja elektrolitu
Teoria dysocjacji elektrolitycznej pod koniec XIX wieku nie zawierała zapisu na temat interakcji jonów w roztworze. Wpływ cząsteczek wody na dystrybucję kationów i anionów wydawał się nieistotny dla Arrheniusa. Pomysły Arrheniusa na temat silnych i słabych elektrolitów były formalne. Na podstawie klasycznych pozycji można uzyskać α = 0,75-0,95 dla silnych elektrolitów. Eksperymenty wykazały nieodwracalność ich dysocjacji (α → 1). Sole rozpuszczalne, siarkowe i kwas chlorowodorowy alkalia. Częściowo dysocjować siarkowy, azotowy, fluorowodorowy, kwas fosforowy. Słabe elektrolity to kwasy krzemowe, octowe, wodorosiarczkowe i węglowe, wodorotlenek amonu, nierozpuszczalne zasady. Woda jest również określana jako słabe elektrolity. Niewielka część cząsteczek H 2 O ulega dysocjacji, a jony są jednocześnie molaryzowane.