Jaki jest rozkład elektronów w poziomach energetycznych różnych pierwiastków chemicznych?
Rozkład elektronów w poziomach energetycznych wyjaśnia metaliczne, a także niemetaliczne właściwości dowolnych pierwiastków.
Formuła elektroniczna
Istnieje pewna zasada, zgodnie z którą wolne i sparowane cząstki ujemne są umieszczane na poziomach i podpoziomach. Rozważmy bardziej szczegółowo rozkład elektronów według poziomów energii.
Na pierwszym poziomie energii są tylko dwa elektrony. Orbitale są przez nie napełniane, gdy wzrasta podaż energii. Rozkład elektronów w atomie pierwiastka chemicznego odpowiada numerowi sekwencji. Na poziomach energii o minimalnej liczbie najbardziej widocznych grawitacja walencyjne elektrony do jądra.
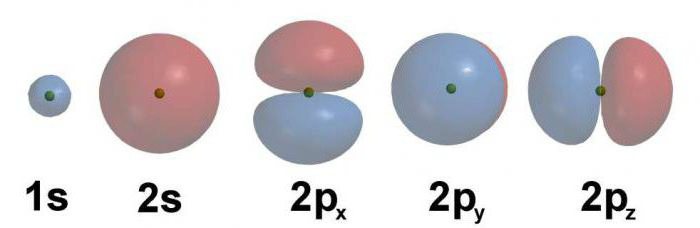
Przykład formuły elektronicznej
Rozważ rozmieszczenie elektronów przez poziomy energii na przykładzie atomu węgla. Jego numer sekwencyjny wynosi 6, dlatego sześć protonów z dodatnim ładunkiem znajduje się w jądrze. Biorąc pod uwagę, że węgiel jest przedstawicielem drugiego okresu, charakteryzuje się obecnością dwóch poziomów energii. Na pierwszym są dwa elektrony, na drugim - cztery.
Ad
Reguła Hunda wyjaśnia rozmieszczenie w tej samej komórce tylko dwóch elektronów, które mają różne spiny. Na drugim poziomie energii są cztery elektrony. W rezultacie rozkład elektronów w atomie pierwiastka chemicznego ma następującą formę: 1s22s22p2.
Istnieją pewne zasady, według których rozkład elektronów według podpoziomów i poziomów.
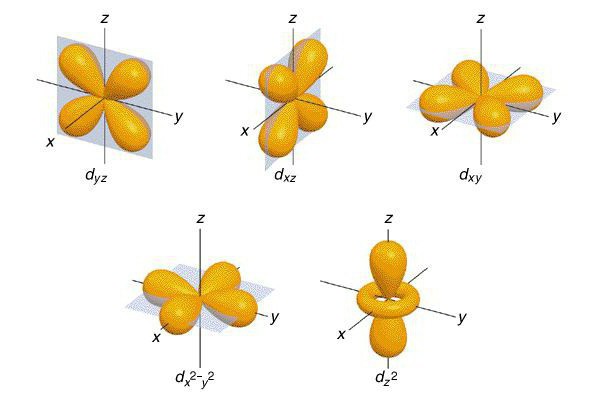
Zasada Pauliego
Zasada ta została sformułowana przez Pauliego w 1925 roku. Naukowiec zgodził się na możliwość umieszczenia w atomie tylko dwóch elektronów o tych samych liczbach kwantowych: n, l, m, s. Zwróć uwagę, że rozkład elektronów w poziomach energii występuje w miarę wzrostu ilości energii swobodnej.
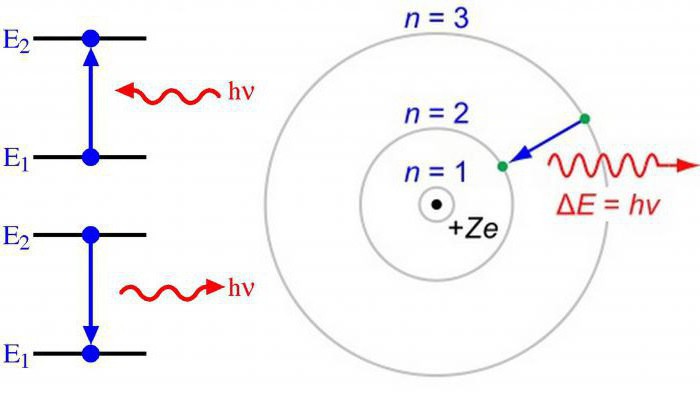
Reguła Klechkowski
Wypełnianie orbitali energetycznych odbywa się zgodnie ze wzrostem liczb kwantowych n + 1 i charakteryzuje się wzrostem rezerwy energii.
Rozważ rozmieszczenie elektronów w atomie wapnia.
W stanie normalnym jego formuła elektroniczna ma następującą postać:
Ca 1s2 2s2 2p6 3s2 3p6 3d0 4s2.
Elementy podobnych podgrup związanych z elementami d- i f, występuje "awaria" elektronu z zewnętrznego podpoziomu, który ma mniejszą rezerwę energii, na poprzedni poziom pod- lub f. Podobne zjawisko jest charakterystyczne dla miedzi, srebra, platyny, złota.
Ad
Rozkład elektronów w atomie obejmuje wypełnianie podpoziomów niesparowanymi elektronami, które mają te same spiny.
Dopiero gdy wszystkie wolne orbitale są całkowicie wypełnione pojedynczymi elektronami, komórki kwantowe są uzupełniane przez drugie ujemne cząstki obdarzone przeciwnymi spinami.
Na przykład w nieokreślonym stanie azotu:
1s2 2s2 2p3.
Właściwości substancji mają wpływ konfiguracja elektroniczna elektrony walencyjne. Według ich liczby można określić wyższą i niższą wartościowość, aktywność chemiczną. Jeśli element znajduje się w głównej podgrupie układu okresowego, numer grupy umożliwia określenie zewnętrznego poziomu energii, określenie go stany utleniania. Na przykład, fosfor, który znajduje się w piątej grupie (główna podgrupa), zawiera pięć elektronów walencyjnych, dlatego jest w stanie przyjąć trzy elektrony lub dać pięć cząsteczek do innego atomu.
Ad
Wyjątkami od tej zasady są wszyscy przedstawiciele podgrup układu okresowego.
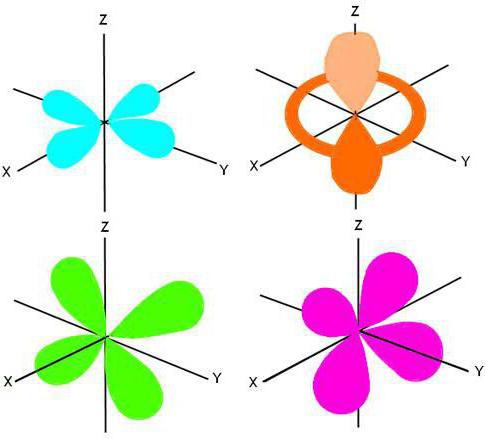
Funkcje rodzinne
W zależności od struktury zewnętrznego poziomu energii, w układzie okresowym występuje podział wszystkich neutralnych atomów na cztery rodziny:
- s-elementy znajdują się w pierwszej i drugiej grupie (główne podgrupy);
- rodzina p znajduje się w grupach III-VIII (podgrupy A);
- d-elementy można znaleźć w podobnych podgrupach z grupy I do VIII;
- Rodzina f składa się z aktynowców i lantanowców.
Wszystkie s-elementy w stanie normalnym mają elektrony walencyjne na pod-poziomie s. Obecność wolnych elektronów na poziomach podtypu s i p jest charakterystyczna dla elementów p.
D-pierwiastki w nieokreślonym stanie mają elektrony walencyjne zarówno na ostatnim s-, jak i na ostatnim, ale jednym d-podpoziomie.
Wniosek
Stan dowolnego elektronu w atomie można opisać za pomocą zestawu podstawowych liczb. W zależności od charakterystyki jego struktury możemy mówić o pewnej ilości energii. Korzystając z reguły Hunda, Klechkowskiego, Pauliego dla dowolnego elementu zawartego w układzie okresowym, możesz utworzyć neutralną konfigurację atomu.
Elektrony znajdujące się na pierwszych poziomach mają najmniejszą ilość energii w stanie niezwiązanym. Gdy podgrzewany jest obojętny atom, obserwuje się przejście elektronów, któremu zawsze towarzyszy zmiana liczby wolnych elektronów, co prowadzi do znaczącej zmiany szybkości utleniania pierwiastka i zmiany jego aktywności chemicznej.