Nieprawidłowe właściwości wody: przyczyny, znaczenie
Ludzie są przyzwyczajeni do wody i uważają ją za zwykłą substancję. Często przyjmują to za pewnik, dopóki susze nie zagrażają uprawom i wodzie pitnej, a poważne powodzie stanowią zagrożenie dla życia i mienia. Wielu nie zdaje sobie sprawy, że struktura wody i jej anomalne właściwości zapewniają egzystencję życia na Ziemi.
Jeden z pierwszych filozofów greckich, Tales of Miletus (640-546 pne, E.), Zbadał uniwersalny charakter wody. Uważał to za główny element, z którego wszystko się rodzi. Obfitość wody była oczywista, ale Thales zauważył, że jest to jedyna substancja naturalnie obecna na Ziemi w tym samym czasie w trzech różnych stanach: stałym, ciekłym i gazowym. W mroźne zimowe dni śnieg i lód pokrywają pola, rzeka płynie w pobliżu, a nad głową płyną chmury.
Ad
Formy materii
Wszystkie substancje występują w trzech różnych stanach, które zależą od temperatury i ciśnienia. Ciała stałe mają określony kształt i mają krystaliczną strukturę wewnętrzną. Według tej definicji substancja taka jak szkło będzie uważana za ciecz o dużej lepkości, ponieważ nie ma struktury krystalicznej. Bryły mają tendencję do opierania się zewnętrznym wpływom. Można je przekształcić w ciecz poprzez ogrzewanie. Temperatura zamarzania wody przy ciśnieniu 1 atmosfery wynosi 0 ° C, poniżej której występuje w postaci lodu.
Ciecz, w przeciwieństwie do ciała stałego, nie ma twardości i nie ma określonej formy. Ma objętość i przyjmuje postać naczynia, w którym jest przechowywany. Wpływ zewnętrzny wymusza przepływ. Woda jest cieczą między temperaturami zamarzania i wrzenia (100 ° C). Ciecze mogą przenosić się do fazy gazowej po podgrzaniu powyżej temperatury wrzenia.
Ad
Gaz nie ma formy ani objętości. Ma kształt i zajmuje objętość naczynia, w którym się znajduje. Gaz rozszerza się i kurczy ze zmianami temperatury i ciśnienia i może łatwo dyfundować do innych gazów.

Punkty wrzenia i zamrożenia
Nieprawidłowe właściwości wody to niezwykle wysoka temperatura wrzenia i zamarzania w porównaniu z innymi związkami o podobnej strukturze cząsteczkowej. Inne podobne substancje w normalnych warunkach to gazy. Oczekuje się, że woda o niższej masie cząsteczkowej niż podobne związki będzie miała niższą temperaturę wrzenia i zamarzania. Jednak ze względu na polarny charakter jego cząsteczek i wiązań wodorowych, jego temperatura wrzenia wynosi 100 ° C, a zamrożenie wynosi 0 ° C. Dla porównania, odpowiednie wartości dla siarkowodoru H2S wynoszą -60 ° C i -84 ° C, dla siarkowodoru H 2 Se, wskaźnik ten wynosi -42 ° C i -64 ° C, a tellur dla -2 ° C i -49 ° C .
Faza stała
Z reguły przy spadku temperatury substancje stają się gęstsze, a woda nie jest wyjątkiem. Jego gęstość w 25 ° C wynosi 0,997 g / ml i wzrasta do maksimum (1 g / ml) w T = 4 ° C. W metrycznym systemie pomiarowym kilogram jest zdefiniowany jako masa 1 litra wody o maksymalnej gęstości. Zdumiewająca rzecz dzieje się między 4 ° C a temperaturą krzepnięcia 0 ° C, co obserwuje się w bardzo małej liczbie substancji. Woda stopniowo się rozszerza, stając się mniej gęsta. Gęstość lodu w 0 ° C wynosi około 0,917 g / ml. Cząsteczki wody tworzą kryształy w kształcie czworościanu (czworościenne figury, z których każda ma trójkąt równoboczny). Ponieważ gęstość fazy stałej jest mniejsza niż ciecz, lód płynie. Po zamrożeniu objętość wody wzrasta o 1%.
Ad
Bardzo ważne jest, aby lód rozszerzał się i unosił na powierzchni. Z tego powodu w zimie pękają rury wodociągowe, a na drogach pojawiają się dziury. Zamrażanie i topnienie wody są w dużej mierze odpowiedzialne za niszczenie skał i tworzenie się gleby. Ponadto, jeżeli jeziora i strumienie zamarzłyby w górę, ogólnie życie wodne przestałoby istnieć, a warunki klimatyczne i pogodowe uległyby radykalnej zmianie.

Pojemność cieplna
Inną nienormalną właściwością wody jest jej wyjątkowo wysoka zdolność do absorbowania ciepła bez znaczącego wzrostu temperatury. Na przykład letnie słońce na plaży rozgrzewa piasek do tego stopnia, że nie można na nim chodzić. Woda pozostaje chłodna. Obie substancje pochłaniają równą ilość energii cieplnej, ale temperatura piasku jest wyższa. Pusty żelazny garnek wiszący nad ogniem szybko zacznie świecić na czerwono, ale jeśli jest napełniony wodą, to jest podgrzewany stopniowo. Wysoka pojemność cieplna wody sprawia, że jest to dobry środek chłodzący w skraplaczach i chłodnicach samochodowych, które zapobiegają przegrzaniu silnika. Jego wartość jest 5-krotnie większa niż pojemność cieplna piasku i około 10-krotność żelaza.
Ad
Klimat umiarkowany w obszarach przybrzeżnych jest wynikiem absorpcji w ciągu dnia dużej ilości słonecznej energii cieplnej przez wodę i powolnego jej uwalniania w nocy. W głębi lądu z dala od wybrzeża zwykle występują znacznie wyższe temperatury ekstremalne. Ogromne oceany na Ziemi (około 75% powierzchni) są odpowiedzialne za łagodzenie klimatu na naszej planecie, wspierając istnienie życia.
Ciepło topnienia i parowania
Ciepło przejścia fazowego jest związane z pojemnością cieplną. Jest to ilość energii cieplnej pochłonięta lub uwolniona przez substancję, która zmienia się w fazie (z cieczy na ciało stałe lub odwrotnie, z cieczy na gaz lub odwrotnie) bez zmiany temperatury. Niezwykle wysokie wartości ciepła właściwego topnienia (332,4 kJ / kg) i parowania (2256 kJ / kg) są kolejnymi anomalicznymi właściwościami fizycznymi wody. Zamrażanie wytwarza taką samą ilość ciepła, która jest absorbowana podczas procesu topienia.

Praktycznym przykładem zastosowania określonego ciepła topnienia wody jest użycie lodu do schłodzenia napojów w izolowanej chłodnicy. W procesie topienia lodu pochłania energię cieplną napojów, utrzymując je w chłodzie. Pojemnik z wodą w szklarni w mroźną zimową noc zmiękczy temperaturę w pomieszczeniu z powodu ciepła uwalnianego podczas zamrażania. Kondensacja pary uwalnia taką samą ilość ciepła, która jest pochłaniana podczas procesu parowania. Ciepło właściwe parowania jest 5-krotnie wyższe od temperatury wymaganej do podniesienia temperatury z 0 do 100 ° C. Nieprawidłowa właściwość wody do magazynowania dużej ilości skumulowanej energii cieplnej sprawia, że ogrzewanie parą jest wydajne. W procesie kondensacji para uwalnia nagromadzoną energię cieplną. Dzienna burza w upalny letni dzień to kolejny przykład uwalniania energii cieplnej w górnych warstwach atmosfery podczas kondensacji gorącego, wilgotnego powietrza. Nawet huragan jest przykładem efektu redystrybucji ogromnych ilości energii cieplnej pochłanianej przez tropikalne oceany.
Ad
Systemy chłodzenia wyparnego działają odwrotnie. Woda w procesie parowania absorbuje energię cieplną z powietrza, chłodząc ją.
Uniwersalny rozpuszczalnik
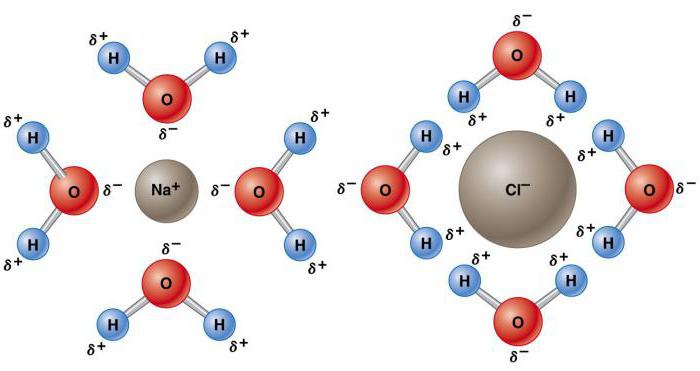
Rozpuszczalnik jest w stanie rozpuścić inną substancję z utworzeniem jednorodnej mieszaniny (roztworu) na poziomie molekularnym. Inną nieprawidłową właściwością wody w chemii ze względu na jego polarność jest zdolność do rozpuszczania innych związków polarnych - soli, alkoholi, związków karboksylowych itp. Więcej substancji rozpuszcza się w wodzie niż w jakimkolwiek innym rozpuszczalniku. Więcej niż połowa znanych pierwiastków chemicznych znajduje się w niej, niektóre w wysokich stężeniach, a inne tylko w śladowych ilościach. Na przykład stężenie nasycenia chlorku sodu wynosi około 36 g na 100 ml, a węglanu wapnia około 0,0015 g. Zdolność wody do rozpuszczania substancji zależy od jej składu chemicznego, wytrzymałości wiązań chemicznych pierwiastków, temperatury i pH.
Związki niepolarne, w tym większość węglowodorów, rozpuszczają się w niewielkich lub śladowych ilościach. Na przykład oleje mają tendencję do unoszenia się na powierzchni wody.

Napięcie powierzchniowe
Nieprawidłowe właściwości wody obejmują najwyższe (po rtęciu) napięcie powierzchniowe w porównaniu z jakimkolwiek innym płynem. Jest to siła przyciągania cząsteczek znajdujących się pod powierzchnią i tych znajdujących się na granicy faz ciecz-powietrze. Chroni wodę przed rozprzestrzenianiem się. Związki polarne z reguły mają znacznie wyższe napięcie powierzchniowe niż związki niepolarne. Woda nie jest wyjątkiem. W temperaturze 20 ° C wskaźnik ten wynosi 0,07286 N / m (dla alkoholu etylowego - 0,0228 N / m).
Bez wpływu zewnętrznego kropla H 2 O przyjmuje postać kuli, ponieważ ta liczba ma najmniejszą powierzchnię na jednostkę objętości. Krople deszczu to małe pociski, które niszczą skały. Z tego samego powodu obiekty cięższe od wody można trzymać na powierzchni. Owady mogą chodzić po nim i pływać żyletkami.
Wiązanie wodorowe określa anomalną właściwość wody, aby zmoczyć większość powierzchni. Takie substancje są uważane za hydrofilowe. Woda może unosić się wzdłuż ścian szkła i innych pojemników. Inne substancje, takie jak oleje, tłuszcze, wosk i syntetyki (polipropylen itp.), Nie ulegają zamoczeniu. Są hydrofobowe. Wkłady filtra membranowego o wielkości porów poniżej 1 mikrona są wykonane z polimerów hydrofobowych za pomocą środków zwilżających, które zmniejszają napięcie powierzchniowe wody, dzięki czemu mogą one penetrować i pozostać w nich. Zjawisko to nazywane jest efektem kapilarnym. Jest odpowiedzialny za ruch wody w glebie i wzdłuż korzeni roślin i krwi przez naczynia krwionośne.

Nieprawidłowe właściwości wody i ich znaczenie dla życia
H 2 O jest integralnym składnikiem istnienia wszelkiego życia. To tłumaczy ostatnie zainteresowanie znalezieniem wody w innych częściach wszechświata. Wszystkie znane procesy biochemiczne zachodzą w środowisku wodnym. Większość żywych istot zawiera wagowo 70-80% H2O.
Ponadto woda odgrywa znaczącą rolę w procesie fotosyntezy. Rośliny wykorzystują promienistą energię słońca do przekształcenia wody i dwutlenku węgla w węglowodany: 6CO 2 + 6H 2 O + 672 kcal → C 6 H 12 O 6 + 6O 2 . Fotosynteza to najbardziej podstawowa i ważna reakcja chemiczna na Ziemi. Dostarcza substancje odżywcze, bezpośrednio lub pośrednio, wszystkim żywym organizmom i jest głównym źródłem tlenu atmosferycznego.
Nieprawidłowe właściwości wody i ich przyczyny
Zdolność pierwiastków do tworzenia związków zależy od zdolności ich atomów do oddawania lub przyjmowania elektronów. Elementy pierwszego typu stają się dodatnio naładowanymi jonami (kationami), a drugiego typu - ujemnie naładowanymi anionami.
Zdolność pierwiastka do interakcji z innymi pierwiastkami do tworzenia związków nazywana jest wartościowością. Odpowiada liczbie otrzymanych lub oddanych elektronów. W przypadku związków nieorganicznych, suma algebraiczna liczb walencyjnych pierwiastków wynosi zero. Elektrostatyczne przyciąganie przeciwnie naładowanych jonów w celu utworzenia związku nazywa się wiązanie jonowe.
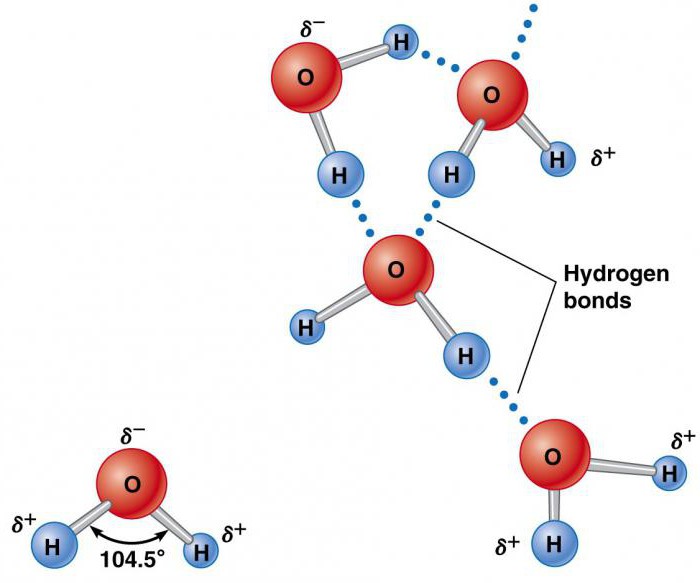
Pierwiastki tworzące wodę (wodór i tlen) występują osobno w cząsteczkach H2 i O2 zawierających po dwa atomy. Są one utrzymywane razem przez wymianę pary elektronów w wiązaniu chemicznym zwanym wiązaniem kowalencyjnym. Jest znacznie silniejszy niż jon. Dwa atomy trzymane razem wiązanie kowalencyjne tworzą znacznie bardziej stabilną cząsteczkę niż jej części składowe. W nim wodór jest łączony przez tlen za pomocą zwykłych par elektronów. Ta wyjątkowa dystrybucja elektronów w powstałym związku chemicznym powoduje, że atomy H są pozycjonowane względem O pod kątem 104,5 °.
Nieprawidłowe właściwości fizyczne wody są wyjaśnione przez jej strukturę i wiązanie chemiczne.
Atom tlenu ma względnie silny wpływ na całkowitą parę elektronów, w wyniku czego atomy wodoru stają się elektrododatnie, a atom tlenu - region elektroujemny. Ponieważ obszary naładowane dodatnio i ujemnie są rozmieszczone nierównomiernie względem punktu centralnego, cząsteczka wody jest polarna.
Taka natura sprawia, że staje się on atrakcyjny elektrostatycznie dla innych cząsteczek H2O, a także jonów i powierzchni kontaktowych z obszarami naładowanymi. Elektropozytywne atomy wodoru są przyciągane do elektroujemnych atomów tlenu sąsiadujących cząsteczek wody. Zjawisko to nazywane jest wiązaniem wodorowym. Jego siła jest tylko około 10% kowalencyjna, ale jest odpowiedzialna za większość anomalnych fizycznych właściwości wody. Należą do nich wysokie temperatury krzepnięcia i wrzenia, pojemność cieplna, ciepło właściwe topnienia i parowania, rozpuszczalność i napięcie powierzchniowe.
Wiązanie wodorowe jest odpowiedzialne za utrzymanie integralności cząsteczki H 2 O podczas reakcji chemicznych. Podczas gdy inne związki ulegają jonizacji, sama woda zachowuje swoją chemiczną integralność. Tylko stosunkowo niewielka liczba cząsteczek ulega jonizacji na jony wodorowe i hydroksylowe. Dlatego H 2 O jest stosunkowo słabym przewodnikiem prądu elektrycznego. Konkretna wytrzymałość teoretycznie czystej wody wynosi 18,3 MΩ cm, podczas gdy opór napoju ma opór właściwy mniejszy niż 10 000 Ω cm. W ten sposób można łatwo sprawdzić czystość H 2 O.
Anomalne właściwości wody tłumaczy się obecnością wiązań wodorowych, dzięki czemu występuje niewielka gęstość lodu. Wzdłuż nich podczas zamrażania znajdują się cząsteczki, co prowadzi do ekspansji substancji. Z tego powodu lód unosi się na powierzchni wody. Zwiększone ciśnienie obniża temperaturę topnienia. Nacisk stworzony przez ostrze łyżwy topi lód, tworząc warstwę, która zapewnia elegancki poślizg. Nawet przy bardzo niskich temperaturach, wysokie ciśnienie osłabia sieć krystaliczna. Jest to powód, dla którego ogromne masy lodowe, takie jak lodowce, stopniowo się przemieszczają.
Dipole moment
Polarny charakter cząsteczki wody sprawia, że orientuje się w polu elektrycznym lub magnetycznym. Elektronegatywny atom tlenu jest dopasowany do bieguna dodatniego, a elektrododatnie atomy wodoru - w kierunku ujemnym. Woda ma wyjątkowo duży moment dipolowy, który jest iloczynem odległości między ładunkami pomnożonej przez ilość ładunku.
Stała dielektryczna jest inną właściwością związaną z momentem dipolowym. Cząsteczki wody poprzez ustawienie w polu elektrycznym mają tendencję do neutralizowania go i tworzenia odporności na przenoszenie ładunku elektrostatycznego. Stała dielektryczna substancji jest określana przez ε w równaniu F = Q1 ∙ Q2 / ε ∙ r 2 , gdzie F jest siłą między dwoma ładunkami Q, podzieloną przez odległość r w ośrodku.
Wraz ze wzrostem stałej dielektrycznej siła między ładunkami maleje. Wysoka stała dielektryczna redukuje siłę przyciągania jonów, co tłumaczy anomalne właściwości chemiczne wody w celu rozpuszczenia wielu różnych substancji.
Wniosek
W przypadku ludzi woda jest powszechnie stosowaną substancją, którą często przyjmuje się za pewnik. Pomimo faktu, że anomalne właściwości wody są wyjaśnione na poziomie atomowym, jej znaczenie jest rzeczywiście duże. Oczywiście konieczne jest istnienie życia na Ziemi. Nieprawidłowe właściwości wody, w skrócie, pozwalają jej służyć jako mediator procesów chemicznych i biochemicznych, kształtować nasze środowisko naturalne i uczestniczyć w tworzeniu klimatu i pogody.