Wiązanie kowalencyjne: pojęcie, znaki, znaczenie chemiczne
Ważny rodzaj więzi między atomami
Wiązanie kowalencyjne wraz z jonowym jest głównym typem wiązanie chemiczne. Charakteryzuje on zdolność atomów do wzajemnego oddziaływania i tworzenia gęstych skorup na poziomie elektronów, które służą jako podstawa dla cząsteczek o zupełnie nowych właściwościach.
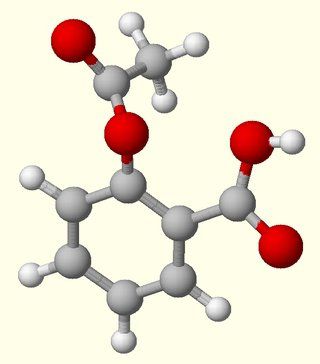
Pojęcie i chemiczne znaczenie tego typu wiązania chemicznego
Zgodnie z zasadą wiązanie kowalencyjne ma bardzo powszechny charakter. rodzaj wiązania chemicznego w którym następuje zjednoczenie elektronów atomów, w wyniku czego powstaje wspólny orbital molekularny. Ta nowo utworzona powłoka umożliwia atomom doprowadzenie liczby ich elektronów do liczby, jaką może pomieścić ich zewnętrzna orbita. W rezultacie cząsteczka zyskuje stabilność i stabilność.
Ad

Najważniejsze cechy i właściwości
Termin "wiązanie kowalencyjne" oznacza pożądanie interakcji atomów z innymi atomami, ich zdolność do tworzenia stabilnego związku. Takie wiązanie może zachodzić zarówno pomiędzy identycznymi atomami (na przykład wodorem lub chlorem), jak i pomiędzy różnymi atomami (na przykład w cząsteczkach siarkowodoru, kwas chlorowodorowy). W pierwszym przypadku powstaje specyficzna chmura elektronowa, której cząstki elementarne, znajdujące się na zewnętrznych orbitach, zaczynają służyć obu rdzeniom, nie zwracając uwagi na to, czy są one "własne" czy "obce".
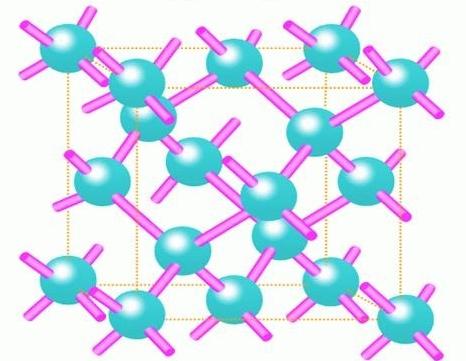
Dążenie do obniżenia kosztów energii
Głównym powodem, że atomy mają tendencję do pozyskiwania brakującego elektronu do ich zewnętrznej powłoki, jest ich pragnienie obniżenia kosztów energii. W końcu od dawna wiadomo, że całkowita energia cząsteczki tego samego wodoru jest znacznie niższa niż suma energii dwóch atomów tego samego pierwiastka. Zatem wiązanie kowalencyjne jest naturalną reakcją materii na chęć znacznego obniżenia kosztu zasobów dla jego istnienia.
Ad
Kolejna ważna konsekwencja
W tworzeniu i dalszym istnieniu tych związków istnieje inna ważna prawidłowość. Faktem jest, że wiązanie kowalencyjne opiera się na pewnych odległościach między atomami w cząsteczce. Nie mogą być mniejsze niż pewna wartość, ponieważ w przeciwnym razie system straci stabilność, a jego energia gwałtownie wzrośnie. Ta nieruchomość jest aktywnie wykorzystywana w różnych sektorach gospodarki narodowej, na przykład w przemyśle jądrowym.
Słynna zasada Lewisa
Więź kowalencyjna, której właściwości są obecnie aktywnie badane w obecnym czasie, działa na podstawie słynnej zasady oktetów-dubletów, która została sformułowana w tym czasie przez słynnego chemika Lyis. Zgodnie z jego koncepcją, tworzenie tego rodzaju wiązania wymaga takiej liczby elektronów, aby zewnętrzne powłoki atomów stały się kompletne, podobnie jak struktura gazów obojętnych. Na przykład w cząsteczce wodoru jej elementy składowe przypominają hel, aw cząsteczce chloru argon.