Acetylen: właściwości chemiczne, przygotowanie, zastosowanie, środki ostrożności
Acetylen (lub zgodnie z międzynarodową nomenklaturą, etyina) jest nienasyconym węglowodorem należącym do klasy alkinów. Wzór chemiczny acetylenu to C2H2. Atomy węgla w cząsteczce są połączone potrójnym wiązaniem. Jest pierwszym w swojej homologicznej serii. Jest to bezbarwny gaz. Produkt wysoce łatwopalny.
Pierwsze
Wszystkie metody przemysłowej produkcji acetylenu zbiegają się w dwóch rodzajach: hydrolizy węglika wapnia i pirolizy różnych węglowodorów. Ten ostatni wymaga mniej energii, ale czystość produktu jest dość niska. Metoda węglika jest odwrotna.
Istotą pirolizy jest to, że metan, etan lub inny lekki węglowodór zamienia się w acetylen po podgrzaniu do wysokiej temperatury (od 1000 ° C). Ogrzewanie można przeprowadzić za pomocą wyładowania elektrycznego, plazmy lub palącej części surowca. Problem polega jednak na tym, że w wyniku reakcji pirolizy powstaje nie tylko acetylen, ale także wiele innych produktów, które należy później usunąć.
Ad
2CH 4 → C2H2 + 3H2
Metoda węglika oparta jest na reakcji interakcji węglika wapnia z wodą. Węglik wapnia jest otrzymywany z jego tlenku przez stapianie z koksem w piecach elektrycznych. Stąd tak duże zużycie energii. Ale czystość acetylenu uzyskanego w ten sposób jest wyjątkowo wysoka (99,9%).
CaC2 + H2O → C2H2 + Ca (OH) 2
W laboratorium acetylen można również otrzymać przez dehydrohalogenację dihalogenowych pochodnych alkanów przy użyciu alkoholowego roztworu alkalicznego.
CH 2 Cl-CH 2Cl + 2KOH → C 2H 2 + 2KCl + 2H 2 O
Właściwości fizyczne acetylenu
Acetylen to gaz bez koloru i zapachu. Chociaż zanieczyszczenia mogą nadać mu zapach czosnku. Praktycznie nierozpuszczalny w wodzie, słabo rozpuszczalny w acetonie. W temperaturze -83,8 ° C jest upłynniany.
Ad
Właściwości chemiczne acetylenu
W oparciu o potrójne wiązanie acetylenu, będzie charakteryzował się reakcjami addycji i reakcje polimeryzacji. Atomy wodoru w cząsteczce acetylenu można zastąpić innymi atomami lub grupami. Dlatego można powiedzieć, że acetylen wykazuje właściwości kwasowe. Zbadajmy chemiczne właściwości acetylenu w określonych reakcjach.
Reakcje załączników:
- Uwodornienie. Przeprowadza się go w wysokiej temperaturze i w obecności katalizatora (Ni, Pt, Pd). Na katalizatorze palladowym może być niecałkowite uwodornienie.
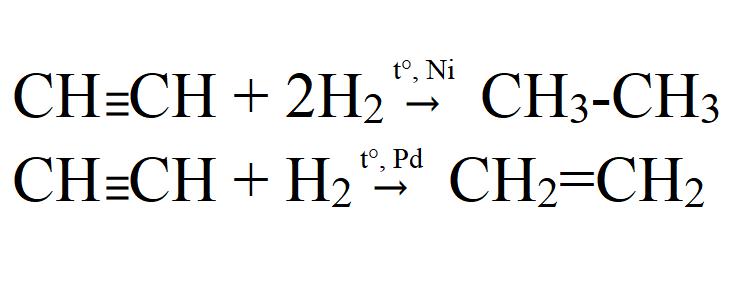
- Halogenowanie Może być zarówno częściowy, jak i kompletny. Jest łatwy nawet bez katalizatora lub ogrzewania. W świetle chlorowania dochodzi do wybuchu. W tym samym czasie acetyl rozkłada się całkowicie na węgiel.
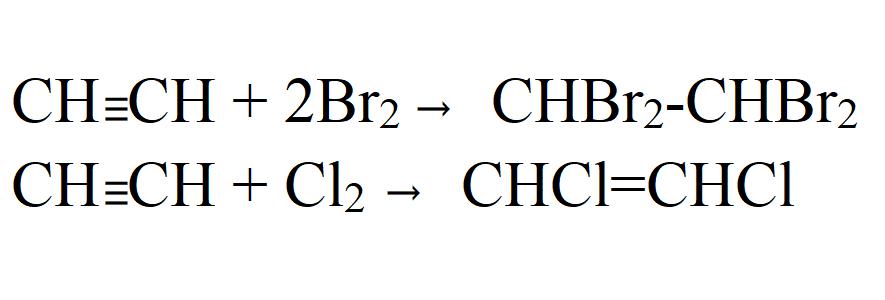
- Dostęp do kwasu octowego i alkoholu etylowego. Reakcje zachodzą tylko w obecności katalizatorów.
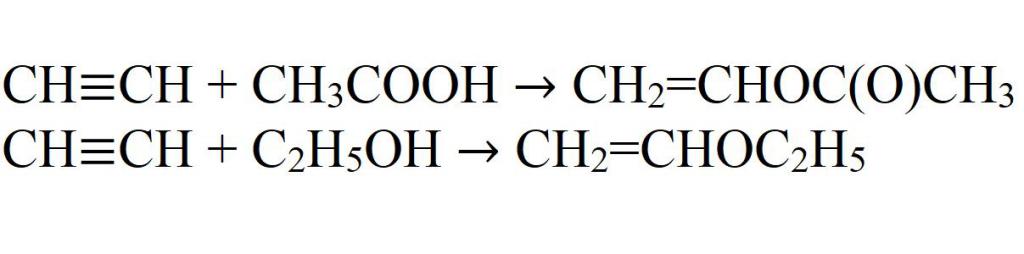
- Dodanie kwasu cyjanowodorowego.
CH≡CH + HCN → CH 2 = CH-CN
Reakcje substytucji:
- Interakcja acetylenu ze związkami metaloorganicznymi.
CH≡CH + 2C2H5MgBr → 2C2H6 + BrMgC≡CMgBr
- Interakcja z metalicznym sodem. Konieczna jest temperatura 150 ° C lub wstępne rozpuszczanie sodu w amoniaku.
2CH≡CH + 2Na → 2CH≡CNa + H 2
- Interakcja ze złożonymi solami miedzi i srebra.
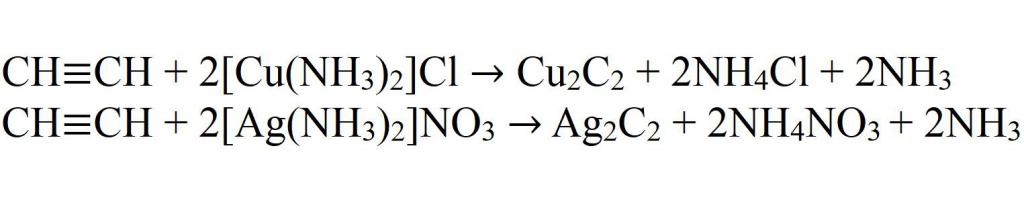
- Interakcje z amidem sodu.
CH≡CH + 2NaNH2 → NaC≡CNa + 2NH 3
Reakcje polimeryzacji:
- Dimeryzacja. W tej reakcji dwie cząsteczki acetylenu są połączone w jeden. Potrzebny jest katalizator - monowalentna sól miedzi.
- Trimeryzacja. W tej reakcji trzy cząsteczki acetylenu tworzą benzen. Wymagane jest ogrzewanie do 70 ° C, ciśnienie i katalizator.
- Tetrameryzacja. W wyniku reakcji otrzymuje się ośmioczłonowy cykl - cyklooktatetraen. Reakcja ta wymaga również niewielkiej ilości ciepła, ciśnienia i odpowiedniego katalizatora. Są to zazwyczaj złożone związki dwuwartościowego niklu.
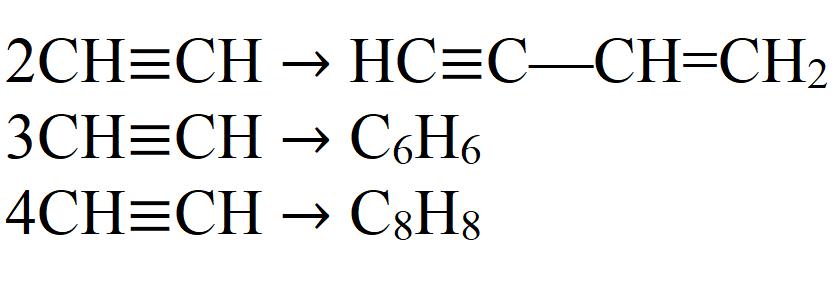
To nie wszystkie właściwości chemiczne acetylenu.
Aplikacja
Wzór strukturalny acetylenu pokazuje nam dość silne wiązanie między atomami węgla. Kiedy się rozpada, na przykład podczas spalania, uwalniana jest duża ilość energii. Z tego powodu płomień acetylenu ma rekordowo wysoką temperaturę około 4000 ° C. Stosowany jest w pochodniach do spawania i cięcia metalu, a także w silnikach rakietowych.
Ad
Płomień spalania acetylenu ma również bardzo dużą jasność, dlatego często jest stosowany w urządzeniach oświetleniowych. Jest stosowany w technologii wybuchowej. To prawda, że sam acetylen nie stosuje się, ale jego sole.
Jak można zauważyć z różnych właściwości chemicznych, acetylen może być stosowany jako surowiec do syntezy innych ważnych substancji: rozpuszczalników, lakierów, polimerów, włókien syntetycznych, tworzyw sztucznych, szkła organicznego, materiałów wybuchowych i kwasu octowego.
Bezpieczeństwo
Jak już wspomniano, acetylen jest substancją łatwopalną. Z tlenem lub powietrzem może tworzyć ekstremalnie łatwopalne mieszaniny. Aby spowodować wybuch, wystarczy pojedyncza iskra od elektryczności statycznej, ogrzewanie do 500 ° C lub małe ciśnienie. W temperaturze 335 ° C czysty acetyl spontanicznie się zapala.
Ad
Z tego powodu acetylen przechowuje się w butlach pod ciśnieniem, które są wypełnione porowatą substancją (pumeks, węgiel aktywny, azbest). W ten sposób acetyl jest rozprowadzany w porach, zmniejszając ryzyko wybuchu. Często pory te są impregnowane acetonem, dzięki czemu powstaje roztwór acetylenu. Czasami acetylen rozcieńcza się innymi, bardziej obojętnymi gazami (azot, metan, propan).
Ten gaz ma także działanie toksyczne. Po inhalacji rozpocznie się odurzenie organizmu. Oznaki zatrucia to nudności, wymioty, szumy w uszach i zawroty głowy. Duże stężenia mogą nawet prowadzić do utraty przytomności.