Aldehydy i ketony. Formuła, przygotowanie, zastosowanie
Spośród związków organicznych zawierających tlen ogromne znaczenie mają dwie klasy substancji, które są zawsze badane razem pod względem podobieństwa struktury i przejawianych właściwości. Są to aldehydy i ketony. To właśnie te cząsteczki leżą u podstaw wielu syntez chemicznych, a ich struktura jest na tyle interesująca, że można je badać. Rozważmy bardziej szczegółowo, jakie są te klasy związków.

Aldehydy i ketony: charakterystyka ogólna
Z punktu widzenia chemii, klasa aldehydów powinna zawierać cząsteczki organiczne zawierające tlen w grupie funkcyjnej -NH, zwanej karbonyl. Ogólna formuła w tym przypadku będzie wyglądać tak: R-COH. Ze swej natury mogą to być zarówno związki ograniczające, jak i nienasycone. Również wśród nich są przedstawiciele aromatyczni, a także alifatyczni. Liczba atomów węgla w łańcuchu rodnikowym zmienia się w dość szerokich granicach, od jednego (formaldehyd lub metan) do kilkudziesięciu.
Ad
Ketony zawierają także grupę karbonylową -CO, ale nie jest ona związana z kationem wodoru, ale z innym rodnikiem, który jest inny lub identyczny z tym, który wchodzi w łańcuch. Ogólny wzór jest następujący: R-CO-R ,. Oczywiste jest, że aldehydy i ketony są podobne w obecności grupy funkcyjnej tej kompozycji.
Ketony mogą również ograniczać i nienasycone, a przejawione właściwości są podobne do blisko spokrewnionych klas. Istnieje kilka przykładów ilustrujących skład cząsteczek i odzwierciedlających przyjęte oznaczenia wzorów substancji, o których mowa.
- Aldehydy: metanal - HCl, butanal - CH3-CH 2 -CH 2- COH, fenylooctowy - C 6H 5 -CH 2- COH.
- Ketony: aceton lub keton dimetylowy - CH 3 -CO-CH 3 , keton metylowo-etylowy - CH3-CO-C 2 H 5 i inne.
Jest oczywiste, że nazwa tych związków powstaje na dwa sposoby:
Ad
- zgodnie z racjonalną nomenklaturą według rodników i sufiksu klasy -al (dla aldehydów) i -onu (dla ketonów);
- trywialnie, historycznie.
Jeśli podasz ogólny wzór dla obu klas substancji, stanie się jasne, że są one swoimi izomerami: Cn H 2n O. Dla siebie charakterystyczne są następujące typy izomerii:
- dla ketonów, struktura łańcucha węglowodorowego rodnika i pozycja grupy -CO;
- dla aldehydów - tylko układ atomów w łańcuchu.

Aby odróżnić przedstawicieli obu klas, użyj reakcje jakościowe z których większość pozwala nam zidentyfikować aldehyd. Ponieważ aktywność chemiczna tych substancji jest nieco wyższa, ze względu na obecność kationów wodoru.
Struktura molekularna
Zastanów się, jak wyglądają aldehydy i ketony w kosmosie. Struktura ich cząsteczek może być odzwierciedlona w kilku punktach.
- Atom węgla bezpośrednio zawarty w grupie funkcyjnej ma hybrydyzację sp2, która pozwala części cząsteczki mieć płaski kształt przestrzenny.
- W takim przypadku polaryzacja wiązania C = O jest silna. Jako bardziej elektroujemny, tlen przyjmuje większość swojej gęstości, koncentrując częściowo ujemny ładunek na sobie.
- W aldehydach wiązanie OH jest również wysoce spolaryzowane, co sprawia, że atom wodoru jest mobilny.
W rezultacie okazuje się, że taka struktura cząsteczek pozwala na utlenianie i zmniejszanie tych związków. Formuła aldehydu i ketonu o redystrybucji gęstości elektronowej pozwala przewidzieć produkty reakcji, w których te substancje uczestniczą.
Ad
Historia odkryć i studiów
Jak wielu związki organiczne dopiero w XIX wieku ludzie zdołali wyizolować i zbadać aldehydy i ketony, gdy witalistyczne poglądy całkowicie się zawaliły i stało się jasne, że związki te można formować syntetycznymi, sztucznymi środkami, bez udziału żywych istot.
Jednak w 1661 R. Boyle udało się uzyskać aceton (keton dimetylowy), gdy poddawał octan wapnia do ogrzewania. Nie mógł jednak szczegółowo badać tej substancji i nazwać jej, określając systematyczną pozycję między innymi. Dopiero w 1852 r. Williamson zdołał doprowadzić tę sprawę do końca, a następnie rozpoczęła się historia szczegółowego rozwoju i akumulacji wiedzy o związkach karbonylowych.

Właściwości fizyczne
Rozważ fizyczne właściwości aldehydów i ketonów. Zacznijmy od pierwszego.
- Zgodnie ze stanem skupienia, pierwszym przedstawicielem jest metan, następne jedenaście to ciecze, ponad 12 atomów węgla jest częścią stałych aldehydów o normalnej strukturze.
- Temperatura wrzenia: zależy od liczby atomów węgla, im więcej, tym jest wyższa. Co więcej, im bardziej rozgałęziony łańcuch, tym niższa wartość temperatury.
- W przypadku ciekłych aldehydów, wskaźniki lepkości, gęstości i współczynnika refrakcji również zależą od liczby atomów. Im więcej z nich, więc są wyższe.
- Aldehydy gazowe i ciekłe bardzo dobrze rozpuszczają się w wodzie, jednak ciał stałych praktycznie nie można tego zrobić.
- Zapach przedstawicieli jest bardzo przyjemny, często jest to zapach kwiatów, perfum, owoców. Tylko te aldehydy, w których liczba atomów węgla wynosi 1-5, są silnie i nieprzyjemnie pachnącymi cieczami.
Jeśli wyznaczysz właściwości ketonów, możesz również wybrać te główne.
Ad
- Stany zagregowane: niższymi przedstawicielami są ciecze, a masywniejsze są związkami stałymi.
- Zapach jest ostry, nieprzyjemny dla wszystkich przedstawicieli.
- Rozpuszczalność w wodzie jest dobra dla dolnych, jest doskonała dla wszystkich w rozpuszczalnikach organicznych.
- Substancje lotne, wskaźnik ten przewyższa kwasy, alkohole.
- Temperatura wrzenia i temperatura topnienia zależy od struktury cząsteczki, różni się znacznie od liczby atomów węgla w łańcuchu.
Są to główne właściwości rozważanych związków, które należą do grupy fizycznej.
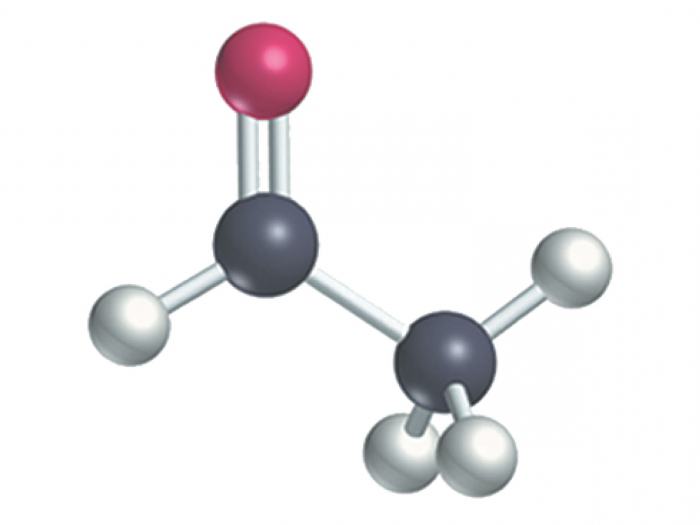
Właściwości chemiczne
Najważniejsze jest to, z czym reagują aldehydy i ketony, właściwości chemiczne tych związków. Dlatego uważamy je za koniecznie. Najpierw zajmij się aldehydami.
- Utlenianie do odpowiednich kwasów karboksylowych. Ogólny pogląd na równanie reakcji: R-COH + [O] = R-COOH. Aromatyczni przedstawiciele jeszcze łatwiej wchodzą w tego typu interakcje, a także mogą tworzyć estry o znaczeniu przemysłowym. Jako środki utleniające stosowane są: tlen, odczynnik Tollensa, wodorotlenek miedzi (II) i inne.
- Aldehydy przejawiają się jako silne środki redukujące, a jednocześnie przekształcają się w monotlenowe alkohole.
- Interakcje z alkoholami w celu wytworzenia produktów zawierających acetale i półacetale.
- Reakcje specjalne - polikondensacja. W wyniku tego powstają żywice fenolowo-formaldehydowe, które są ważne dla przemysłu chemicznego.
- Kilka specyficznych reakcji z następującymi odczynnikami:
- alkalia alkoholowe;
- Odczynnik Grignarda;
- hydrosulfity i inne.
Jakościową reakcją na tę klasę substancji jest reakcja "srebrnego lustra". W wyniku tego powstaje metaliczne zredukowane srebro i odpowiedni kwas karboksylowy. Wymaga roztworu amoniaku tlenku srebra lub odczynnika Tollinsa.
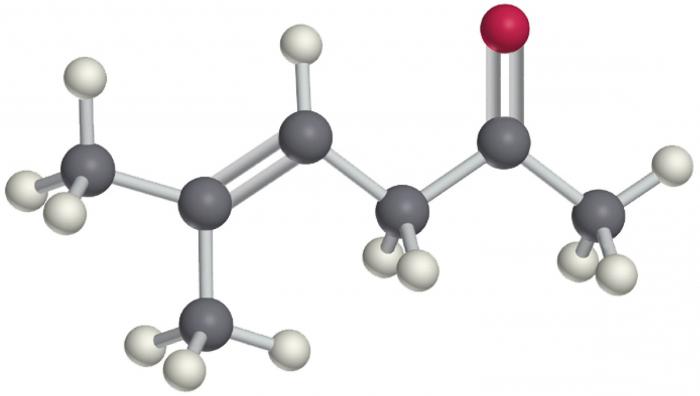
Właściwości chemiczne ketonów
Alkohole, aldehydy, ketony są podobne pod względem właściwości związków, ponieważ wszystkie zawierają tlen. Jednak już na etapie utleniania staje się jasne, że alkohole są najbardziej aktywnymi i łatwo podatnymi związkami. Ketony są najtrudniejsze do utlenienia.
Ad
- Właściwości utleniające. W wyniku tego powstają drugorzędowe alkohole.
- Uwodornienie prowadzi również do produktów wymienionych powyżej.
- Tautomeria keto-enolowa jest szczególną właściwością ketonów do przyjmowania postaci beta.
- Reakcje kondensacji aldolowej z tworzeniem beta-ketospirtov.
- Ponadto ketony mogą wchodzić w interakcję z:
- amoniak;
- kwas cyjanowodorowy ;
- wodorosiarczyn;
- hydrazyna;
- kwas ortokrzemowy.
Oczywiście reakcje takich interakcji są bardzo złożone, szczególnie te, które są specyficzne. Są to wszystkie główne cechy, które wykazują aldehydy i ketony. Właściwości chemiczne leżą u podstaw wielu syntez ważnych związków. Dlatego znajomość natury cząsteczek i ich charakteru podczas interakcji jest niezwykle potrzebna w procesach przemysłowych.
Reakcje addycji aldehydu i ketonu
Dokonaliśmy już przeglądu tych reakcji, ale nie nadaliśmy im takiego imienia. Wszystkie interakcje można przypisać dodaniu, w wyniku czego grupa karbonylowa wykazuje aktywność. A raczej mobilny atom wodoru. Dlatego w tym przypadku priorytetem są aldehydy, ze względu na ich lepszą reaktywność.
Jakie substancje są możliwymi reakcjami aldehydów i ketonów na podstawienie nukleofilowe? To jest:
- Powstaje kwas cyjanowodorowy, cyjanowce - surowiec do syntezy aminokwasów.
- Amoniak, aminy.
- Alkohole.
- Woda
- Wodorosiarczan sodu.
- Odczynnik Grignarda.
- Tiole i inne.
Reakcje te mają wielkie znaczenie przemysłowe, ponieważ produkty są wykorzystywane w różnych obszarach ludzkiej działalności.

Sposoby na zdobycie
Istnieje kilka podstawowych metod syntezy aldehydów i ketonów. Poruszanie się w laboratorium i przemyśle można wyrazić na następujące sposoby.
- Najpopularniejszą metodą, w tym w laboratoriach, jest utlenianie odpowiednich alkoholi: pierwszorzędowych do aldehydowych, wtórnie do przedstawicieli ketonów. Chromiany, jony miedzi, nadmanganian potasu mogą działać jako środek utleniający. Ogólny widok reakcji: R-OH + Cu (KMnO 4 ) = R-COH.
- W przemyśle często stosuje się metodę opartą na utlenianiu alkenów - oksosyntezę. Głównym czynnikiem jest gaz syntezowy, mieszanina CO 2 + H2. Wynikiem tego jest aldehyd o dużej liczbie atomów na węgiel łańcucha. R = RR + CO 2 + H 2 = RRR-COH.
- Utlenianie alkenów przez ozon - ozonoliza. Wynik sugeruje również obecność aldehydu, ale poza tym keton znajduje się również w mieszaninie. Jeśli produkty są połączone mentalnie, usuwając tlen, staje się jasne, co zostało zrobione oryginalnym alkenem.
- Reakcja Kuchevova - hydratacja alkinów. Obowiązkowe środki - sole rtęci. Jedna z przemysłowych metod syntezy aldehydów i ketonów. R≡RR + Hg 2+ + H20 = RR-COH.
- Hydroliza dihalogenowych pochodnych węglowodorów.
- Redukcja kwasów karboksylowych, amidów, nitryli, chlorków kwasowych, estrów. W wyniku tego powstają zarówno aldehyd, jak i keton.
- Piroliza mieszanin kwasów karboksylowych z katalizatorami tlenków metali. Mieszaninę należy odparować. Najważniejsze jest wyeliminowanie cząsteczek dwutlenku węgla i wody. Wynikiem jest aldehyd lub keton.
Aromatyczne aldehydy i ketony wytwarza się innymi sposobami, ponieważ związki te mają rodnik aromatyczny (na przykład fenyl).
- Według Friedela-Craftsa: w wyjściowych odczynnikach występuje aromatyczny węglowodór i keton o podstawionym dihalogenem. Katalizator - ALCL 3 . Wynikiem jest aromatyczny aldehyd lub keton. Inną nazwą tego procesu jest acylacja.
- Utlenianie toluenu różnymi środkami.
- Odzyskiwanie aromatycznych kwasów karboksylowych.
Oczywiście przemysł stara się stosować te metody, w których surowce są tak tanie, jak to możliwe, a katalizatory są mniej toksyczne. Do syntezy aldehydów należy utlenianie alkenów za pomocą tlenu.

Zastosowania przemysłowe i znaczenie
Zastosowanie aldehydów i ketonów odbywa się w takich branżach jak:
- farmaceutyki;
- synteza chemiczna;
- medycyna;
- powierzchnia perfumeryjna;
- przemysł spożywczy;
- produkcja farb i lakierów;
- synteza tworzyw sztucznych, tkanin i nie tylko.
Możesz wyznaczyć więcej niż jeden obszar, ponieważ rocznie tylko synteza formaldehydu wynosi około 6 milionów ton rocznie! Jego 40% roztwór nazywa się formaliną i służy do przechowywania obiektów anatomicznych. Zajmuje się także produkcją leków, środków antyseptycznych i polimerów.
Aldehyd octowy, lub etanal, także produkt wytwarzany masowo. Ilość rocznego zużycia na świecie wynosi około 4 milionów ton, co jest podstawą wielu syntez chemicznych, w których powstają ważne produkty. Na przykład:
- kwas octowy i jego bezwodnik;
- octan celulozy;
- leki;
- butadien - podstawa kauczuku;
- alkohol etylowy ;
- włókno octanowe.
Aromatyczne aldehydy i ketony są integralną częścią wielu smaków, zarówno żywności, jak i perfum. Większość z nich ma bardzo przyjemne kwiatowe, cytrusowe, ziołowe aromaty. To pozwala na produkcję na ich podstawie:
- odświeżacze powietrza różnego rodzaju;
- woda toaletowa i perfumowana;
- różne środki czyszczące i detergenty.
Niektóre z nich to aromatyzowane dodatki do żywności dopuszczone do spożycia. Ich naturalna zawartość w olejkach, owocach i żywicach świadczy o możliwości takiego wykorzystania.
Poszczególni przedstawiciele
Taki aldehyd, jak cytral, jest cieczą o wysokiej lepkości i silnym aromacie cytryny. W naturze zawarta jest w olejkach eterycznych tego ostatniego. Również w składzie eukaliptusa, sorgo, kebaba.
Znane obszary zastosowania:
- pediatrii - obniżenie ciśnienia wewnątrzczaszkowego;
- normalizacja ciśnienia krwi u dorosłych;
- składnik medycyny dla narządów wzroku;
- część wielu zapachów;
- przeciwzapalne i antyseptyczne;
- surowce do syntezy retinolu;
- aromat do celów spożywczych.