Aldehydy: właściwości chemiczne, przygotowanie, struktura
Praktycznie wszystkie chemikalia wokół nas są testowane przez ludzi w oparciu o ich potrzeby i wymagania. Każdy związek ma unikalny, nieodłączny zestaw cech i właściwości, z których wybiera się przydatne i niezbędne nam w życiu codziennym. Omawiane aldehydy również nie stanowią wyjątku.
Skromne dziecko chemii organicznej
Wśród związków węgla, które nazywane są organicznymi, są znane, które, jak mówią, są "powszechnie znane". Na przykład glukoza, alkohol etylowy lub tworzywa sztuczne. Aldehydy w tym sensie nie mają szczęścia. O nich wiadomo tylko wąskim specjalistom, a nawet licealistom, którzy ciężko pracują nad studiowaniem chemii na studia. W rzeczywistości takie związki (takie jak aldehyd octowy) którego właściwości chemiczne uważamy, jest szeroko stosowane zarówno w produkcji przemysłowej, jak iw życiu codziennym.
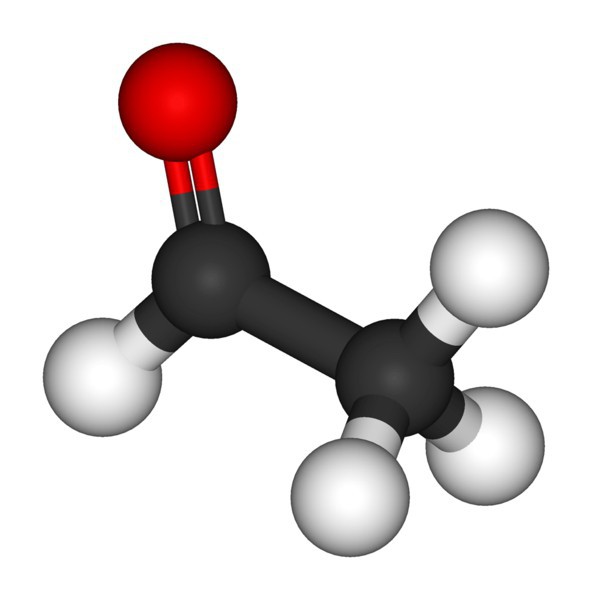
Apple of contention
Niestety, ale odkrycia w nauce dość często nie występują różowo. Aldehydy, ich struktura chemiczna i właściwości zostały odkryte w wyniku długich sporów i dyskusji wśród XIX-wiecznych naukowców. A tacy znani chemicy, jak Liebig i Döbereiner, nawet trochę żartowali, zastanawiając się, kto faktycznie posiada palmę w pozyskiwaniu i izolowaniu aldehydu octowego w czystej postaci. Wyekstrahowano go z par etanolu przepuszczonego przez sito platynowe, które służyło jako katalizator reakcji. Jedyną rzeczą, która mogła pogodzić przeciwników, była bezwarunkowa akceptacja przez wszystkich chemików nazwy nowej klasy substancji - aldehydów, co dosłownie oznacza "wolne od wodoru alkohole". Wskazuje metodę otrzymywania ich z alkoholi poprzez eliminację dwóch atomów wodoru.

Nie będziesz się mylić z niczym
Biorąc pod uwagę fizyczne i chemiczne właściwości aldehydów, łatwo jest upewnić się, że są one wystarczająco specyficzne. Tak więc, formaldehyd, który jest toksycznym gazem, ma ostry, duszący zapach. Jego 40% wodny roztwór, zwany formaliną, powoduje specyficzny zapach w anatomicznych laboratoriach i kostnicach, gdzie jest stosowany jako środek przeciwgrzybiczny, zachowujący białka narządów i tkanek.

Aldehyd octowy, który jest następny w serii homologicznej, jest bezbarwną cieczą łatwo rozpuszczalną w wodzie z nieprzyjemnym zapachem zgniłych jabłek. Aldehydy, właściwości chemiczne charakteryzujące się reakcjami utleniania i addycji, można przekształcić w substancje o genetycznie powiązanych klasach: kwasy karboksylowe lub alkohole. Rozważmy je za pomocą konkretnych przykładów.
Aldehyde Business Card
W chemii organicznej, podobnie jak w nieorganicznej, istnieje coś takiego jak "reakcja jakościowa". Można go porównać z latarnią morską, sygnalizując, że mamy do czynienia właśnie z substancjami określonej klasy, na przykład z aldehydami. Potwierdzają chemiczne właściwości aldehydów poprzez reakcję z roztworem amoniaku tlenku srebra i wodorotlenkiem miedzi po podgrzaniu (reakcja srebra w lustrze)
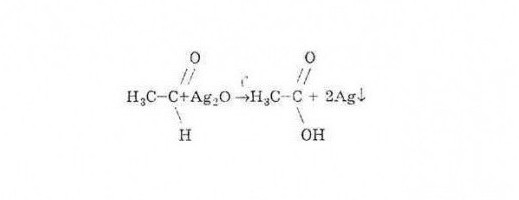
Produktem reakcji będzie czyste srebro uwalniane w postaci warstwy lustrzanej na ściankach rury.
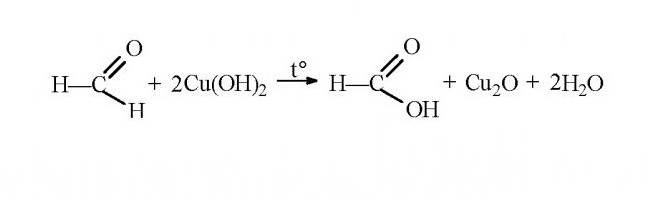
W rezultacie reakcja wytrąca ceglany tlenek miedzi.
Substancje podwójne
Nadszedł czas, aby uporać się z takim zjawiskiem, charakterystycznym dla wszystkich. materia organiczna w tym dla aldehydów, jako izomeria. Jest całkowicie nieobecny w świecie chemii nieorganicznej. Wszystko tam jest proste: tylko jeden określony związek o nieodłącznych właściwościach fizycznych i chemicznych odpowiada jednej formule chemicznej. Na przykład, wzór HNO 3 odpowiada jednej substancji, zwanej kwasem azotowym, o temperaturze wrzenia 86 ° C, o ostrym zapachu, bardzo higroskopijny.
W dziedzinie chemii organicznej izomery żyją - żyją, w których formuły są takie same, a właściwości są różne. Na przykład, wzór C4H8O ma dwa całkowicie różne aldehydy: butanal i 2-metylopropanal.
Ich formuły:
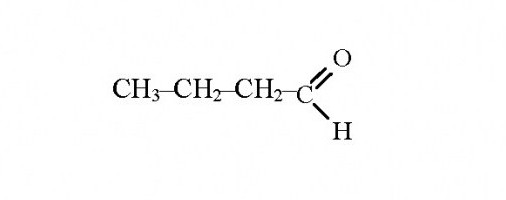
Izomeryczne aldehydy, których właściwości chemiczne zależą od ich składu i struktury, są doskonałym dowodem genialnej teorii budowy związków organicznych stworzonej przez rosyjskiego naukowca M. Butlerowa. Jego odkrycie ma takie samo fundamentalne znaczenie dla chemii jak okresowe prawo D Mendelejewa.
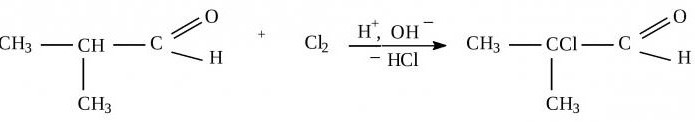
Unikalny węgiel
Doskonały dowód na teorię M. Butlerow służą chemiczne właściwości aldehydów. Chemia organiczna, dzięki badaniom rosyjskiego naukowca, była wreszcie w stanie odpowiedzieć na pytanie, które nękało więcej niż jedno pokolenie naukowców swoją złożonością, a mianowicie: jak wytłumaczyć różnorodność związków organicznych, która zadziwia wyobraźnię, która jest oparta na zjawisku izomerii. Rozważmy strukturę cząsteczek dwóch izomerów aldehydowych: butanalu i 2-metylopropanalu o tym samym wzorze cząsteczkowym - C4H8O, ale o różnej strukturze, a zatem różniących się od siebie właściwościami fizycznymi i chemicznymi.
Zwróćmy uwagę na dwie najważniejsze cechy atomu węgla, które zostały wprowadzone jako postulaty do teorii M. Butlerova:
1. Węgiel w związki organiczne zawsze czterowartościowy.
2. Atomy węgla mogą łączyć się ze sobą i tworzyć różne konfiguracje przestrzenne: nierozgałęzione i rozgałęzione łańcuchy lub cykle.
Zgodnie z wartościowością, na nie nawleczone są atomy innych pierwiastków chemicznych: wodoru, tlenu, azotu, tworząc w ten sposób cały gigantyczny arsenał istniejących związków organicznych (i jest ich ponad 10 milionów), a ponadto stale wzrasta dzięki nowym substancjom uzyskanym w chemia syntezy organicznej.
Im bardziej biegun, tym lepiej
Kontynuując badania aldehydów, ich strukturę chemiczną i właściwości, będziemy zastanawiać się nad zjawiskiem polarności atomów tworzących cząsteczki aldehydów. Tak więc, atom węgla grupy aldehydowej w cząsteczce aldehydu octowego nabywa częściowy ładunek dodatni, a atom tlenu - częściowo ujemny. Powodem ich występowania jest: gęstość elektronowa wiązania π jest bardziej ruchliwa niż wiązanie σ.

W ogólnym wzorze aldehydów, gdzie R oznacza rodnik węglowodorowy związany z grupą aldehydową, częściowy ładunek ujemny tworzy się na atomie tlenu i częściowy ładunek dodatni na atomie węgla. Tak więc, grupa funkcyjna aldehydów staje się silnie spolaryzowana, co powoduje wysoką reaktywność tych substancji. Mówiąc prosto, im bardziej spolaryzowane atomy w cząsteczce substancji, tym lepiej i szybciej wchodzi reakcje chemiczne. Szybka zdolność utleniania atomu wodoru w grupie aldehydowej i reaktywność grupy karbonylowej zapewniają aldehydy o charakterystycznych reakcjach addycji i polimeryzacji.
Życie w plastikowym świecie
To aldehydy, których właściwości chemiczne wynikają ze zdolności do polikondensacji i reakcji polimeryzacji, stały się przodkami fenoplastów i aminoplastów - podstawowych materiałów współczesnego przemysłu polimerowego. Formaldehyd i acetaldehyd służą jako surowce dla swoich przedsiębiorstw. Tak więc żywice fenolowo-formaldehydowe są fenoplastami - najważniejszymi substytutami metali żelaznych i nieżelaznych. Formaldehyd otrzymuje się przez utlenianie metanu przez ogrzewanie go do 600 ° C w mieszaninie z powietrzem, a także utlenianie metanolu ogrzanego do 300 ° C na katalizatorze miedzianym. Tak więc, aldehydy, przygotowanie i właściwości chemiczne, które uważamy, są ważnym surowcem w reakcjach syntezy organicznej.

Wyciągaj wnioski
Jak widać, w historii aldehydów jest wystarczająco dużo niezbędnych i ważnych substancji, takich jak na przykład formaldehyd i aldehyd octowy, których właściwości chemiczne z powodzeniem wykorzystuje człowiek w różnych sferach jego życia.