Metale alkaliczne. Struktura, właściwości fizyczne i chemiczne, zastosowanie
Metale alkaliczne - nazwa zwyczajowa pierwiastków z 1. grupy układu okresowego pierwiastków chemicznych. Jego skład: lit (Li), sód (Na), potas (K), rubid (Rb), cez (Cs), francium (Fr), i hipotetyczny element - ununenium (Uue). Nazwa grupy pochodzi od nazwy rozpuszczalnych wodorotlenków sodu i potasu, które mają reakcję alkaliczną i smak. Rozważ ogólne cechy strukturalne atomów pierwiastków, właściwości, produkcję i zastosowanie prostych substancji.
Nieaktualna i nowa numeracja grup
Zgodnie z przestarzałym systemem numerowania, metale alkaliczne zajmujące skrajnie lewą pionową kolumnę układu okresowego należą do grupy IA. W 1989 r. Międzynarodowa Unia Chemiczna (IUPAC) zaproponowała inną opcję (długoterminową) jako główną. Metale alkaliczne zgodnie z nową klasyfikacją i ciągłą numeracją należą do pierwszej grupy. Reprezentant II okresu - lit - otwiera to kruszywo, uzupełnia swój pierwiastek radioaktywny w 7. okresie - Francja. Wszystkie metale pierwszej grupy w zewnętrznej powłoce atomów zawierają jeden s-elektron, który łatwo oddają (zostają przywrócone).
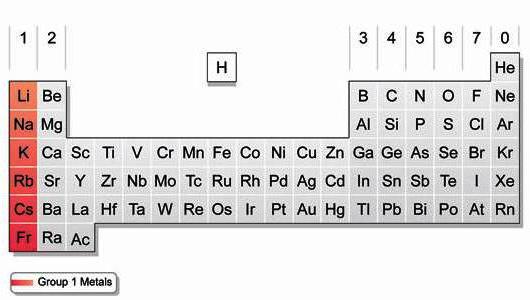
Struktura atomów metali alkalicznych
Pierwiastki z pierwszej grupy charakteryzują się obecnością drugiego poziomu energetycznego, powtarzającego strukturę poprzedniego gazu obojętnego. Lit zawiera 2 elektrony w ostatniej warstwie, a 8 elektronów w pozostałych. W reakcjach chemicznych atomy łatwo oddają zewnętrzny s-elektron, uzyskując energetycznie korzystną konfigurację gazu szlachetnego. Elementy pierwszej grupy mają małe wartości energii jonizacji i elektroujemności (EO). Z łatwością tworzą one pojedyncze naładowane jony dodatnie. Podczas przejścia z litu na Francję wzrasta liczba protonów i elektronów, promień atomu. Rubid, cez i francium łatwiej przekazują elektrony zewnętrzne niż pierwiastki, które je poprzedzają. Dlatego w grupie od góry do dołu zmniejsza się zdolność redukcji.
Zawartość w skorupie
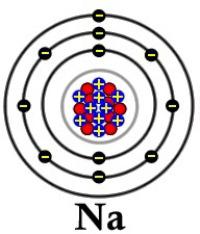 Łatwość utleniania metali alkalicznych prowadzi do tego, że pierwiastki z 1. grupy występują w przyrodzie w postaci związków ich pojedynczo naładowanych kationów. Zawartość w skorupie ziemskiej sodu - 2,0%, potasu - 1,1%. Pozostałe elementy są w małych ilościach, na przykład akcje Francji - 340 g. Chlorek sodu rozpuszczone w wodzie morskiej, solance jezior solnych i ujściach rzek, tworzy złoża kamienia lub sól. Razem z halitem znaleziono sylwinit NaCl • KCl i sylvin KCl. Skaleń utworzone przez glinokrzemian potasu K 2 [Al 2 Si 6 O 16 ]. W wodzie wielu jezior rozpuścił się węglan sodu a zasoby siarczanu pierwiastka są skoncentrowane na Morzu Kaspijskim (Kara-Bogaz-Gol). Są depozyty azotan sodu w Chile (chilijski saletra). Istnieje ograniczona liczba naturalnych związków litu. Rubid i cez są uznawane za zanieczyszczenia dla pierwiastków z pierwszej grupy pierwiastków, a francium w składzie rud uranu.
Łatwość utleniania metali alkalicznych prowadzi do tego, że pierwiastki z 1. grupy występują w przyrodzie w postaci związków ich pojedynczo naładowanych kationów. Zawartość w skorupie ziemskiej sodu - 2,0%, potasu - 1,1%. Pozostałe elementy są w małych ilościach, na przykład akcje Francji - 340 g. Chlorek sodu rozpuszczone w wodzie morskiej, solance jezior solnych i ujściach rzek, tworzy złoża kamienia lub sól. Razem z halitem znaleziono sylwinit NaCl • KCl i sylvin KCl. Skaleń utworzone przez glinokrzemian potasu K 2 [Al 2 Si 6 O 16 ]. W wodzie wielu jezior rozpuścił się węglan sodu a zasoby siarczanu pierwiastka są skoncentrowane na Morzu Kaspijskim (Kara-Bogaz-Gol). Są depozyty azotan sodu w Chile (chilijski saletra). Istnieje ograniczona liczba naturalnych związków litu. Rubid i cez są uznawane za zanieczyszczenia dla pierwiastków z pierwszej grupy pierwiastków, a francium w składzie rud uranu.
Sekwencja Alkali Metal Discovery
Brytyjski chemik i fizyk G. Devi w 1807 roku przeprowadził elektrolizę stopów metali alkalicznych, najpierw otrzymując sód i potas w postaci wolnej. W 1817 r. Szwedzki naukowiec Johann Arfvedson odkrył pierwiastek litowy w minerałach, aw 1825 r. G. Devi wyróżnił czysty metal. Rubidium po raz pierwszy odkrył w 1861 r. R. Bunsen i G. Kirchhoff. Niemieccy badacze analizowali skład glinokrzemianów i uzyskali w widmie czerwoną linię odpowiadającą nowemu pierwiastkowi. W 1939 r. Pracownik paryskiego instytutu radioaktywności Margarita Pere ustalił istnienie izotopu Francji. Określiła również żywioł na cześć swojej ojczyzny. Ununteenus (eka-francia) to tymczasowa nazwa nowego rodzaju atomu o numerze seryjnym 119. Symbol chemiczny Uue jest tymczasowo używany. Od 1985 roku badacze próbowali zsyntetyzować nowy element, który będzie pierwszym w ósmym okresie, siódmym w pierwszej grupie.
Właściwości fizyczne metali alkalicznych
 Prawie wszystkie metale alkaliczne mają srebrzystobiały kolor i metaliczny połysk na świeżym cięciu (cez ma złoty żółty kolor). Blask ściemnia się w powietrzu, pojawia się szary film, na licie jest zielonkawo-czarny. Metal ten ma najwyższą twardość wśród sąsiadów w grupie, ale jest gorszy od talku - najdelikatniejszego minerału, który otwiera skalę Mohsa. Sód i potas są łatwo zginane, mogą być cięte. Rubid, cez i francium w czystej postaci stanowią masę o konsystencji pasty. Topienie metali alkalicznych zachodzi w stosunkowo niskiej temperaturze. W przypadku litu osiąga on temperaturę 180,54 ° C. Sód topi się w 97,86 ° C, potas w 63,51 ° C, rubid w 39,32 ° C, cez przy 28,44 ° C. Gęstość metali alkalicznych jest mniejsza niż substancji pokrewnych. Płyną w nim także płyny litowe nafty, wznoszące się na powierzchnię wody, potasu i sodu.
Prawie wszystkie metale alkaliczne mają srebrzystobiały kolor i metaliczny połysk na świeżym cięciu (cez ma złoty żółty kolor). Blask ściemnia się w powietrzu, pojawia się szary film, na licie jest zielonkawo-czarny. Metal ten ma najwyższą twardość wśród sąsiadów w grupie, ale jest gorszy od talku - najdelikatniejszego minerału, który otwiera skalę Mohsa. Sód i potas są łatwo zginane, mogą być cięte. Rubid, cez i francium w czystej postaci stanowią masę o konsystencji pasty. Topienie metali alkalicznych zachodzi w stosunkowo niskiej temperaturze. W przypadku litu osiąga on temperaturę 180,54 ° C. Sód topi się w 97,86 ° C, potas w 63,51 ° C, rubid w 39,32 ° C, cez przy 28,44 ° C. Gęstość metali alkalicznych jest mniejsza niż substancji pokrewnych. Płyną w nim także płyny litowe nafty, wznoszące się na powierzchnię wody, potasu i sodu.
Stan krystaliczny
Krystalizacja metali alkalicznych zachodzi w sześciennym syngonie (skupionym na ciele). Atomy w swoim składzie mają pasmo przewodnictwa, do poziomów wolnych, z których mogą się przenieść elektrony. To te aktywne cząstki niosą specjalne wiązanie chemiczne - metaliczne. Wspólna struktura poziomów energetycznych i natura sieci krystalicznych wyjaśniają podobieństwo elementów pierwszej grupy. Podczas przejścia od litu do cezu zwiększają się masy atomów pierwiastków, co prowadzi do regularnego wzrostu gęstości, jak również do zmiany innych właściwości.
Właściwości chemiczne metali alkalicznych
Jedyny zewnętrzny elektron w atomach metali alkalicznych jest słabo przyciągany do jądra, więc mają niską energię jonizacji, ujemne lub zbliżone do zera powinowactwo elektronowe. Pierwiastki z pierwszej grupy, mające aktywność redukującą, praktycznie nie są zdolne do utleniania. W grupie odgórnej aktywność reakcji chemicznych wzrasta:
- Sód, potas i lit z lekkim światłem grzewczym w powietrzu. W przypadku dwóch pierwszych metali tworzenie się nadtlenków i nadtlenków w tej reakcji jest charakterystyczne, aw przypadku litu tlenek Li2O. Rubid i cez w powietrzu ulegają samozapaleniu.
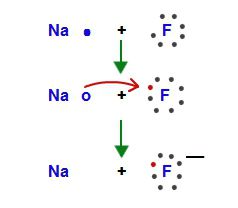 Metale alkaliczne mogą nawet redukować wodór. Po podgrzaniu oddziałuj z atomami najlżejszego pierwiastka i przywróć go do ujemnie naładowanego jonu H. W reakcji otrzymuje się wodorek, na przykład NaH, KH.
Metale alkaliczne mogą nawet redukować wodór. Po podgrzaniu oddziałuj z atomami najlżejszego pierwiastka i przywróć go do ujemnie naładowanego jonu H. W reakcji otrzymuje się wodorek, na przykład NaH, KH. - Proste substancje odpowiadające elementom pierwszej grupy wchodzą w interakcję z wodą i tworzą alkalia, na przykład LiOH, NaOH, KOH. Procesowi temu towarzyszy uwalnianie się wodoru w stanie gazowym, który sam się zapala lub eksploduje. 2Na + 2H20 = 2NaOH + H2 . Rubid i cez reagują nawet z lodem. Przechowywanie metali alkalicznych jest dozwolone pod warstwą oleju mineralnego, nafty, w zamkniętych szklanych naczyniach.
- Metale z pierwszej grupy aktywnie wchodzą w interakcję z halogenami, reakcja z fluorem i chlorem jest szczególnie silna, a po podgrzaniu - siarką i fosforem. Większość otrzymanych soli ma dobrą rozpuszczalność.
- Wysokiej jakości reakcja - rozkład soli metali alkalicznych w ogniu palnika gazowego. Pary barwią płomień w określonym kolorze.
- Gdy metale alkaliczne oddziałują z alkoholami, otrzymuje się alkoholany, z kwasami karboksylowymi dają one odpowiednie sole, na przykład mrówczan sodu.
Przygotowanie i stosowanie metali alkalicznych
Metale należące do pierwszej grupy są przemysłowo wytwarzane przez elektrolizę stopów ich halogenków i innych naturalnych związków. Po rozpadzie pod działaniem prądu elektrycznego jony dodatnie na katodzie przyłączają elektrony i są redukowane do wolnego metalu. Anion utlenia się na przeciwnej elektrodzie.
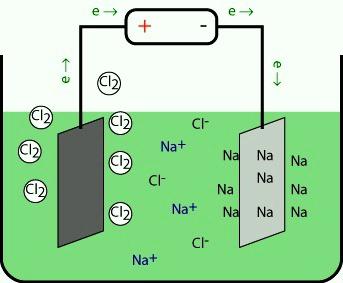
Podczas elektrolizy topników wodorotlenku na anodzie, cząsteczki OH- są utleniane, powstaje tlen i otrzymuje się wodę. Inną metodą jest termiczna redukcja metali alkalicznych ze stopionych soli wapniowych. Proste substancje i związki pierwiastków z 1. grupy mają znaczenie praktyczne. Lit jest wykorzystywany jako surowiec w energii atomowej, wykorzystywany w technologii rakietowej. W hutnictwie służy do usuwania resztkowego wodoru, azotu, tlenu i siarki. Wodorotlenek jest uzupełniany elektrolitem w bateriach alkalicznych.

Sód jest niezbędny dla energii jądrowej, metalurgii, syntezy organicznej. Cez i rubid są wykorzystywane do produkcji ogniw fotowoltaicznych. Często stosuje się wodorotlenki i sole, zwłaszcza chlorki, azotany, siarczany, węglany metali alkalicznych. Kationy mają aktywność biologiczną, jony sodu i potasu są szczególnie ważne dla organizmu człowieka.