Stała Boltzmanna: znaczenie i znaczenie fizyczne
Jako dokładna nauka ilościowa, fizyka nie może obejść się bez zestawu bardzo ważnych stałych, które są uwzględnione jako uniwersalne współczynniki w równaniach, które ustanawiają związek między tymi lub innymi wielkościami. Są to podstawowe stałe, dzięki którym takie relacje nabierają niezmienności i są w stanie wyjaśnić zachowanie systemów fizycznych w innej skali.
Wśród tych parametrów, które charakteryzują właściwości właściwe dla naszego Wszechświata, jest stała Boltzmanna, ilość zawarta w szeregu najważniejszych równań. Zanim jednak przejdziemy do rozważenia jego cech i znaczeń, nie sposób nie powiedzieć kilku słów o uczonym, którego nazwisko nosi.
Ludwig Boltzmann: wartość naukowa
Jeden z największych naukowców XIX wieku, austriacki Ludwig Boltzmann (1844-1906), wniósł istotny wkład w rozwój molekularnej teorii kinetyki, stając się jednym z założycieli mechaniki statystycznej. Był autorem hipotezy ergodycznej, metody statystycznej w opisie gazu idealnego, podstawowego równania fizykalnej kinetyki. Dużo pracował nad zagadnieniami termodynamiki (twierdzenie H-Boltzmanna, zasada statystyczna dla drugiej zasady termodynamiki), teorią promieniowania (prawo Stefana-Boltzmanna). W swoich pracach poruszał także zagadnienia elektrodynamiki, optyki i innych gałęzi fizyki. Jego imię zostało unieśmiertelnione na dwie fizyczne stałe, które zostaną omówione poniżej.
Ludwig Boltzmann był zagorzałym i konsekwentnym zwolennikiem teorii atomowo-molekularnej struktury materii. Przez lata zmuszony był zmagać się z brakiem zrozumienia i odrzucenia tych idei w społeczności naukowej w czasach, kiedy wielu fizyków uważało atomy i molekuły za niepotrzebną abstrakcję, w najlepszym przypadku, jako warunkowe urządzenie dla wygody obliczeń. Bolesna choroba i ataki konserwatywnych kolegów wywołały ciężką depresję u Boltzmanna, która nie mogła znieść wybitnego naukowca, który popełnił samobójstwo. Na pomniku nagrobnym, ponad popiersiem Boltzmanna, na znak uznania jego zasług, równanie S = k ∙ logW zostaje znokautowane - jedno z rezultatów jego owocnych naukowych działań. Stała k w tym równaniu jest stałą Boltzmanna.

Energia cząsteczki i temperatura substancji
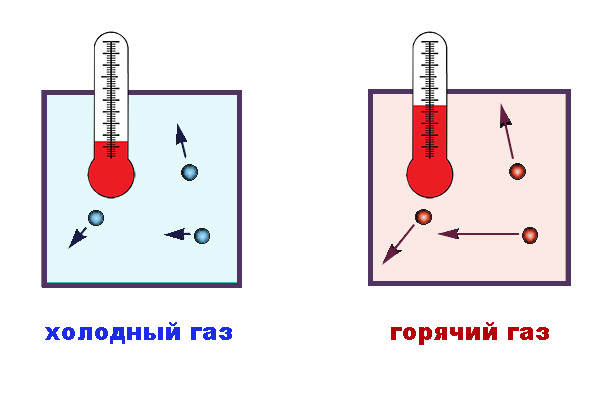
Pojęcie temperatury służy do scharakteryzowania stopnia ciepła ciała. W fizyce stosowana jest bezwzględna skala temperatury, w oparciu o wnioski z kinetycznej teorii temperatury cząsteczkowej jako miary odzwierciedlającej energię ruchu termicznego cząsteczek substancji (co oznacza, oczywiście, średnią energię kinetyczną wielu cząstek).
Zarówno dżul przyjęty w systemie SI, jak i erg stosowany w systemie GHS są zbyt dużymi jednostkami do wyrażania energii cząsteczek, a tak naprawdę bardzo trudno było zmierzyć temperaturę w ten sposób. Dogodną jednostką temperatury jest stopień, a pomiar odbywa się pośrednio, poprzez rejestrację zmieniających się właściwości makroskopowych substancji - na przykład objętość.

Jaka jest energia i temperatura
Aby obliczyć stany rzeczywistej substancji w temperaturach i ciśnieniach zbliżonych do normalnych, idealny model gazu jest z powodzeniem stosowany, to jest cząsteczka, której rozmiar jest znacznie mniejsza niż objętość zajmowana przez pewną ilość gazu, a odległość między cząstkami znacznie przekracza promień ich oddziaływania. W oparciu o równania teorii kinetycznej, średnia energia takich cząstek jest zdefiniowana jako E cf = 3/2 ∙ kT, gdzie E to energia kinetyczna, T to temperatura, a 3/2 ∙ k to współczynnik proporcjonalności wprowadzony przez Boltzmanna. Liczba 3 tutaj charakteryzuje liczbę stopni swobody ruchu translacyjnego cząsteczek w trzech wymiarach przestrzennych.
Wielkość k, nazwana później od austriackiego fizyka jako stała Boltzmanna, pokazuje, która część dżuli lub erga zawiera jeden stopień. Innymi słowy, jego wartość określa, jak statystycznie rośnie średnio energia termicznego ruchu chaotycznego pojedynczej cząstki monatomicznego gazu doskonałego, gdy temperatura wzrasta o 1 stopień.
Ile razy jest stopień mniej niż dżul
Wartość liczbową tej stałej można uzyskać na różne sposoby, na przykład mierząc absolutną temperaturę i ciśnienie, stosując równanie gazu idealnego lub stosując ruchomy model Browna. Teoretyczne wyprowadzenie tej ilości na obecnym poziomie wiedzy nie jest możliwe.
Stała Boltzmanna jest równa 1,38 × 10-23 J / K (tutaj K to Kelwin, stopień skali bezwzględnej temperatury). Dla zbiorników cząstek na 1 mol idealnego gazu (22,4 litra), współczynnik łączenia energii z temperaturą (uniwersalną stałą gazu) uzyskuje się przez pomnożenie stałej Boltzmanna przez liczbę Avogadro (liczba cząsteczek w molach): R = kN A , i wynosi 8.31 J / (mol ∙ Kelvin). Jednak w odróżnieniu od tego ostatniego, stała Boltzmanna ma bardziej uniwersalny charakter, ponieważ wchodzi również w inne ważne relacje, a także służy do zdefiniowania innej stałej fizycznej.
Statystyczny rozkład energii cząsteczek
Ponieważ stany materii o porządku makroskopowym są wynikiem zachowania się dużego zestawu cząstek, opisano je metodami statystycznymi. Ta ostatnia obejmuje ustalenie, w jaki sposób rozdzielane są parametry energetyczne cząsteczek gazu:
- Rozkład Maxwella energii kinetycznych (i prędkości). Pokazuje, że w stanie równowagi gazowej większość cząsteczek ma prędkość zbliżoną do pewnej najbardziej prawdopodobnej prędkości v = √ (2kT / m 0 ), gdzie m 0 jest masą cząsteczki.
- Rozkład potencjalnej energii Boltzmanna dla gazów znajdujących się w polu dowolnych sił, takich jak grawitacja Ziemi. Zależy od stosunku dwóch czynników: przyciągania do Ziemi i chaotycznego ruchu termicznego cząsteczek gazu. W rezultacie im niższa energia potencjalna cząsteczek (bliżej powierzchni planety), tym wyższa ich koncentracja.
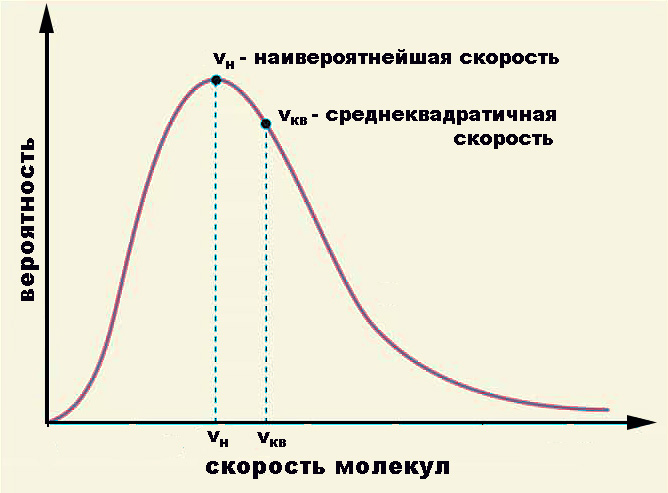
Obie metody statystyczne są połączone w rozkład Maxwella - Boltzmanna, który zawiera czynnik wykładniczy e - E / kT , gdzie E jest sumą energii kinetycznej i potencjalnej, a kT jest średnią energią ruchu termicznego już nam znaną, kontrolowaną przez stałą Boltzmanna.
Stała k i entropia
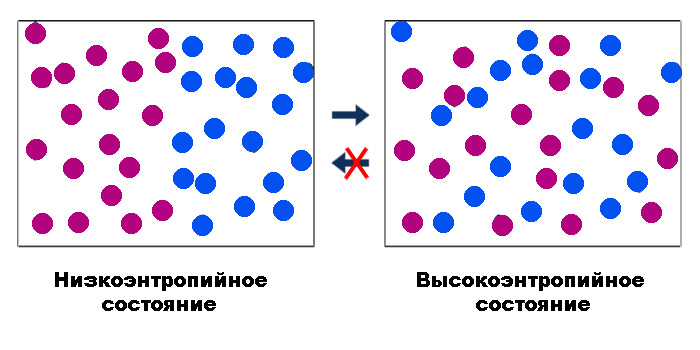
W sensie ogólnym entropię można scharakteryzować jako miarę nieodwracalności procesu termodynamicznego. Ta nieodwracalność wiąże się z rozpraszaniem - rozpraszaniem - energii. Zgodnie z podejściem statystycznym zaproponowanym przez Boltzmanna, entropia jest funkcją liczby sposobów, w jakie można wprowadzić system fizyczny bez zmiany jego stanu: S = k ∙ lnW.
Tutaj stała k wyznacza skalę wzrostu entropii wraz ze wzrostem tej liczby (W) wariantów układu lub mikrostanów. Max Planck, który poprowadził tę formułę do nowoczesnej formy i zaproponował, by nadać ciągowi k nazwisko Boltzmann.
Prawo promieniowania Stefana - Boltzmanna
Fizyczne prawo, które określa, w jaki sposób jasność energii (moc promieniowania na jednostkę powierzchni) absolutnie czarnego ciała zależy od jego temperatury, ma postać j = σT 4 , czyli ciało promieniuje proporcjonalnie do czwartej potęgi jego temperatury. Prawo to stosuje się na przykład w astrofizyce, ponieważ emisja gwiazd ma cechy charakterystyczne dla ciała czarnego.
Jest jeszcze jedna stała w tym stosunku, która również kontroluje skalę zjawiska. Jest to stała Stefana - Boltzmanna σ, która wynosi w przybliżeniu 5,67 × 10 -8 W / (m 2 K 4 ). Jego wymiar obejmuje Kelvin - oznacza to, że jest oczywiste, że bierze w tym udział również stała K Boltzmanna. Rzeczywiście, ilość σ jest zdefiniowana jako (2π 2 ∙ k 4 ) / (15c 2 h 3 ), gdzie c jest prędkością światła, a h jest stałą Plancka. Stała Boltzmanna, w połączeniu z innymi stałymi światowymi, tworzy pewną ilość, ponownie łącząc energię (moc) i temperaturę między nimi - w tym przypadku w odniesieniu do promieniowania.

Fizyczna esencja stałej Boltzmanna
Już wcześniej zauważono, że stała Boltzmanna jest jedną z tak zwanych stałych podstawowych. Chodzi nie tylko o to, że pozwala nam ustalić związek między cechami zjawisk mikroskopowych poziomu molekularnego a parametrami procesów obserwowanych w świecie makr. I nie tylko, że ta stała jest zawarta w wielu ważnych równaniach.
Obecnie nie wiadomo, czy istnieje jakakolwiek zasada fizyczna, na podstawie której można ją uzyskać teoretycznie. Innymi słowy, nie wynika z niczego, że wartość danej stałej powinna być właśnie taka. Moglibyśmy użyć innych wartości i innych jednostek zamiast stopni jako miary zgodności energii kinetycznej cząstek, wtedy wartość liczbowa stałej byłaby inna, ale pozostałaby wartością stałą. Wraz z innymi fundamentalnymi wartościami tego rodzaju - prędkość graniczna c, stała Plancka h, ładunek elementarny e, stała grawitacyjna G - nauka przyjmuje stałą Boltzmanna jako daną z naszego świata i wykorzystuje do teoretycznego opisu zachodzących w niej procesów fizycznych.