Właściwości chemiczne kwasów karboksylowych i metody ich otrzymywania
Związki chemiczne, które składają się w szczególności z grupy karboksylowej COOH, otrzymały od naukowców nazwy kwasów karboksylowych. Istnieje wiele nazw tych związków. Są one klasyfikowane według różnych parametrów, na przykład liczby grup funkcyjnych, obecności pierścienia aromatycznego i tak dalej.
Struktura kwasów karboksylowych
Jak już wspomniano, aby kwas był karboksylowy, musi on zawierać grupę karboksylową, która z kolei ma dwie części funkcyjne: hydroksyl i karbonyl. Ich wzajemne oddziaływanie zapewnia funkcjonalna kombinacja jednego atomu węgla z dwoma atomami tlenu. Właściwości chemiczne kwasów karboksylowych zależą od struktury tej grupy.
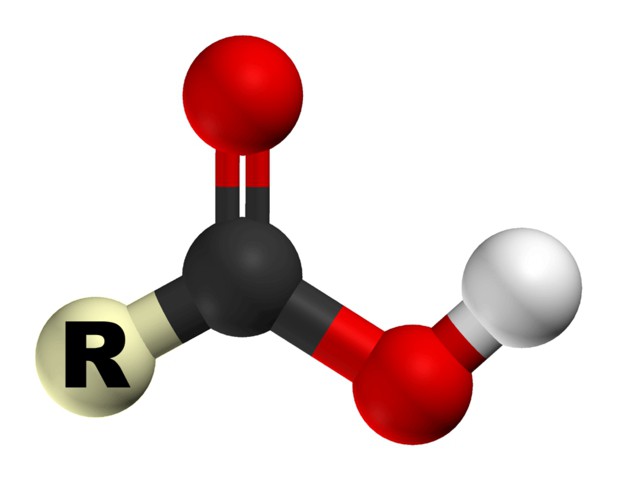
Ze względu na grupę karboksylową, te związki organiczne można nazwać kwasami. Ich właściwości wynikają ze zwiększonej zdolności przyciągania jonu H + do tlenu, co dodatkowo polaryzuje wiązanie OH. Również z powodu tej właściwości, kwasy organiczne są zdolne do dysocjacji w roztworach wodnych. Zdolność rozpuszczania spadków odwrotnie ze wzrostem masy cząsteczkowej kwasu.
Odmiany kwasów karboksylowych
Chemicy wydzielają kilka grup kwasów organicznych.
Klasyfikacja kwasów karboksylowych | |
Według liczby grup funkcyjnych | Monocarbon |
Diwęglan | |
Poliwęglan | |
Z natury radykalny | Alifatyczny |
Aromatyczny | |
Cykliczny | |
Według stopnia nasycenia rodnika | Nienasycony |
Nasycony | |
Przez obecność grup funkcyjnych w rodniku, to jest przez podstawienie jednego atomu wodoru | Halogen (Cl 2 , F 2 , Br 2 , I 2 ) |
Oxogroup (COH) | |
Hydroksy (OH) | |
Grupa aminowa (NH 2) | |
Monozasadowe kwasy karboksylowe składają się ze szkieletu węglowego i tylko jednej funkcjonalnej grupy karboksylowej. Każdy student zna chemiczne właściwości kwasów karboksylowych. Program 10 stopnia chemii obejmuje bezpośrednie badanie właściwości kwasów jednozasadowych. Kwasy dwuzasadowe i wielozasadowe mają odpowiednio dwie lub więcej grup karboksylowych.
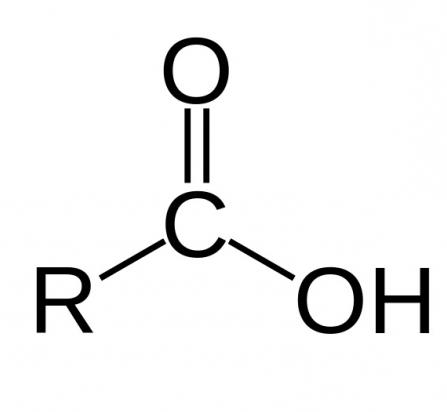
Również obecność lub brak podwójnych i potrójnych wiązań w cząsteczce zawiera nienasycone i nasycone kwasy karboksylowe. Właściwości chemiczne i ich różnice zostaną omówione poniżej.
Jeśli kwas organiczny ma podstawiony atom w rodniku, to jego nazwa zawiera nazwę grupy podstawników. Tak więc, jeśli atom wodoru zostanie zastąpiony przez halogen, wówczas nazwa kwasu będzie zawierała nazwę fluorowca. Te same zmiany ulegną zmianie, jeśli nastąpi substytucja grupami aldehydowymi, hydroksylowymi lub aminowymi.
Izomeria organicznego kwasu karboksylowego
Prawie wszystkie materia organiczna mieć zdolność do izomeryzacji. Kwasy karboksylowe nie są wyjątkiem. Wyróżnia się następujące typy izomerii:
- Szkielet węglowy.
- Izomeria międzyklasowa.
- Izomeria przestrzenna;
Zdolność do izomeryzacji wpływa bezpośrednio na właściwości chemiczne kwasów karboksylowych.
Izomeria szkieletu jest możliwa dla kwasów, których węglowodory zawierają co najmniej cztery atomy węgla. Interklasa z kolei jest możliwa dla kwasów z dwoma atomami węgla w rodniku. I tylko kwasy karboksylowe z pojedynczymi wiązaniami w szkielecie są zdolne do przestrzeni.
Lista i podstawowe kwasy karboksylowe
Nazwy i wzory znanych kwasów karboksylowych | ||
Systematyczna nazwa kwasu | Trzecie imię | Formuła kwasu karboksylowego |
Kwas metanowy | Ant | HCOOH |
Kwas etanowy | Acetic | CH 2 COOH |
Kwas propanowy | Propionowy | CH3CH2COOH |
Kwas butanowy | Oliwy | CH3CH2CH2COOH |
Kwas pentanowy | Walerian | CH3CH2CH2CH2COOH |
Kwas pentenowy | Akryl | CH2 = CH-COOH |
Benzen kwasu karboksylowego | Benzoin | C 6H 5 COOH |
Heksadekan | Palmitic | C 15H 31COOH |
Oksodekan | Stearic | C17H35COOH |
Ethandium | Szczaw | HOOC-COOH |
Propandia | Malonovaya | HOOC-CH 2- COOH |
Butandiova | Bursztynowy | HOOC-CH 2 -CH 2- COOH |
Benzen dikarboksylowy | Ftalowy | HOOC-C6H5-COOH |
Kwas 2-hydroksypropanowy | Nabiał | CH3 CHOHCOOH |
Kwas hydroksybutanodiowy | Apple | HOOC-CH2CHOH-COOH |
Kwas 2,3-dihydroksybutanodiowy | Winiarnia | HOOC-OHCH-OHCH-COOH |
3-karboksy-3-hydroksypentanedium | Lemon | HOOC-CH2-CHOH-COOH-CH 2COOH |
Kwas 2-oksopropanowy | Pyruvic | CH 3 COCOOH |
Kwas 2-hydroksybenzoesowy | Salicylowy | C 6H 5 OHCOOH |
Kwasy karboksylowe: właściwości chemiczne
Dla bardziej szczegółowego zrozumienia istoty kwasów karboksylowych rozważ ich właściwości. W szkolnym programie nauczania, monozasadowe kwasy karboksylowe są rozpatrywane w dużej objętości, której właściwości chemiczne przejawiają się w reakcjach między halogenowodorkami, wodą i innymi substancjami. Cały ten rodzaj kwasu:
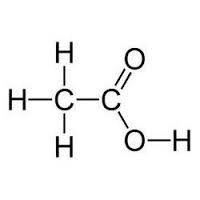
- Dysocjować w roztworze do jonów wodorowych i rodnika za pomocą karboksylu. Dzięki temu kwas mrówkowy odnosi się do elektrolitów o średniej sile i słabego kwasu octowego, to znaczy, że siła dysocjacji zmniejsza się w szeregu homologicznym.
- Pomaluj test lakmusowy na czerwono.
- Przeprowadź prąd elektryczności.
- Reaguje z halogenami: 2RCOOH + Cl2 = 2RCOOCl + 2HCL.
- Wchodzą one w reakcję estryfikacji z alkoholami: R-COOH + R'OH = RCOOR '+ H2O.
- Interakcja z niektórymi metalami: RCOOH + Mg = RCOOMg + H2.
- Reaguj z podstawowe tlenki rodzaj i wodorotlenki, sole tworzące: RCOOH + NaOH = RCOONa + H2O.
- Reaguj z solami: RCOOH + Na2CO3 = RCOONa + H2O + CO2.
Takie własności kwasów jednozasadowych wyjaśniono zmianą w grupie karboksylowej, z grupy hydroksylowej, z której elektrony przesuwają się do najbliższego atomu węgla, częściowo hartując jego ładunek dodatni. Ponadto kwasy karboksylowe, których właściwości chemiczne opisano powyżej, mają dwukierunkową interakcję między atomami.
Właściwości chemiczne pozostałych kwasów monozasadowych
Z klasyfikacji wiadomo, że występują również monozasadowe nienasycone kwasy karboksylowe, których właściwości chemiczne różnią się od właściwości granicy.
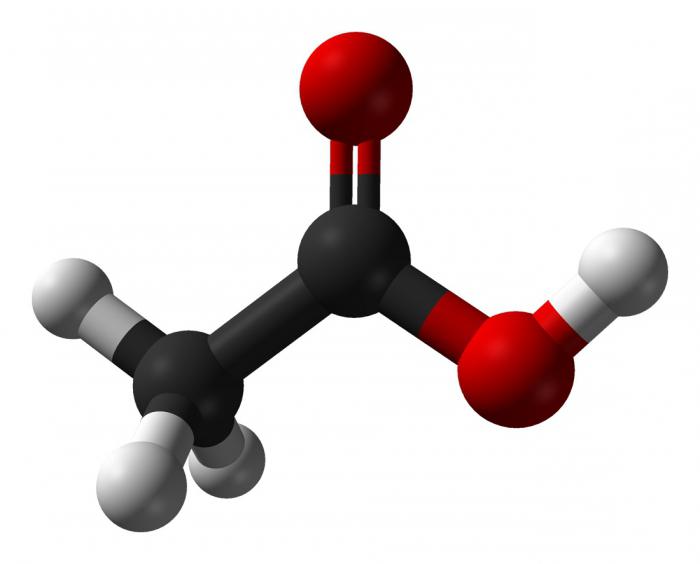
Tak więc, podwójne wiązania kwasów w rodniku węglowodorowym są jednozasadowymi nienasyconymi kwasami karboksylowymi. Właściwości chemiczne takich kwasów wyrażane są w reakcjach:
- Z halogenowodorem, ale znacznie wolniejszym niż ograniczenia i w przeciwieństwie do reguły Markowa, ponieważ grupa karboksylowa zmniejsza gęstość elektronową podwójnego wiązania: R = CH - COOH + HCl = RCl - CH2 - COOH.
- W przypadku halogenów: Br2 + R = CH-COOH = RBr-CHBr-COOH.
- Z wodorem, w wyniku którego pęka wiązanie podwójne: H2 + R = CH-COOH = COOH-R-CH.
- Ostrożne utlenianie, w wyniku którego powstają hydroksykwasy: R = CH-COOH + H2O [O] R (OH) -CH (OH) COOH.
- Radykalne utlenianie, które zachodzi wraz z rozerwaniem cząsteczki kwasu (na przykład, kwas propenowy): CH3-CH = C-COOH + H2O [O] CH3COOH + HOOC-COOH.
- Polimeryzacja: n COOH- (CH = CH) -R = n (-COOH-CH-CH-R-)
Właściwości chemiczne kwasów dwukarboksylowych
Dikarboksylowe kwasy organiczne są dwuzasadowymi kwasami karboksylowymi. Właściwości chemiczne takich kwasów różnią się od właściwości monokarboksylowych. Wynika to z faktu, że wytrzymałość kwasów dwuzasadowych jest większa niż wytrzymałość monozasadowa ze względu na wpływ drugiej grupy karboksylowej i hydroksylowej. Co więcej, efekt ten maleje wraz z odległością od łańcucha atomów węgla.
Kwasy dwuzasadowe wykazują następujące właściwości:
- Kwasowa dekarboksylacja (na przykład, etanedyna): HOOC-COOH (t) = HOOC + CO2. Ważne jest, aby wiedzieć, że kwasy szczawiowy i malonowy ulegają dekarboksylacji znacznie łatwiej niż inne.
- Tworzenie kwaśnych i średnich soli: HOOC-RR-COOK lub HOOK-RR-COOK.
- Tworzenie kompletnych i niekompletnych eterów.
- Kwas malonowy może wchodzić w reakcje podstawień: wodór z grupy CH2 rodnika węglowodorowego łatwo zastąpić atomami metali.
Sole utworzone przez kwasy karboksylowe
Sole to związki organiczne powstałe w wyniku zastąpienia atomu wodoru i hydroksylu grupy karboksylowej kwasu karboksylowego metalem. Oznacza to, że kwasy organiczne w reakcjach z zasadami lub solami nieorganicznymi mogą tworzyć sole kwasów karboksylowych. Właściwości chemiczne, dzięki którym otrzymuje się związki organiczne, takie jak sole, są wykorzystywane w przemyśle domowym do produkcji mydła.
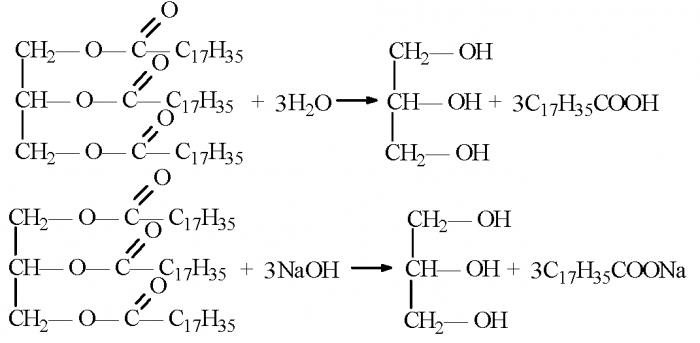
Kwasy stearynowy (oktadekanowy) i palmitynowy (heksadekanowy) są najbardziej odpowiednie do syntezy stałych i ciekłych mydeł. Olejek (cis-9-oktadekan) lub mirystynowy (tetradekan kwas).
Podstawą mydła jest reakcja syntezy estrów powyższych kwasów z solą potasową lub sodową.
Metody wytwarzania kwasów karboksylowych
Istnieje wiele metod i metod wytwarzania kwasów z grupą COOH, ale najczęściej stosuje się następujące:
- Ekstrakcja z naturalnych substancji (tłuszczów i innych rzeczy).
- Utlenianie monoalkoholi lub związków z grupą COH (aldehydami): ROH (RCOH) [O] R-COOH.
- Hydroliza trihaloalkanów w środowisku alkalicznym przy pośredniej produkcji monoalkoholu: RCl3 + NaOH = (ROH + 3NaCl) = RCOOH + H2O.
- Zmydlanie lub hydroliza estrów kwasu i alkoholu (estrów): R - COOR '+ NaOH = (R - COONa + R'OH) = R - COOH + NaCl.
- Utlenianie alkanów nadmanganianem (twarde utlenianie): R = CH2 [O], (KMnO4) RCOOH.
Wartość kwasów karboksylowych dla ludzi i przemysłu

Właściwości chemiczne kwasów karboksylowych mają ogromne znaczenie dla życia człowieka. Są niezwykle niezbędne dla organizmu, tak jak w dużych ilościach zawartych w każdej komórce. Metabolizm tłuszczy, białek i węglowodanów zawsze przechodzi przez etap, w którym otrzymuje się jeden lub drugi kwas karboksylowy.
Ponadto kwasy karboksylowe są stosowane do wytwarzania leków. Żaden przemysł farmaceutyczny nie może istnieć bez praktycznego wykorzystania właściwości kwasów organicznych.

Ważną rolę odgrywają związki z grupą karboksylową w przemyśle kosmetycznym. Synteza tłuszczu do późniejszej produkcji mydła, detergentów i chemii gospodarczej opiera się na reakcji estryfikacji z kwasem karboksylowym.
Właściwości chemiczne kwasów karboksylowych znajdują odzwierciedlenie w życiu człowieka. Mają wielkie znaczenie dla ludzkiego ciała, ponieważ są zawarte w dużych ilościach w każdej komórce. Metabolizm tłuszczy, białek i węglowodanów zawsze przechodzi przez etap, w którym otrzymuje się jeden lub drugi kwas karboksylowy.