Układy koloidalne: rodzaje, właściwości i wartość
Jeśli chodzi o zagregowany stan substancji, zwykle rozróżnia się cztery główne typy:
- osocze;
- stały;
- płynny;
- gaz
Jednak większość biologicznych mediów, płynów i zjawisk naturalnych jest mieszaniną kilku wariantów. Znaczna część wszystkich rozwiązań ma specjalne właściwości. Różnią się one zarówno cechami zewnętrznymi, jak i strukturą wewnętrzną. Nazwijmy je w ten sposób: systemy koloidalne. Jest to skumulowana mieszanina substancji o różnym charakterze, które znajdują się w różnych stanach agregacji. Aby lepiej zrozumieć ten problem, powinieneś rozważyć wszystkie właściwości i cechy takich rozwiązań, które zrobimy w trakcie tego artykułu.
Układ koloidowo-dyspersyjny: charakterystyczny
Mówiąc prostym, codziennym językiem, system ten jest czymś pomiędzy prawdziwym rozwiązaniem, które jest w 100% homogenicznym medium i grubymi zawiesinami, w których linia rozdziału faz jest wyraźnie widoczna.
Ogólnie rzecz biorąc, systemy koloidalne są częścią systemów rozproszonych, jednej z ich odmian. Dlatego nie jest zaskakujące, że ich właściwości są pod wieloma względami podobne. Aby lepiej wyobrazić sobie opisany stan substancji, przytoczmy kilka przykładów z życia.
- Żele i żelowe korpusy. Na przykład te, które są używane do stylizacji włosów. Również tutaj można przypisać żel i żelatynowy krem, w tym słodycze. Roztwór agar-agar, spęczniona skrobia, roztwór białek kurzej są układami koloidalnymi. Chemia, która zajmuje się badaniem takich struktur, nazywa się fizyczną koloidalną lub fizyczną.
- Zoli Innymi słowy, są to zniszczone żele. To oni stoją na granicy systemów gruboziarnistych i prawdziwych rozwiązań. Przykłady tego stanu: mgła, dym lub kurz w powietrzu.
Możesz również podać kilka bardziej znanych związków, które są uważane za koloidy:
- pył;
- aerozol;
- emulsja;
- zawieszenie;
- mgła i inne.
Dla każdego podanego przykładu możesz przynieść swoje specyficzne właściwości. Są jednak te, które są dla nich wspólne.
Klasyfikacja układów koloidalnych
Ponieważ różnorodność rozważanych związków jest duża, naturalne jest, że istnieje ich klasyfikacja. Opiera się na oznakach struktury - strukturze, rozmiarze fazy rozproszonej w stosunku do środowiska i innych. Jeśli wszystkie układy koloidalne są podzielone na typy w zależności od rodzaju cząstek w nich, to można wyróżnić te główne:
- ciecz w gazie - mgła, na przykład;
- cząsteczki stałe w środowisku gazowym - dym, pył;
- płyn w cieczy - różne emulsje;
- stałe cząstki w cieczy - zawiesiny;
- ciecz w postaci stałej - emulsja;
- stałe cząstki w stałej pożywce - stałe zole.
Istnieje również inna cecha, która stanowi podstawę do oddzielenia rozpatrywanych systemów. Jest to wzajemne oddziaływanie cząstek fazy i medium. Klasyfikacja układów koloidalnych w tym przypadku przyjmuje następującą formę.
- Liofilny. Obejmują systemy, w których zachodzi interakcja, a nawet rozpuszczanie się cząstek fazowych w ośrodku.
- Lyophobic. Nie ma interakcji między medium a fazą, ani ich wzajemnego rozpadu.
Jeśli mówimy o środowisku takim jak woda, to te same grupy można nazwać odpowiednio hydrofilowymi i hydrofobowymi.
Inną opcją podziału rozważanych systemów jest:
- Swobodnie rozproszone. Są to te, w których cząsteczki są w ciągłym ruchu, wchodzą ze sobą w interakcje i nie tworzą specyficznej struktury, to jest w jakimś chaosie. Przykłady: drobne zawiesiny, emulsje, liosole, aerozole.
- Związane zdyspergowane układy koloidalne, w których struktura wewnętrzna jest uporządkowana i reprezentuje rodzaj szkieletu molekularnego z ośrodka wypełnionego fazą. Przykłady obejmują żele, pasty, proszki, gęste emulsje i zawiesiny.
Możliwe jest spontaniczne przejście zolu na żel, proces ten nazywa się żelowaniem. Często jednak obserwuje się odwrotny proces.
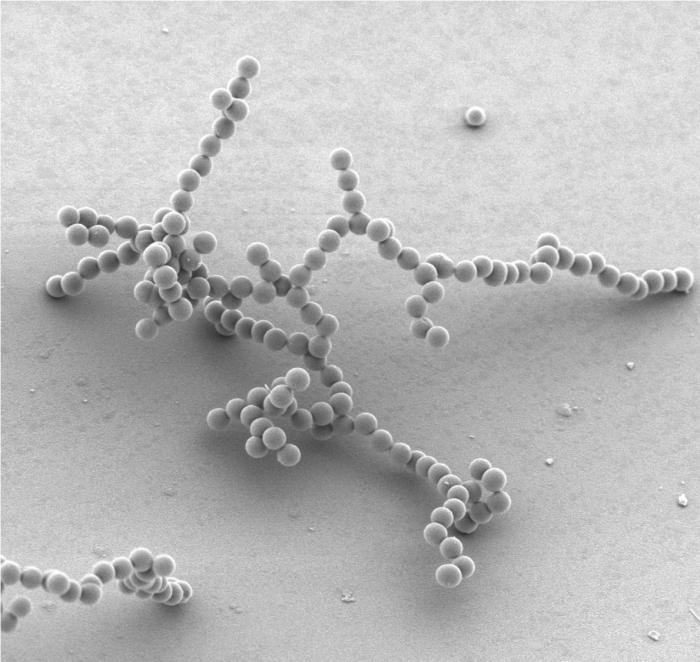
Systemy lofoficzne: sol
Jest to taki układ koloidalny, którego fazy są wyraźnie oddzielone od siebie przez interfejs. Jednak trudno to zobaczyć, ponieważ rozmiar zdyspergowanych cząstek wynosi nie więcej niż 100 nm. Dlatego zole są stanem pośrednim między prawdziwymi roztworami i grubymi zdyspergowanymi kompozycjami.
Systemy te mają własną klasyfikację. Są one rozdzielone w zależności od rodzaju ośrodka dyspersyjnego. Istnieje kilka głównych opcji:
- hydrosols - ośrodek wodny;
- alkohol - alkohol;
- eterosole - eteryczne;
- Organosole są bardziej ogólnym określeniem organicznej natury środowiska.
Właśnie dla liozoli (średnio - płynnych) charakterystyczna jest taka koncepcja, jak micele. Oznaczają one cząstki fazowe w połączeniu ze sferą zewnętrzną - cząstkami (jonami) środowiska. Dla każdego systemu popiołu możesz napisać swoją chemiczną ekspresję, odzwierciedlającą jej skład w postaci miceli.
Przykład: czerwony złoty zol o składzie NaAuO 2 + HCOH + Na2CO3 → Au + HCOONa + H 2 O ma micelę w następującej postaci: {[Au] m · n AuO 2 - · (nx) Na + } x- · xNa + .
Właściwości zoli można opisać kilkoma punktami:
- Istnieje granica faz, która ma silne napięcie powierzchniowe.
- Faza cząstek i medium są w stałym ruchu Browna.
- Cząsteczki są zdolne do agregacji - koalescencji i strącania. Wynika to z ich ciągłej interakcji.
Jeśli mówimy o użyciu zolu w przemyśle, to jest dość szeroki. Jeśli przypominamy, że wszystkie aerozole, zawiesiny i emulsje należą do nich specjalnie, to staje się jasne, że takie układy koloidalne nie są kompletne bez:
- przemysł chemiczny;
- farmaceutyki;
- działalność wojskowa;
- przemysł spożywczy i inne.
W pewnych warunkach zole mogą zacząć się układać. To znaczy, aby zbudować wewnętrzną strukturę zdyspergowanych cząstek, w których komórki będą wypełnione cząsteczkami o średniej wielkości. Inną nazwą tego, co się dzieje, jest koagulacja lub przyklejanie. W tym przypadku mówimy o żelowaniu, ponieważ produkt będzie żelem.

Systemy liofilowe
Struktury te powstają w wyniku bliskiego oddziaływania cząstek medium i fazy. Prowadzi to do tego, że rozpuszczają się one w sobie nawzajem, tworzą się pęczniejące i zżelowane żelopodobne związki. Wewnątrz stanowią trójwymiarową siatkę przestrzenną, w której wszystkie pory wypełnione są cząstkami ciekłego lub stałego ośrodka. Ze względu na tę strukturę wszystkie żele do zamrażania mają następujące właściwości:
- elastyczność;
- zdolność do utrzymywania stałej formy;
- siła;
- plastyczność;
- niepłynność
Takie koloidalne układy molekularne są bardzo powszechne. W końcu ze swej natury są to zarówno substancje wielkocząsteczkowe, jak i niskomolekularne, które są narażone na zmiany właściwości. Oto kilka dobrze znanych opcji:
- kosmetyczne żele do golenia do włosów;
- leki - na ból, siniaki, rany i inne;
- chemia gospodarcza;
- adsorbenty w przemyśle chemicznym.
Szczególną właściwością tych substancji jest zdolność do samorzutnego nieodwracalnego zapadnięcia się podczas suszenia. Z pewnością wielu ludzi zauważyło, że istnieje zwykły żel do włosów otwarty, a za dwa lub trzy dni pozostanie tylko mała sucha masa, która nie nadaje się do użytku.
Jest to spowodowane zniszczeniem struktury przestrzennej i odparowaniem wilgoci. Czasami wilgoć jest specjalnie usuwana z kompozycji żeli, aby uzyskać pożądany produkt. Ale robi się to chemicznie, bez niszczenia całej struktury. Więc zdobądź żele krzemionkowe, alumogeli.

Specjalne i ogólne właściwości koloidów
Właściwości układów koloidalnych (lub koloidów) są następujące:
- Charakterystyczny wygląd, szczególnie w przypadku żeli, emulsji i zawiesin, aerozoli.
- Szczególny związek ze światłem przechodzącym przez substancję: większość z nich nie ingeruje w to, a niektóre (przeźroczyste) generalnie rozpraszają wiązkę kierunkową.
- Stały ruch cząstek nie pozwala na tworzenie osadów w układach koloidalnych.
- Ponieważ medium i faza mogą się bardzo różnić w stosunku do siebie, trudno jest wyodrębnić wspólne parametry fizyczne. Muszą odnosić się do każdej konkretnej substancji.
Jeśli mówimy o szczególnych właściwościach rozpatrywanych stanów substancji, powinniśmy zwrócić uwagę Ruch Browna elementy strukturalne i efekt Tyndalla, czyli rozproszenie światła.
Efekt Tyndalla
Zjawisko to zawarte jest w specjalnych właściwościach optycznych układów koloidalnych. Jego istota jest następująca: wiązka światła przechodząca przez roztwór (lub aerozol) układu jest rozproszona. Jednak nie całkiem normalnie. Ponieważ zdolność odbijania lub absorpcji wiązek światła wszystkich cząsteczek jest inna, współczynnik załamania światła zmienia się, okazuje się, że można obserwować punkt w kształcie stożka na ciemnym tle.
Ten efekt służy do określenia jakości, ilości i wielkości cząsteczek tworzących ten system. Po raz pierwszy technika została opracowana i zastosowana przez Johna Tyndalla, za co otrzymała taką nazwę.
Bardzo proste i niedrogie doświadczenie w domu sprawi, że ten efekt będzie dostępny. Konieczne jest przygotowanie roztworu białka z kurczaka w wodzie. Powstanie typowy liofilowy układ koloidalny. Następnie przepuść przez nią promień lasera i zapewnij ciemne tło za naczyniem. Tak więc stożek Tyndalla będzie widoczny bardzo wyraźnie, a światło wewnątrz roztworu rozproszy się.

Ruch Browna cząstek
Jest to kolejna cecha szczególna rozważanych systemów. Polega na ciągłym ruchu cząstek fazowych w środowisku roztworu, zarówno gazowych, jak i ciekłych. Cząsteczki, atomy, jony są w ciągłym chaotycznym krążeniu. Dzięki temu koloid istnieje niezmieniony. Ponadto, ze względu na ich identyczne ładunki, nie występuje przywieranie między nimi. Dzięki temu system może być dość stabilny.
Zjawisko to jest charakterystyczne tylko dla tych cząstek, których rozmiar nie przekracza 3 mikronów. W przeciwnym razie roztwór ulega sedymentacji.
Metody tworzenia koloidów
Metody otrzymywania układów koloidalnych są dość zróżnicowane, ponieważ same systemy nie są takie same. Istnieje kilka najczęściej używanych technik.
- Kondensacja
- Rozpraszanie.
- Peptization
Wszystkie te metody systemów koloidalnych mają szeroką wartość przemysłową podczas pracy z nimi, gdy są one uzyskiwane i badania właściwości. Rozważ bardziej szczegółowo każdy z nich.
Kondensacja to metoda oparta na zdolności cząsteczek i jonów do wiązania się ze sobą, do sklejania się, tworzenia większych cząstek. W ten sposób powstaje nowy system, najczęściej o właściwościach koloidu. Można to zrobić na dwa sposoby:
- zastępowanie rozpuszczalnika (tj. medium);
- kondensacja chemiczna, czyli szereg kolejnych oddziaływań prowadzących do powiększenia cząstek.
I faktycznie, w innym przypadku są to koloidy, w których cząstki stałe są utrzymywane przez ruch Browna w zawieszeniu.
Natomiast dyspergowanie polega na zmieleniu fazy składnika mieszaniny do stanu, w którym roztwór staje się koloidem. Zrób to na kilka sposobów:
- kruszenie mechaniczne;
- natryskiwanie łukiem elektrycznym;
- szlifowanie ultradźwiękowe i tak dalej.
Peptizatsiya - chemiczne rozdrobnienie sklejonych skoagulowanych cząstek na mniejsze struktury. W ten sposób rozwiązania są przygotowywane w przemyśle. W tym samym czasie biorą udział specyficzni agenci - peptizers.

Warunki stanu ustalonego
Stabilność układów koloidalnych wymaga pewnych warunków. W końcu już mówiliśmy, że z czasem mogą się zawalić, czasem nieodwracalnie. Dotyczy to zwłaszcza systemów liofilicznych - zoli. Dlatego istnieją sposoby na zachowanie i zwiększenie stabilności koloidów:
- Dodanie specjalnych antykoagulantów - stabilizatorów.
- Wprowadzenie stałych i tymczasowych elektrolitów w celu zmiany wartości potencjału elektrody uczestników systemu.
Pozostałe metody są wąsko specyficzne dla każdego poszczególnego koloidu, gdy wszystkie właściwości roztworu są brane pod uwagę.
Rozkład i znaczenie układów koloidalnych
Możesz spotkać się z koloidami zarówno w laboratorium chemicznym, jak iw przyrodzie. Wiadomo, że prawie wszystkie wewnętrzne biologiczne żywa materia organizm to dokładnie takie rozproszone systemy. Na przykład:
- cytoplazma;
- stroma;
- szpik kostny i inne.
Wśród materiałów budowlanych znajduje się wiele systemów koloidalnych, które mają dobre właściwości techniczne. Są to beton, stopy metali, związki zawierające glinę, piany, aerozole i tak dalej.
Farmaceutyki są na ogół niemożliwe bez koloidów. Wszystkie pasty, maści, żele, zawiesiny i emulsje są lekami, które są systemami, które rozważamy. Dlatego trudno jest przecenić wartość i rozkład koloidów, są one jednym z najbardziej powszechnych i powszechnie stosowanych rodzajów agregacyjnego stanu materii.