Energia Gibbs i jej wykorzystanie do opisania możliwości procesów
Pojęcie wolnej energii Gibbsa wprowadzono do chemii w celu wyjaśnienia możliwości spontanicznego lub spontanicznego wystąpienia określonej reakcji. Obliczenie tej energii wymaga znajomości zmiany entropii procesu i ilości energii, która jest absorbowana lub uwalniana podczas jego realizacji.
Josiah Willard Gibbs

Wolna energia, która determinuje możliwość różnych procesów, jest oznaczona wielką literą G. Na cześć XIX-wiecznego amerykańskiego fizyka teoretycznego Josiaha Willarda Gibbsa, nazwana została energią Gibbsa, która wniosła istotny wkład w rozwój nowoczesnej teorii termodynamiki.
Warto zauważyć, że jego pierwsza teza, po obronie, który Gibbs otrzymał tytuł doktora, pisał o kształcie zębów kół zębatych. W tym badaniu użył metod geometrycznych do opracowania idealnego kształtu tych zębów. Naukowiec rozpoczął naukę termodynamiki dopiero w wieku 32 lat, aw tej dziedzinie fizyki osiągnął wielki sukces.
Podstawowe pojęcia termodynamiki
Standardowa energia Gibbsa jest energią w standardowych warunkach, tj. W temperaturze pokojowej (25 ° C) i ciśnieniu atmosferycznym (0,1 MPa).
Aby zrozumieć podstawowe zasady termodynamiki, należy również wprowadzić pojęcia entropii i entalpii systemu.
Entalpia rozumiana jest jako energia wewnętrzna układu, który ma określone ciśnienie i objętość. Wartość ta jest oznaczona przez łacińską literę H i jest równa U + PV, gdzie U - energia wewnętrzna systemy, P - ciśnienie, V - objętość systemu.
Entropia systemu jest wielkością fizyczną, która charakteryzuje miarę zaburzenia. Innymi słowy, entropia opisuje położenie cząstek, które składają się na ten system, czyli charakteryzuje prawdopodobieństwo istnienia każdego stanu tego układu. Zazwyczaj jest to oznaczone literą łacińską S.
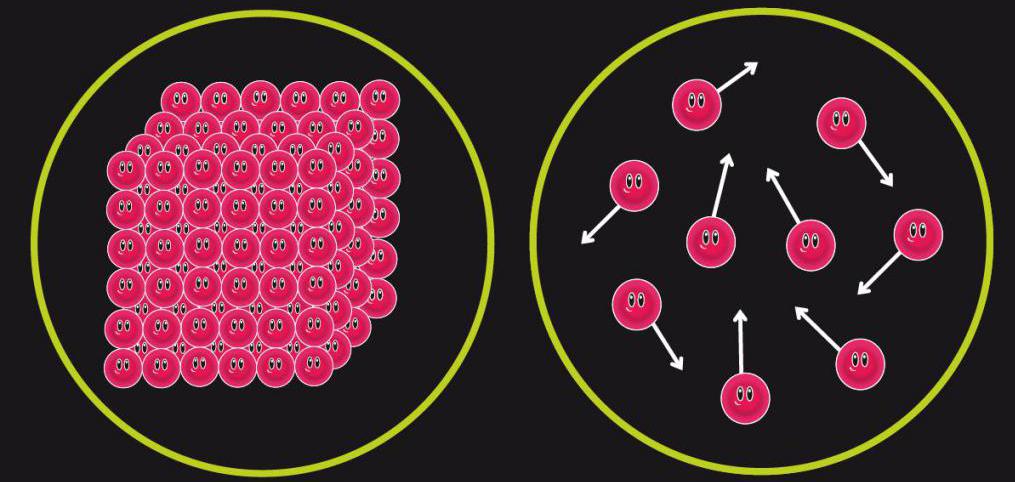
Zatem entalpia jest charakterystyką energetyczną, a entropia jest geometryczna. Zauważmy, że dla zrozumienia i opisania występujących procesów termodynamicznych, bezwzględne wartości entropii i entalpii nie niosą użytecznej informacji, ważne są tylko wielkości ich zmian, to jest ΔH i ΔS.
Termodynamiczne stwierdzenia
To prawo pomaga zrozumieć, w którym kierunku reakcja może przebiegać arbitralnie, lub będzie w stanie równowagi. Poniższe stwierdzenia mają fundamentalne znaczenie dla termodynamiki:
- Druga zasada termodynamiki mówi, że proces w dowolnym systemie zachodzi arbitralnie, jego entropia musi wzrosnąć, to jest ΔS> 0.
- Przy stałej temperaturze i ciśnieniu zmiana energii Gibbsa układu określona jest wzorem ΔG = ΔH - TΔS.
- Jeśli dla dowolnego procesu ΔG <0, to działa spontanicznie i jest nazywany egzergonicznym.
- Kierunek dowolnego przebiegu danej reakcji może zależeć od temperatury w układzie.
Procesy spontaniczne
W chemii procesy losowe to te, które występują bez zewnętrznego wkładu energii do nich. Samowolność perkolacji wskazuje na prawdopodobieństwo takiej możliwości i nie jest w żaden sposób związana z kinetyką procesu. Tak więc może przebiegać szybko, to znaczy mieć charakter wybuchowy, ale może również postępować bardzo powoli przez tysiące milionów lat.

Klasycznym przykładem spontanicznie występującej reakcji jest konwersja węgla w postaci diamentu w alotropową modyfikację węgla grafitu. Taka reakcja jest tak powolna, że w jego życiu nikt nie zauważy żadnych zmian w oryginalnym diamentie, więc mówią, że diamenty są wieczne, chociaż jeśli poczekasz odpowiedni okres czasu, możesz zobaczyć, jak brylantowy kamień staje się czarny, jak grafit z sadzy.
Uwolnienie energii i absorpcja

Innym ważnym aspektem dowolnie postępujących procesów jest uwalnianie lub absorpcja ciepła, w pierwszym przypadku mówią o procesie egzotermicznym, w drugim przypadku proces endotermiczny, to znaczy jest to znak zmiany entalpii ΔH. Należy pamiętać, że zarówno procesy egzotermiczne, jak i endotermiczne mogą przebiegać dowolnie.
Najlepszym przykładem losowego procesu jest zapłon mieszanki paliwowej w cylindrze silnika spalinowego. W tej reakcji uwalniana jest duża ilość energii cieplnej, która jest przekształcana z wydajnością około 30% energia mechaniczna wymuszenie obrotu wału korbowego. Ten ostatni przenosi moment obrotowy poprzez przekładnię na koła samochodu, a samochód porusza się.
Przykładem endotermicznej reakcji, która przebiega niezależnie od absorpcji ciepła, jest rozpuszczanie zwykłego chlorku sodu w wodzie. W tej reakcji ΔH = +3,87 kJ / mol> 0. Fakt ten można sprawdzić mierząc temperaturę wody, zanim sól się w niej rozpuszcza i po jej rozpuszczeniu. Powstała różnica między temperaturą końcową a temperaturą początkową będzie ujemna.
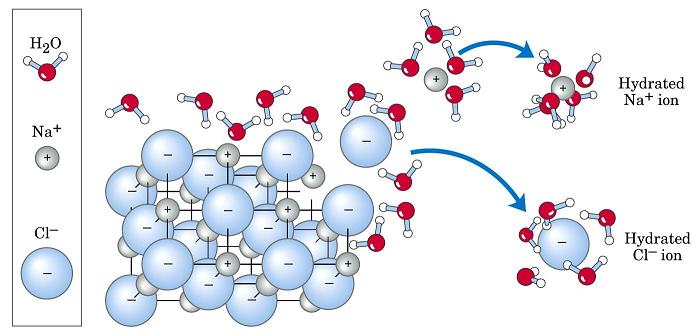
Proces energetyczny Gibbs
Jeżeli jakikolwiek proces odbywa się w układzie o stałym ciśnieniu i temperaturze, wówczas drugie prawo termodynamiki można przepisać w następujący sposób: G = H - TS. Wartość energii swobodnej G - Gibbs ma wymiar kJ / mol. Określenie spontaniczności danej reakcji zależy od znaku zmiany tej wielkości, to jest ΔG. W rezultacie druga zasada termodynamiki przyjmuje postać: ΔG = ΔH -TΔS. Możliwe są następujące przypadki:
- ΔG <0 - reakcja jest nazywana egzergoniczną i losowo pojawia się w kierunku do przodu z tworzeniem produktów;
- ΔG> 0 - reakcja endogeniczna, która nie może dowolnie wystąpić w kierunku do przodu, ale niezależnie pójdzie w przeciwnym kierunku ze wzrostem liczby odczynników;
- ΔG = 0 - układ jest w równowadze, a stężenia reagentów i produktów pozostają stałe przez arbitralnie długi czas.
Analiza uzyskanego równania
Wprowadzone wyrażenie drugiej zasady termodynamiki pozwala nam określić, w którym przypadku proces może przebiegać dowolnie. W tym celu należy przeanalizować trzy wielkości: zmianę entalpii ΔH, zmianę entropii ΔS i temperatury T. Należy zauważyć, że temperatura jest wyrażona w jednostkach bezwzględnych zgodnie z międzynarodowym systemem miar i wag, to jest w kelwinach, więc zawsze jest to wartość dodatnia.
Kierunek reakcji nie zależy od temperatury, jeśli:
- Reakcja jest egzotermiczna (ΔH <0), a jej entropia wzrasta (ΔS> 0). W tym przypadku proces przebiega arbitralnie w kierunku do przodu;
- Reakcja endotermiczna (ΔH> 0) i zmiana jej entropii są ujemne (ΔS <0). Proces nigdy nie pójdzie spontanicznie w kierunku do przodu.
Jeżeli objawy zmian wartości ΔH i ΔS pokrywają się, to temperatura już odgrywa ważną rolę w możliwości takiego procesu. Zatem egzotermiczna reakcja będzie przebiegać dowolnie w niskich temperaturach i egzotermiczna reakcja w wysokich temperaturach.
Obliczenia topnienia lodu

Dobrym przykładem reakcji, w której energia Gibbsa zależy od temperatury, jest topnienie lodu. W tym procesie ΔH = 6,01 kJ / mol, to znaczy, reakcja jest endotermiczna, ΔS = 22,0 J / mol * K, to znaczy, proces zachodzi ze wzrostem entropii.
Do topienia lodu obliczamy temperaturę, w której zmiana energii Gibbsa będzie równa zeru, czyli układ będzie w stanie równowagi. z druga zasada termodynamiki otrzymujemy: T = ΔH / ΔS, zastępując wartości tych wielkości, obliczamy T = 6,01 / 0,022 = 273,18 K.
Jeśli zmienimy temperaturę z Kelvina na zwykłą stopnie Celsjusza, otrzymamy 0 ºC. Oznacza to, że w temperaturze wyższej od tej, wartość ΔG <0, i topnienie lodu samorzutnie, w temperaturze poniżej 0 ° C ΔG> 0, a proces odwrotny nastąpi arbitralnie, to jest, krystalizacja ciekłej wody.