Druga zasada termodynamiki. Interpretacja, uzasadnienie teoretyczne i praktyczne
W fizyce, ponieważ jest to nauka ścisła, większość dogmatów udowodniono empirycznie. Tak powstała druga zasada termodynamiki, która jest obecnie badana w każdej szkole. Nieodwracalne procesy termiczne - tak mówi. Warto zauważyć, że na początkowych etapach badania taka interpretacja jest znacznie bardziej zrozumiała.
Ogólne widoki
Zasada fizyczna, która ogranicza kierunek różnych procesów w systemy termodynamiczne jest drugą zasadą termodynamiki. Definicja tego terminu została sformułowana w XIX wieku, najpierw przez Rudolfa Clausisa, a następnie przez Williama Thomsona (lorda Kelvina). Zgodnie z dwoma postulatami na świecie nie może istnieć rodzaj perpetuum mobile drugiego rodzaju. Nie ma i nie będzie takiej instalacji, która mogłaby ogrzewać się, emanując ze wszystkich rzeczy, żywych istot i zjawisk, zamienionych w energię do swojej stałej pracy. Na tej podstawie ustalono zasadę, że wydajność nie może być równa jednej. Można to porównać z działaniem lodówki, gdzie temperatura, powiedzmy, będzie równa absolutne zero. W takich warunkach wykluczona jest okrągła wymiana ciepła. 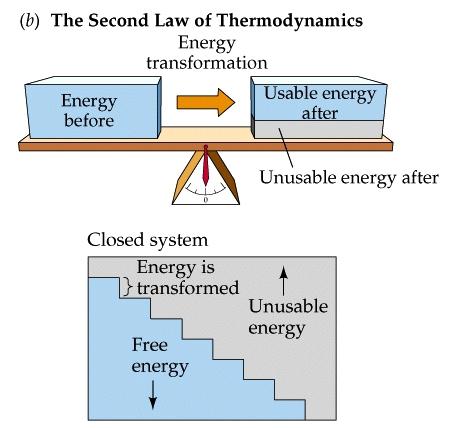
Formulacja Rudolph Clausis
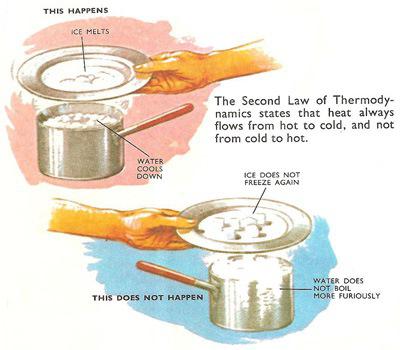
Pierwszy głosił drugi prawo termodynamiki R. Clausis - niemiecki fizyk i matematyk. Według niego, niemożliwy jest okrągły proces, w którym wynik osiąga się poprzez przeniesienie ciepła z mniej ogrzanego ciała do bardziej ogrzanego. Innymi słowy, temperatura w całości lub w części może swobodnie przechodzić z cieplejszego ciała do chłodniejszego, ale proces ten nie może zachodzić w przeciwnym kierunku. To wyraźnie pokazuje nam brak cykliczności, błędne koło. Takie koncepcje są nie do przyjęcia dla termodynamiki. Ciepło jest po prostu wymieniane między ciałami, a w wyniku tych działań nie wytwarza się nadwyżka energii. 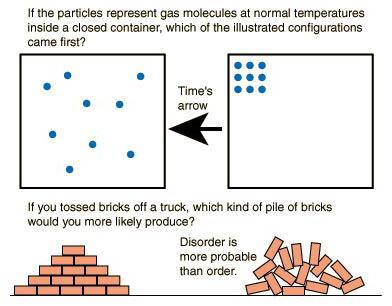
Postulat wyprowadzony przez Lorda Kelvina
Podobna definicja drugiej zasady termodynamiki otrzymana w pismach Thomsona - brytyjskiego fizyka i mechanika. Teoretycznie brzmi to tak: "Cykliczny proces, którego jedynym rezultatem może być praca uzyskana przez ochłodzenie ciepłego ciała lub zbiornika, jest niemożliwa". Aby lepiej zrozumieć tę interpretację, wyobraźmy sobie pewną maszynę (nie może istnieć zgodnie z postulatem termodynamicznym). Okresowo chłodzi zbiornik z ciągle gorącą wodą, odbierając z tej energii cieplnej. Dzięki tej energii maszyna unosi różne obciążenia, takie jak dźwig budowlany. W tym przypadku nie ma silnika, elektrowni i innego mechanicznego wypełnienia. Pod względem fizyki empirycznej jest to niemożliwe. 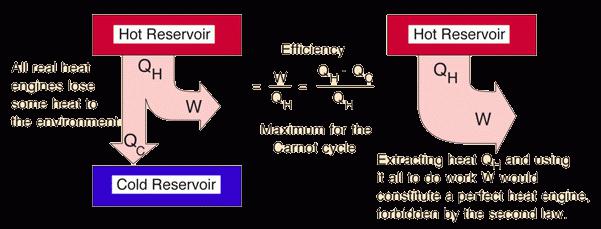
Co jest wspólne?
Teraz zastanowimy się, w jaki sposób te dwie interpretacje są połączone i na których opiera się druga zasada termodynamiki. Entropia jest miarą chaosu, który wzrasta w procesie wymiany ciepła. Że jest to element łączący do opisu Clausisa i Kelvina. Ale wróć trochę. Druga zasada termodynamiki mówi, że przy wymianie ciepła energia maleje (dlatego uzyskanie pracy nie jest możliwe), ale miara chaosu wzrasta. Proces ten jest nieodwracalny i często nazywany spontanicznym. W termodynamice entropia jest ciągle mnożona, ale jej zniszczenie jest niemożliwe. Dlatego nawet 100 procent energii, która jest w jakimkolwiek ciele, nie może zostać przekształcone w pracę. 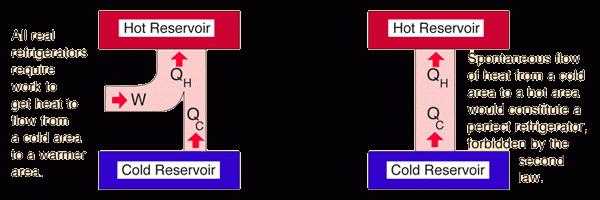
Jaka jest miara chaosu?
Koncepcję entropii sformułowano po raz pierwszy w ustach Clausisa. Wykorzystano go do określenia miary nieodwracalnego procesu rozpraszania energii. To była pewna różnica w odchyleniu rzeczywistego procesu od ideału. Entropia w systemach zamkniętych, gdzie wszystkie procesy zachodzą cyklicznie, ma stałą wartość. Jeśli proces jest nieodwracalny (który bezpośrednio dotyczy termodynamiki), wówczas entropia ma zawsze znaczenie pozytywne. Warto również zauważyć, że miara chaosu jest generowana przez absolutnie wszystkie procesy zachodzące we Wszechświecie. Przy stałych wskaźnikach objętości i energii ciała lub zbiornika entropia stale rośnie. Jeśli te liczby zmieniają się okresowo, wówczas miara chaosu może zostać zmniejszona z powodu wykonywanej pracy, ale całkowite jej zniszczenie jest niemożliwe. Należy zauważyć, że entropia Wszechświata nie zmniejsza się. Pozostaje on normalny lub na stałe rośnie.
Ad
Przykładowy przykład
Drugą zasadę termodynamiki można wyjaśnić za pomocą standardowego przykładu, który często jest przekazywany studentom. Mamy dwa ciała o różnych temperaturach. Im bardziej nagrzana substancja wydzieli się, tym mniej ciepła będzie ogrzewana, aż odczyty temperatury staną się równe. Podczas tego procesu entropia pierwszego, cieplejszego ciała zmniejszy się o mniejszą liczbę, niż wzrośnie w drugim, chłodniejszym ciele. W rezultacie taki spontaniczny proces stworzy entropię systemu, którego indeks będzie wyższy niż całkowita wartość entropii dwóch ciał w pozycji wyjściowej. Innymi słowy, zwiększyła się miara chaosu układu dwóch substancji, wynikająca z wymiany ciepła. 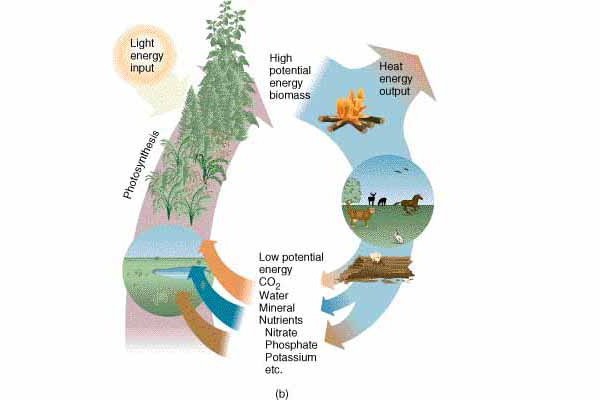
Termiczna śmierć wszechświata
Prowadząc badania, Clausis doszedł do wniosku, że niezależnie od tego, jak otwarta wydaje się nam przestrzeń (nasza planeta, jej odrębne terytoria, obszary wodne itp.), Wszystko to znajduje się w przestrzeni. Wszechświat jest z kolei największą zamkniętą przestrzenią, w której zachodzą procesy makroskopowe. Ponieważ w zamkniętym systemie entropia stale zwiększa swój wskaźnik, nasz świat zbliża się do tego, że już wkrótce miara chaosu osiągnie nieskończoną wartość. Oznacza to, że wszystkie procesy po prostu się zatrzymują z powodu wyczerpania energii. Taki punkt krytyczny, do którego dojdziemy prawdopodobnie w pewnej przyszłości, otrzymał nazwę śmierci termicznej. Okazuje się, że wszystkie nasze działania (ruchy, chodzenie, bieganie), wszystkie zjawiska zachodzące na planecie (powiew wiatru, tsunami, ruch płyt litosfery) - wszystko to powoduje nieodwracalny wzrost entropii i energii wydechowej.
Ad
Obalenie teorii
Człowiek nadal nie może osądzać całego kosmosu. Widzimy tylko część świata, w którym żyjemy, i badamy ten kąt, udowadniając pewne prawa i tworząc na ich podstawie własne pomysły. Dlatego pierwszym odrzuceniem możliwości śmierci termicznej, która opiera się na drugiej zasadzie termodynamiki, jest to, że Wszechświat może nie być systemem zamkniętym. Wiadomym jest, że 85 procent kosmosu składa się z antymaterii, której właściwości nikomu nie są znane. Drugie obalenie jest takie, że nasz kosmos, nawet jeśli jest zamknięty, jest ciągłą fluktuacją. Ze względu na różne fluktuacje i zmiany wielkości, masy, energii i temperatury, entropia nie wzrasta (w ogólnej wartości uniwersalnej) i nie zmniejsza się. W związku z tym jesteśmy już w stanie równowagi termodynamicznej lub, według słów Clausisa, w stanie termicznej śmierci.
Podsumowując
Druga zasada termodynamiki jest nierozerwalnie związana z rozwojem nauk ścisłych. Został otwarty na początku postępu naukowego i technologicznego i stał się, jak można powiedzieć, punktem wyjścia do dalszych prac naukowców w dziedzinie matematyki, fizyki i astronomii. Należy zauważyć, że reprezentujemy to wszystko w warunkach ziemskich. Jest prawdopodobne, że w innym środowisku, w którym pola grawitacyjne mają inną siłę, termodynamika będzie działać zgodnie z zupełnie innym schematem.