Tlenek ołowiu: formuła, właściwości, metoda otrzymywania
W tym artykule zajmiemy się tlenkiem ołowiu, pokażemy jego wzór, uwzględnimy właściwości chemiczne i fizyczne, a także nie zapomnimy porozmawiać o tym, jak je uzyskać. Ogólnie rzecz biorąc, ten artykuł spodoba się osobom, które chcą lub już znają chemię. W końcu ołów znajduje się wszędzie. Jeśli nadal nie znasz jego zakresu, przeczytaj ten artykuł, aby zrozumieć pełen potencjał tego pierwiastka chemicznego w układzie okresowym.
Sposoby na zdobycie
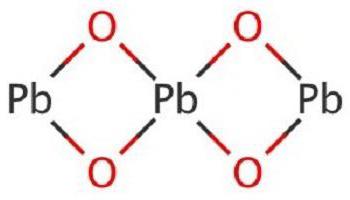
Początkowo zrozumiemy, co nazywa tlenek ołowiu. Jest tradycyjnie określany jako tlenek ołowiu i jest grupą substancji dwuskładnikowych tworzonych przez pierwiastki metalu z ołowiu i niemetalicznego tlenu. Istnieje sześć głównych form PbO: PbO2, PbO, Pb12O19, Pb12O17, Pb3O4. Każda z nich ma swoje cechy strukturalne cząsteczki, metody produkcji i zakres. Najpowszechniejszymi postaciami są tlenek ołowiu (II) i (IV).
Właściwości fizyczne
Tlenek ołowiu, którego formuła jest PbO, może być modyfikowany w dwóch gatunkach: wysoka i niska temperatura. Przejścia od wysokiej temperatury do niskiej temperatury występują wolniej niż w odwrotnej kolejności. W rezultacie pierwiastek może pozostać w metastabilności w temperaturze pokojowej, a podczas procesu mielenia może zmienić formę modyfikacji.

Odparowanie postępuje zgodnie, najczęściej w postaci Pb2O2 i Pb4O4. Również ta grupa tlenków jest półprzewodnikiem. W zależności od rodzaju przewodnictwa, w zależności od składu, ale nie przekraczającego granic jednorodności, tlenki są dziurami i elektronicznymi. W kolorze są zwykle żółte, czerwone i czarne.
Cechy chemiczne i właściwości
Rozpuszczanie zachodzi dobrze w kwasach azotowych i tlenowych, pogarsza się rozpuszczalność w kwasie siarkowym i kwasie chlorowodorowym, ponieważ powstają PbC12 i PbSO4, które są słabo rozpuszczalne. Po rozpuszczeniu w środowisku alkalicznym powstają sześciowodoropropyloaminy (Na2 [Pb (OH) 4]). Są to silne środki utleniające, z których niektóre mogą wykazywać właściwości amfoteryczne - utleniają i absorbują inne substancje. Wszystkie z nich są w stanie utlenić się do różnych stanów, na przykład na otwartym powietrzu, PbO w temperaturze 370 stopni zmieni się w Pb12O17, w 540 stopniach utworzy się Pb3O4, a w wodorze (H2) i tlenku węgla (CO) metal powstaje przez redukcję.
Ołów tlenek II
PbO jest związkiem nieorganicznym, który jest słabo rozpuszczalny w wodzie. Jest to dwuskładnikowa substancja w postaci czerwonych lub żółtych kryształów. W tym związku ołów wykazuje drugą wartościowość, co odpowiada stałej wartościowości tlenu. Występuje w przyrodzie z zanieczyszczeniami, na przykład w masie lub lontu ołowiowym.
Jak zdobyć tlenek ołowiu w przemyśle? Wytwarza się go przepuszczając tlen przez przewód ogrzany do temperatury 600 stopni (2Pb + O2-2PbO), ogrzewając wodorotlenek ołowiu w temperaturach około 100-145 stopni (Pb (OH) 2-PbO + CO2) i rozkładając azotany (2Pb (NO3) ) 2-2Pb + 4NO2 + O2), węglan ołowiu grzejnego (PbCO3 - PbO + CO2), rozkład dwutlenku ołowiu (2PbO2 - PbO + O2) i utlenianie siarczków ołowiu (2PbS + 3O2 -2PbO + 2SO2).
Dzięki swoim właściwościom, PbO (II) jest zdolny do tworzenia kryształów w dwóch wariantach modyfikacji, które są stabilne w 489 stopniach i wyższych.

Modyfikacja alfa (węgiel ołowiowy) jest czerwonym kryształem układu tetragonalnego, z grupą przestrzenną P 4 / nmm. Wskaźnik rozpuszczalności w wodzie wynosi α 0,279 22 . Modyfikacja beta (massicot) wykazuje metastabilność w temperaturze pokojowej, ma żółty kolor, postać krystaliczną, rombowy syngon, grupę przestrzenną P bcm. Indeks rozpuszczalności w wodzie wynosi β 0,513 22 g / 100 ml.
Tlenek ołowiu może wykazywać właściwości amfoteryczne podczas interakcji z kwasami (PbO + 2HCl - PbCl2 + H2O) i alkaliami (PbO + 2NaOH- (400 stopni) Na2PbO2 + H2O). Potrafi utleniać się, wchodząc w reakcję z tlenem do Pb3O4 i w wodnej zawiesinie z bromem jest utleniany do ditlenku ołowiu PbO2. Odzyskiwanie metalu następuje przy udziale tlenek węgla wodór i aluminium. W stanie pochłania wilgoć dwutlenek węgla podczas tworzenia podstawowych soli.
Ołów tlenek IV
Tlenek ołowiu 4, znany również jako ditlenek ołowiu, ma wzór PbO2. Jest tlenkiem o wyższych stopniach. Podobnie jak inne związki wiodące z tlenem jest substancją dwuskładnikową. Jest to ciemnobrązowy proszek, dość ciężki, o zapachu ozonu. Wcześniej można go było znaleźć pod nazwą nadtlenku lub nadtlenku ołowiu.

PbO2 jest wydobywany w przemyśle przez przetwarzanie kwas azotowy czerwony ołów, a następnie przemywanie, odkurzanie i suszenie: Pb3O4 + 4HNO3 - PbO2 + 2Pb (NO3) 2 + 2H2O.
Temperatura topnienia tego związku wynosi 290 stopni, gęstość wynosi 9,38 g / cm3, masa molowa 239,1988 g / mol. Dwutlenek ołowiu 4 jest bardzo silnym utleniaczem, może wypierać chlor ze stężonego kwasu solnego poprzez ogrzewanie (PbO2 + 4HCl - PbCl2 + Cl2 + 2H2O). Sole manganu (II) są również utleniające się do nadmanganianu (5Pb02 + 2MnSO4 + 3H2SO4-5PbSO4 + 2HMnO4 + 2H2O). Jest to bardzo toksyczna substancja.
Aplikacja
Zasięg dwutlenku ołowiu jest najbardziej zróżnicowany. Ołówek tlenku 4 znajduje swoje zastosowanie poprzez spełnianie funkcji sykatyw (substancje oleiste niezbędne do przyspieszenia procesu suszenia farb), katalizator (substancje niezbędne do przyspieszenia przepływu reakcje chemiczne pomiędzy związkami, które nie są częścią końcowego składu produktów jakichkolwiek zachodzących reakcji) i środkiem utleniającym (substancjami, które zawierają atomy zdolne do przyłączania się do siebie samych podczas reakcji chemicznej, utleniacz można również nazwać akceptorem).

PbO2 jest szeroko stosowany w akumulatorach kwasowo-ołowiowych, jako dodatnie masy elektronów w ogniwach galwanicznych. Często, ale w małych ilościach, może być stosowany jako powłoka dla elektrod w celu usprawnienia procesu elektrolizy. Dwutlenek ołowiu 2 jest wykorzystywany do produkcji kratek, PbO2 można znaleźć w bateriach. Tlenek ołowiu jest szeroko stosowany w produkcji ołowianych szkieł i szkliw. Pb3O4 można znaleźć w akumulatorach ołowiowych jako szpachlówkę i jako pigment do farb antykorozyjnych. Większość tlenków ołowiu jest wykorzystywanych do produkcji urządzeń radiotechnicznych, wyrobów gumowych. Są one również niezbędne w procesie ekstrakcji soli ołowiu podczas syntezy chemicznej.