Produkcja alkoholi, zastosowanie, właściwości. Metody produkcji alkoholi
Alkohole mają powszechny charakter. Większość ludzi zna alkohol etylowy (etanol) jest aktywnym składnikiem napojów alkoholowych, ale jest tylko jedną z rodziny związków organicznych znanych jako alkohole. Zdobycie ich, przede wszystkim etylowego (wino w wyniku enzymatycznej fermentacji soku z winogron, było jednym z pierwszych procesów chemicznych opanowanych przez ludzkość.
Nomenklatura alkoholi
Alkohole reprezentują związki organiczne hydroksylowa (OH) grupa funkcyjna z alifatycznym atomem węgla. Ponieważ OH jest członkiem cząsteczek wszystkich alkoholi, są one często przedstawiane jako pochodne wody o wzorze ogólnym ROH, gdzie R oznacza grupę alkilową.
Produkcja alkoholi metanolowych (CH 3 OH) i etanolu (CH 3 CH 2 OH), które są pierwszymi dwoma członkami ich serii homologicznej, jest ważnym zadaniem przemysłu chemicznego w wielu krajach. Zawierając od jednego do czterech atomów węgla, często nazywa się je pospolitymi nazwami, w których po nazwie grupy alkilowej występuje słowo alkohol: 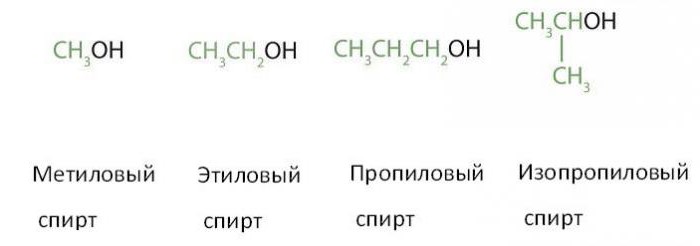
Można zauważyć, że wszystkie cztery (ostatnie dwa są izomerami jednej substancji) powyższe cząsteczki alkoholu zawierają jedną grupę hydroksylową. Na tej podstawie wszystkie należą do jednowodorotlenowych alkoholi (są też dwa, trzy, cztery i wieloatomowe). Ponadto wszystkie są pochodnymi nasyconych węglowodorów z szeregu alkanów: metanu, etanu, propanu (nazwy alkoholi otrzymuje się przez dodanie do nazwy alkenu końcówki "-ol"). Dlatego nazywane są one również marginalnymi jednowodorotlenowymi alkoholami.
Ad
Alkohole jednowodorotlenowe
Produkcja, właściwości (fizyczne i chemiczne) tych związków zależą od liczby atomów węgla przyłączonych do atomu, bezpośrednio związanych z grupą OH. Dlatego jednowodorotlenowe alkohole można podzielić na trzy klasy na tej podstawie.
- Pierwszorzędowe alkohole mają cząsteczkę, w której jeden atom węgla związany z grupą OH jest przyłączony do innego atomu C. Ich ogólny wzór to RCH2OH. Na przykład alkoholem podstawowym jest etanol.
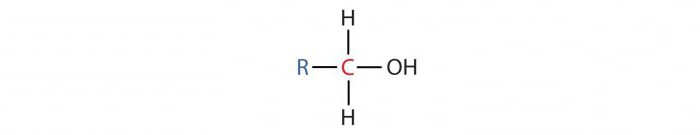
- Wtórne alkohole mają jeden atom węgla w cząsteczce z grupą OH przyłączoną do dwóch innych atomów C. Ich ogólny wzór to R2 CHOH. Należą do nich: alkohol propylowy i izopropylowy.
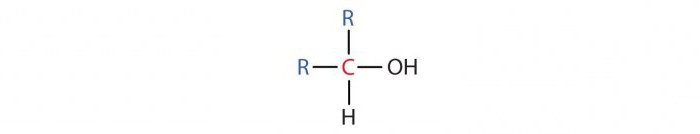
- Trzeciorzędowe alkohole zawierają w cząsteczce atom węgla z grupą OH przyłączoną do trzech innych atomów C. Ich ogólnym wzorem jest R3COH.

Otrzymywanie jednowodorotlenowych alkoholi w przemyśle jest możliwe na wiele sposobów, co zostanie omówione poniżej.
Metanol jako produkt z gazu ziemnego
Metanol otrzymuje się przez zmieszanie gazu z wodorem i tlenku węgla w wysokich temperaturach i ciśnieniach (200 przy 350 ° C) w obecności katalizatora składającego się z tlenek cynku (ZnO) i tlenek chromu (Cr 2 O 3 ) jako katalizator: 2H 2 + CO → CH 3OH. 
W tym przypadku surowcem do produkcji odczynników jest gaz ziemny i para wodna, mieszanie, które wytwarza gaz syntezowy, który jest mieszaniną CO i H2.
Metanol jest ważnym rozpuszczalnikiem i jest używany jako paliwo samochodowe, albo jako czysty płyn - w niektórych samochodach wyścigowych, albo jako wysokooktanowy dodatek do benzyny. Produkcja i wykorzystanie alkoholi na świecie, w szczególności metanolu, mierzona jest w milionach ton. Pod koniec 2013 r. Na całym świecie zużyto 66 milionów ton metanolu, z czego 65% w Azji, 17% w Europie i 11% w USA.
Ad
Uzyskiwanie najlepszych alkoholi z alkenów
Wiele prostych alkoholi o znaczeniu przemysłowym wytwarza się przez hydratację (przez dodanie wody) alkenów (etylenu, propylenu, butenu). W wyniku tej reakcji otrzymuje się etanol, izopropanol, butanol (drugorzędowy i trzeciorzędowy).
Znane bezpośrednie i pośrednie sposoby wytwarzania alkoholi przez hydratację. Direct pozwala uniknąć tworzenia stabilnych produktów pośrednich, zwykle za pomocą katalizatorów kwasowych.
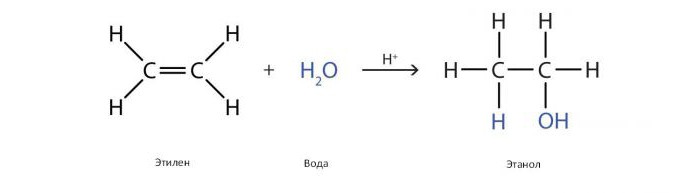
Katalizator jest zwykle kwas fosforowy, adsorbowane na porowatym nośniku, takim jak żel krzemionkowy lub ziemia okrzemkowa. Katalizator ten został po raz pierwszy użyty do produkcji etanolu na dużą skalę w Stanach Zjednoczonych przez Shell w 1947 roku. Reakcję prowadzi się w obecności pary o wysokim ciśnieniu w 300 ° C, przy czym stosunek 1,0: 0,6 utrzymuje się pomiędzy etylenem i parą.
Ad
Podobna reakcja na wytwarzanie alkoholu izopropylowego z katalizatorami w postaci kwas siarkowy wygląda tak 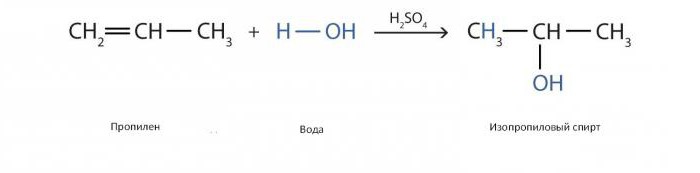
Pośrednia metoda hydratacji etylenu
W sposób pośredni, w praktyce po raz pierwszy zastosowany na skalę przemysłową w 1930 r., Ale dziś uważany za prawie całkowicie przestarzały, reakcją na wytwarzanie alkoholi jest zamiana alkenu w estry siarczanowe, które są następnie hydrolizowane. Tradycyjnie alken traktuje się kwasem siarkowym w celu wytworzenia estrów alkilosiarczanowych. W przypadku produkcji etanolu, etap ten można zapisać następująco: H 2 SO 4 + C 2 H 4 → C 2 H 5 -O-SO 3 H
Następnie, ester siarczanowy hydrolizuje aż do regeneracji kwasu siarkowego i uwolnienia etanolu: C 2 H 5 -O-SO 3 H + H 2 O → H 2 SO 4 + C 2 H 5 OH.
Metody wytwarzania alkoholi są niezwykle różnorodne, ale proces opisany poniżej jest prawdopodobnie znany, przynajmniej w oparciu o informacje dla każdego czytelnika.
Fermentacja alkoholowa
Jest to proces biologiczny, w którym cząsteczki, takie jak glukoza, fruktoza i sacharoza, przekształcają się w energię komórkową dzięki równoległemu wytwarzaniu etanolu i dwutlenku węgla jako produktów przemiany materii. Fermentacja jest katalizowana przez enzymy zawarte w drożdżach i przebiega w złożonym wieloetapowym mechanizmie, który zwykle obejmuje przekształcenie (w pierwszym etapie) skrobi zawartej w ziarnach roślinnych w glukozę, a następnie wytworzenie z niej etanolu. Ponieważ drożdże przeprowadzają tę transformację w nieobecności tlenu, fermentacja alkoholowa jest uważana za proces beztlenowy.
Ad
Reakcje fermentacji alkoholi można przedstawić następująco: 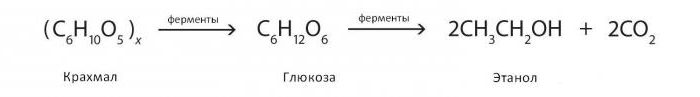
Sposoby pobierania napojów alkoholowych
Cały etanol zawarty w napojach alkoholowych powstaje w wyniku fermentacji spowodowanej przez drożdże.
Wino powstaje w drodze fermentacji naturalnych cukrów obecnych w winogronach; Cydr jest otrzymywany przez analogiczną fermentację naturalnego cukru odpowiednio w jabłkach i gruszkach; i inne wina owocowe są wytwarzane przez fermentację cukrów w dowolnych innych rodzajach owoców. Orzechy brandy i wódki brandy (na przykład śliwowica) są produkowane przez destylację napojów otrzymywanych przez fermentację cukrów owocowych.
Napoje miodowe są wytwarzane w drodze fermentacji z naturalnych cukrów obecnych w miodzie. 
Piwo, whisky i wódka są produkowane przez fermentację ziaren skrobi, które są przekształcane w cukier przez działanie enzymu amylazy, który jest obecny w ziarnach ziarna, które uległy kiełkowaniu słodowania. Inne źródła skrobi (na przykład, ziemniaki i niesłodowane ziarna) można dodać do mieszaniny, ponieważ amylaza będzie również działać na ich skrobię.
Ad
Wina ryżowe (w tym sake) są produkowane w drodze fermentacji skrobi zbożowej, przekształconej w cukier przez Asugi Aspergillus ogugae.
Rum i inne napoje są otrzymywane przez fermentację i destylację trzciny cukrowej. Rum jest zwykle wytwarzany z trzciny cukrowej - melasy.
We wszystkich przypadkach fermentacja powinna nastąpić w naczyniu, które pozwala na ucieczkę dwutlenku węgla, ale zapobiega przedostawaniu się powietrza z zewnątrz. Jest to konieczne, ponieważ działanie tlenu zapobiega tworzeniu się etanolu, a nagromadzenie dwutlenku węgla stwarza ryzyko pęknięcia naczynia. 
Reakcja substytucji nukleofilowej
Alkohole są produkowane w laboratoriach metodami, w których jako substancje wyjściowe w reakcjach stosuje się substancje chemiczne o różnych klasach, od węglowodorów po związki karbonylowe. Istnieje kilka sposobów, które sprowadzają się do kilku podstawowych reakcji.
Początkowe halogenoalkany reagują z wodnymi roztworami alkalicznego NaOH lub KOH, tworząc, głównie, pierwszorzędowe alkohole w reakcji nukleofilowego podstawienia alifatycznego. Gdy, na przykład, bromek metylu reaguje z roztworem wodorotlenku sodu, grupy hydroksylowe powstałe podczas dysocjacji alkaliów, zastępują jony bromu powstawaniem metanolu. 
Poniżej wymieniono kilka reakcji, które pozwalają na wytwarzanie alkoholi w laboratoriach.
Dodatek nukleofilowy.
Odczynniki Grignarda (związki magnezu z halogenkami alkilowymi - jodkami lub bromkami), a także związki metaloorganiczne miedzi i litu reagują z grupami karbonylowymi (C = O) aldehydami tworząc pierwszorzędowe i drugorzędowe alkohole, w zależności od mechanizmu dodawania .. Podobne reakcje z ketonami prowadzą do trzeciorzędowych alkoholi . 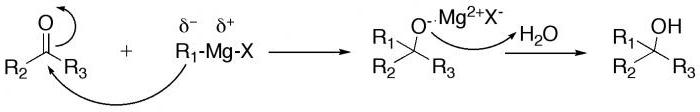
Reakcja Barbiera przebiega pomiędzy chlorowco-alkanem i grupą karbonylową jako elektrofilowym substratem w obecności magnezu, glinu, cynku, indu, cyny lub jego soli. Produktem reakcji jest pierwszorzędowy, drugorzędowy lub trzeciorzędowy alkohol. Jego mechanizm jest podobny do reakcji Grignarda, z tą różnicą, że reakcja Barbiera jest syntezą w jednym naczyniu, podczas gdy odczynnik Grignarda wytwarza się oddzielnie przed dodaniem związku karbonylowego. 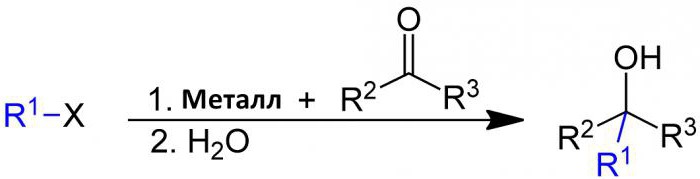 Będąc nukleofilową reakcją addycji, występuje ona w przypadku stosunkowo tanich i wodoodpornych metali lub ich związków, w przeciwieństwie do odczynników Grignarda lub odczynników organolitycznych. Z tego powodu w wielu przypadkach można go uruchomić w wodzie, co czyni proces częścią zielonej chemii. Reakcja Barbiera pochodzi od Philipa Barbiera, nauczyciela Victora Grignarda.
Będąc nukleofilową reakcją addycji, występuje ona w przypadku stosunkowo tanich i wodoodpornych metali lub ich związków, w przeciwieństwie do odczynników Grignarda lub odczynników organolitycznych. Z tego powodu w wielu przypadkach można go uruchomić w wodzie, co czyni proces częścią zielonej chemii. Reakcja Barbiera pochodzi od Philipa Barbiera, nauczyciela Victora Grignarda.
Reakcja regeneracji
Aldehydy lub ketony redukuje się do alkoholi z borowodorkiem sodu (NaBH4) lub (po obróbce kwasem) wodorkiem litowo-glinowym (LiAlH).
W reakcji Meerweina-Pondorfa-Wehrli (MPV) wytwarzanie alkoholi przez ich redukcję z ketonów i aldehydów odbywa się z użyciem katalizatora alkoholanowo-glinowego. Zaletami MPV są wysoka chemoselektywność i zastosowanie taniego, przyjaznego dla środowiska katalizatora metalicznego. Reakcję odkryli Meerwein i Schmidt, a niezależnie Verli w 1925 r. Stwierdzili, że mieszanina etoksylanu glinu i etanolu może redukować aldehydy do ich alkoholi. Ponndorf zastosował reakcję do ketonów i zaktualizował katalizator do izopropanu glinu (Al (Oi-Pr) 3 , gdzie i-Pr oznacza grupę izopropylową (CH (CH3) 2 ). w celu uzyskania izopropanolu.
Ogólne równanie otrzymywania alkoholu przez redukcję ketonów do alkoholi MPV jest następujące:
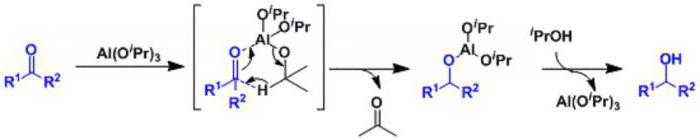
To oczywiście nie wszystko, co można powiedzieć o alkoholach i ich właściwościach, ale mamy nadzieję, że udało się uzyskać ogólny pogląd na ich temat.