Zagregowany stan materii. Zmiana stanu materii
Cała materia może istnieć w jednym z czterech typów. Każdy z nich jest pewnym skupionym stanem materii. W naturze Ziemi tylko jedna reprezentowana jest w trzech z nich naraz. To jest woda. Łatwo go zobaczyć i odparować, stopić i stwardnieć. To znaczy, para wodna, woda i lód. Naukowcy nauczyli się zmieniać stan agregacji materii. Największą trudnością dla nich jest tylko plazma. Ten stan wymaga specjalnych warunków.

Co to jest i na czym polega?
Jeśli ciało przeniosło się do innego stanu skupienia substancji, to nie oznacza to, że pojawiło się coś innego. Substancja pozostaje taka sama. Jeśli ciecz ma cząsteczki wody, to będą one takie same w przypadku pary z lodem. Zmieni się tylko ich położenie, prędkość ruchu i siły wzajemnego oddziaływania.
Podczas studiowania tematu "Kraje zagregowane (klasa 8)" rozważa się tylko trzy z nich. Tak jest gaz płynny i stałe. Ich przejawy zależą od fizycznych warunków środowiskowych. Charakterystykę tych stanów przedstawiono w tabeli.
| Nazwa stanu agregacji | ciało stałe | ciecz | gaz |
| Jego właściwości | utrzymuje kształt z objętością | ma stałą objętość, przyjmuje postać naczynia | nie ma stałej objętości i kształtu |
| Układ cząsteczek | w punktach kratowych | niekonsekwentny | chaotyczny |
| Odległość między nimi | porównywalne do wielkości cząsteczek | w przybliżeniu równe wielkości cząsteczek | znacznie większy niż ich rozmiar |
| Jak poruszają się molekuły | unoszą się w miejscu kraty | nie ruszaj się z miejsca równowagi, ale czasami wykonuj duże skoki | losowo z przypadkowymi zderzeniami |
| Jak wchodzą w interakcje | mocno przyciąga | mocno przyciągają się do siebie | nie przyciągnięte, siły odpychające powstają przy uderzeniu |
Pierwszy stan: solidny
Podstawową różnicą w stosunku do innych jest to, że cząsteczki mają ściśle określone miejsce. Kiedy mówią o stałym stanie skupienia, często odnoszą się do kryształów. W nich struktura kratowa jest symetryczna i ściśle okresowa. Dlatego zawsze zachowuje się, jak daleko ciało się nie rozprzestrzeni. Ruch oscylacyjny molekuł substancji nie wystarcza do zniszczenia tej sieci.
Ale są też ciała amorficzne. Brak im ścisłej struktury w układzie atomów. Mogą być wszędzie. Ale to miejsce jest tak stabilne jak w krystalicznym ciele. Różnica pomiędzy substancjami amorficznymi i krystalicznymi polega na tym, że nie mają one określonej temperatury topnienia (zestalenie) i charakteryzują je sypkość. Żywe przykłady takich substancji: szkło i plastik.
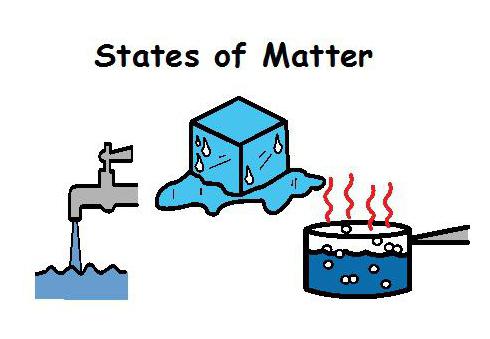
Drugi stan: ciecz
Ten agregatywny stan materii jest krzyżem między ciałem stałym a gazem. Dlatego łączy niektóre właściwości pierwszego i drugiego. Odległość między cząsteczkami i ich oddziaływanie są podobne do kryształów. Ale lokalizacja i ruch bliżej gazu. Dlatego płyn nie zachowuje kształtu, ale rozlewa się na naczynie, do którego jest nalewany.
Trzeci stan: gaz
Dla nauki zwanej "fizyką", stan skupienia w postaci gazu nie jest na ostatnim miejscu. W końcu bada świat, a powietrze w nim jest bardzo powszechne.
Osobliwością tego stanu jest to, że siły oddziaływania pomiędzy cząsteczkami są praktycznie nieobecne. To tłumaczy ich swobodny ruch. Dzięki temu gazowa substancja wypełnia całą dostarczoną do niej objętość. W tym stanie możesz wszystko przenieść, wystarczy tylko podnieść temperaturę do pożądanej wartości.
Czwarty stan: plazma
Ten zagregowany stan skupienia jest gazem całkowicie lub częściowo zjonizowanym. Oznacza to, że liczba ujemnie i dodatnio naładowanych cząstek w nim jest prawie taka sama. Ta sytuacja powstaje, gdy gaz jest ogrzewany. Następnie następuje gwałtowne przyspieszenie procesu termicznej jonizacji. Polega ona na tym, że cząsteczki są podzielone na atomy. Te ostatnie zamieniają się w jony.

W ramach wszechświata taki stan jest bardzo powszechny. Ponieważ zawiera wszystkie gwiazdy i środowisko między nimi. W granicach powierzchni Ziemi występuje niezwykle rzadko. Z wyjątkiem jonosfery i wiatru słonecznego plazma jest możliwa tylko podczas burzy. W przebłyskach błyskawic powstają takie warunki, w których gazy z atmosfery przechodzą do czwartego stanu materii.
Ale to nie oznacza, że plazma nie powstaje w laboratorium. Pierwszą rzeczą, która była w stanie odtworzyć, było wyładowanie gazu. Teraz plazma wypełnia fluorescencyjne światła i reklamę neonową.

Jak przebiega przejście między stanami?
Aby to zrobić, musisz stworzyć określone warunki: stałe ciśnienie i określoną temperaturę. W takim przypadku zmianie stanu skupienia substancji towarzyszy uwalnianie lub absorpcja energii. Co więcej, przejście to nie następuje z prędkością błyskawicy, ale wymaga pewnej ilości czasu. Przez cały ten czas warunki muszą pozostać niezmienione. Przejście następuje z jednoczesnym istnieniem substancji na dwa sposoby, które utrzymują równowagę termiczną.
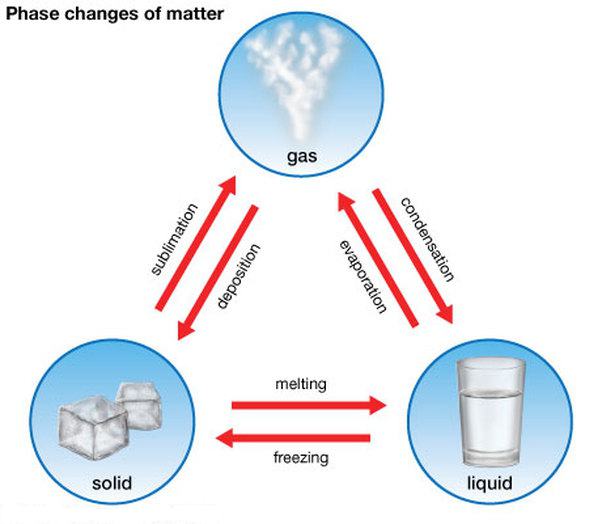
Pierwsze trzy stany materii mogą nawzajem się przenikać. Istnieją procesy bezpośrednie i odwrotne. Mają następujące nazwy:
- topienie (od ciała stałego do cieczy) i krystalizacja , taka jak topnienie lodu i utwardzanie wody;
- waporyzacja (z cieczy na gaz) i kondensacja , przykładem jest parowanie wody i jej wytwarzanie z pary;
- sublimacja (od stałych do gazowych) i desublimacja , na przykład, odparowanie suchego aromatu do pierwszego i odszranianie szkła do drugiego.
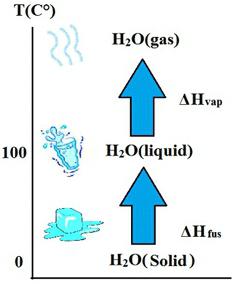
Fizyka topnienia i krystalizacji
Jeśli ciało stałe jest ogrzewane, to w określonej temperaturze, zwanej temperaturą topnienia konkretnej substancji, rozpocznie się zmiana stanu skupienia, zwana topieniem. Proces ten polega na absorpcji energii, która jest nazywana ilością ciepła i jest oznaczona literą Q. Aby to obliczyć, musisz znać ciepło ciepła , które jest oznaczone przez λ . Formuła przyjmuje następujące wyrażenie:
Q = λ * m , gdzie m jest masą substancji biorącej udział w topieniu.
Jeśli wystąpi proces odwrotny, to jest, krystalizacja cieczy, warunki powtarza się. Jedyna różnica polega na tym, że energia jest uwalniana, a znak minus pojawia się w formule.
Fizyka parowania i kondensacji
Przy dalszym nagrzewaniu substancji będzie stopniowo zbliżać się do temperatury, w której rozpocznie się intensywne parowanie. Ten proces nazywa się odparowaniem. Ponownie charakteryzuje się pochłanianiem energii. Tylko do jego obliczeń wymagane jest poznanie ciepła właściwego parowania r . A formuła będzie:
Q = r * m .
Odwrotny proces lub kondensacja następuje po uwolnieniu tego samego ilości ciepła. Dlatego minus pojawia się ponownie w formule.