Atom węgla: struktura, cechy i właściwości
W tym artykule rozważamy element, który jest częścią układu okresowego D.I. Mendeleev, czyli węgiel. W nowoczesnej nomenklaturze jest oznaczony symbolem C, znajduje się w czternastej grupie i jest "uczestnikiem" drugiego okresu, ma szósty numer sekwencji i jej amu. = 12,0107.
Orbitale atomowe i ich hybrydyzacja
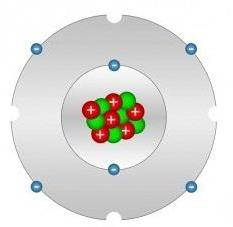
Zacznijmy rozważać węgiel z jego orbitali i ich hybrydyzację - jego główne cechy, dzięki którym wciąż zastanawiają się naukowcy całego świata. Jaka jest ich struktura?
Hybrydyzacja atomu węgla jest zorganizowana w taki sposób, że elektrony walencyjne zajmują pozycje na trzech orbitach, a mianowicie: jeden znajduje się na orbitach 2s, a dwa na orbitach 2p. Dwa ostatnie z trzech orbitali tworzą kąt równy 90 stopni względem siebie, a orbital 2s ma sferyczną symetrię. Jednak ta forma urządzenia z rozważanych orbitali nie pozwala nam zrozumieć, dlaczego węgiel, wchodząc w związki organiczne tworzy kąty 120, 180 i 109,5 stopnia. Wzór na strukturę elektronową atomu węgla wyraża się następująco: (He) 2s 2 2p 2 .
Rozstrzygnięcie powstałej sprzeczności dokonano poprzez wprowadzenie pojęcia hybrydyzacji orbitali atomowych. Aby zrozumieć trihedron, wariant natury C, konieczne było stworzenie trzech form zrozumienia jego hybrydyzacji. Główny wkład w powstanie i rozwój tej koncepcji złożył Linus Pauling.
Właściwości fizyczne
Struktura atomu węgla determinuje obecność pewnej liczby pewnych cech natury fizycznej. Atomy tego pierwiastka tworzą prostą substancję - węgiel, który ma modyfikacje. Różnice w zmianach jego struktury mogą nadawać uformowanej substancji różne cechy jakościowe. Przyczyną obecności dużej liczby modyfikacji węgla jest jego zdolność do tworzenia i tworzenia heterogenicznych wiązań o charakterze chemicznym.
Struktura atomu węgla może być różna, co pozwala na uzyskanie pewnej liczby form izotopowych. Węgiel występujący w przyrodzie tworzy się za pomocą dwóch izotopów w stanie stabilnym - 12 ° C i 13 ° C - oraz izotopu o właściwościach radioaktywnych - 14 ° C. Ostatni izotop jest skoncentrowany w górnych warstwach skorupy ziemskiej i w atmosferze. Ze względu na wpływ promieniowania kosmicznego, a mianowicie jego neutronów, na jądro atomów azotu, powstaje radioaktywny izotop 14 C. Po połowie lat pięćdziesiątych XX wieku zaczął on wpadać do środowiska jako produkt wytworzony przez człowieka podczas eksploatacji elektrowni jądrowych, a także ze względu na wykorzystanie bomba wodorowa. Właśnie w procesie rozpadu 14 C opiera się metoda datowania radiowęglowego, która znalazła szerokie zastosowanie w archeologii i geologii.
Modyfikacja węgla w postaci allotropowej
W przyrodzie istnieje wiele substancji, które zawierają węgiel. Człowiek używa struktury atomu węgla do swoich własnych celów podczas tworzenia różnych substancji, w tym:
- Węglany krystaliczne (diamenty, nanorurki węglowe, włókna i druty, fulereny itp.).
- Węgle amorficzne (węgiel aktywowany i węgiel drzewny, różne rodzaje koksu, sadza, sadza, nanopianki i antracyt).
- Klastry formy węgla (związki di-węgla, nanokon i astralenu).
Strukturalne cechy struktury atomowej
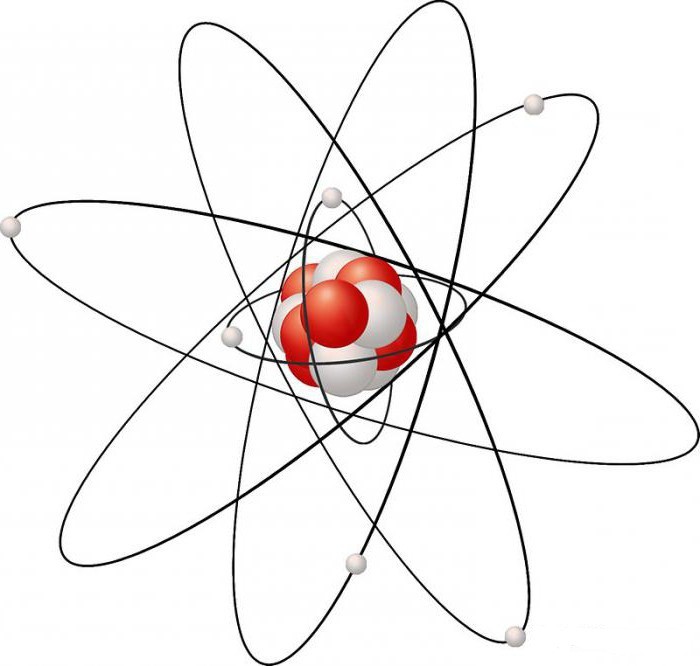
Struktura elektronowa atomu węgla może mieć inną geometrię, która zależy od poziomu hybrydyzacji orbitali, które posiada. Istnieją 3 główne typy geometrii:
- Tetrahedral - powstaje w wyniku przesunięcia czterech elektronów, z których jeden to s-, a trzy należą do p-elektronów. Atom C zajmuje centralne położenie w czworościanie i jest połączony przez cztery równoważne wiązania sigma z innymi atomami zajmującymi wierzchołek tego czworościanu. Przy takim geometrycznym układzie węgla jego alotropowe formy mogą tworzyć, na przykład, diament i lonsdaleit.
- Trigonal - zawdzięcza swój wygląd przesunięciu trzech orbitali, z których jeden to s- i dwa p-. Tutaj są trzy wiązania sigma, które znajdują się w równej pozycji względem siebie; leżą we wspólnej płaszczyźnie i przylegają do siebie pod kątem 120 stopni względem siebie. Wolny orbital p znajduje się prostopadle do płaszczyzny wiązania sigma. Grafit ma podobną geometrię.
- Przekątna - pojawia się ze względu na mieszanie s-i p-elektronów (hybrydyzacja sp). Chmury elektronów są wyciągane wzdłuż ogólnego kierunku i przyjmują formę asymetrycznego hantli. Wolne elektrony tworzą wiązania π. Ta struktura geometrii w węglu powoduje powstanie Carbyne, specjalnej formy modyfikacji.
Atomy węgla w przyrodzie
Struktura i właściwości atomu węgla od dawna są uważane przez człowieka i są wykorzystywane do uzyskiwania dużej liczby różnych substancji. Atomy tego pierwiastka, ze względu na ich wyjątkową zdolność do tworzenia różnych wiązań chemicznych i obecności hybrydyzacji orbitali, tworzą wiele różnych alotropowych modyfikacji z udziałem tylko jednego pierwiastka, z atomów tego samego typu, węgla.

W naturze węgiel znajduje się w skorupie ziemskiej; Ma on postać diamentów, grafitów, różnych palnych bogactw naturalnych, na przykład ropy naftowej, antracytu, węgla brunatnego, łupków, torfu itp. Zawarte w gazach używanych przez człowieka w przemyśle energetycznym. Węgiel w składzie dwutlenku węgla wypełnia hydrosferę i atmosferę Ziemi, aw powietrzu osiąga 0,046%, a w wodzie - nawet sześćdziesiąt razy więcej.
W ludzkim ciele C jest zawarty w ilości w przybliżeniu równej 21% i jest głównie wydalany z moczem i wydychanym powietrzem. Ten sam element bierze udział w cyklu biologicznym, jest pochłaniany przez rośliny i konsumowany podczas fotosyntezy.
Atomy węgla, ze względu na ich zdolność do tworzenia różnych wiązań kowalencyjnych i ich łańcuchów budujących, a nawet cykli, mogą wytworzyć ogromną ilość substancji o charakterze organicznym. Ponadto element ten jest częścią atmosfery słonecznej, będąc w związkach z wodorem i azotem.
Właściwości chemiczne

Rozważmy teraz strukturę i właściwości atomu węgla z chemicznego punktu widzenia.
Ważne jest, aby wiedzieć, że węgiel wykazuje właściwości obojętne w normalnych warunkach temperaturowych, ale może pokazać nam właściwości o charakterze redukującym pod wpływem wysokich temperatur. Główny stany utleniania: + - 4, czasami +2, a także +3.
Uczestniczy w reakcji z dużą liczbą elementów. Może reagować z wodą, wodorem, halogenami, metale alkaliczne kwasy, fluor, siarka itp.
Struktura atomu węgla generuje niesamowicie dużą ilość substancji rozdzielonych na osobną klasę. Takie związki są nazywane organicznymi i są oparte na C. Jest to możliwe dzięki właściwościom atomów tego pierwiastka do tworzenia łańcuchów polimerowych. Do najbardziej znanych i rozległych grup należą białka (białka), tłuszcze, węglowodany i związki węglowodorowe.
Metody operacyjne
Ze względu na unikalną strukturę atomu węgla i towarzyszące mu właściwości, element ten jest szeroko stosowany przez ludzi, na przykład podczas tworzenia ołówków, wytapiania metalowych tygli - stosuje się tutaj grafit. Diamenty są używane jako materiały ścierne, biżuteria, dysze do wiertarek itp.
Farmakologia i medycyna są również zaangażowane w wykorzystanie węgla w różnych związkach. Ten element stanowi część stali i stanowi podstawę każdego z nich materia organiczna bierze udział w procesie fotosyntezy itp.
Toksyczność pierwiastka

Struktura atomu węgla zawiera niebezpieczny wpływ na żywą materię. Węgiel przedostaje się do otaczającego nas świata w wyniku spalania węgla w elektrowniach cieplnych, jest częścią gazów produkowanych przez samochody, w przypadku koncentratu węgla itp.
Wysoki procent węgla w aerozolach, co pociąga za sobą wzrost liczby osób. Najczęściej dotyczy to górnych dróg oddechowych i płuc. Niektóre choroby można sklasyfikować jako profesjonalne, na przykład pyłkowe zapalenie oskrzeli i choroby z grupy pylicy płuc.
14 C jest toksyczne, a siła jego oddziaływania jest określona przez radiacyjne oddziaływanie z β-cząstkami. Ten atom jest częścią składu cząsteczek biologicznych, w tym zawartych w kwasach deoksy i rybonukleinowych. Dopuszczalna ilość 14 C w powietrzu obszaru roboczego to 1.3 Bq / l. Maksymalna ilość węgla wchodzącego do organizmu podczas oddychania wynosi 3,2 * 10 8 Bq / rok.