Pojęcie, właściwości i ładunek elektronu
Elektron jest cząstką elementarną, która jest jedną z głównych jednostek w strukturze substancji. Ładunek elektronów jest ujemny. Najdokładniejsze pomiary zostały wykonane na początku XX wieku przez Millikena i Ioffe.
Ładunek elektronów wynosi minus 1,602176487 (40) * 10 -1 9 Cl.
Poprzez tę wartość mierzy się ładunek elektryczny inne małe cząsteczki.

Ogólna koncepcja elektronu
W fizyce cząstek elementarnych mówi się, że elektron jest niepodzielny i niestrukturalny. Zajmuje się procesami elektromagnetycznymi i grawitacyjnymi, należy do grupy leptonów, a także jej antycząstki - pozytonu. Wśród innych leptonów ma najlżejszą wagę. Jeśli zderzają się elektrony i pozytony, prowadzi to do ich anihilacji. Taka para może powstać z cząstek gamma-kwantowych.
Zanim zmierzono neutrina, elektron był uważany za najlżejszą cząstkę. W mechanice kwantowej określa się ją mianem fermionów. Również elektron ma moment magnetyczny. Jeśli pozyton jest również do niego odniesiony, wówczas pozyton jest dzielony jako cząstka naładowana dodatnio, a elektron nazywany jest negatronem, jako cząstka o ładunku ujemnym.
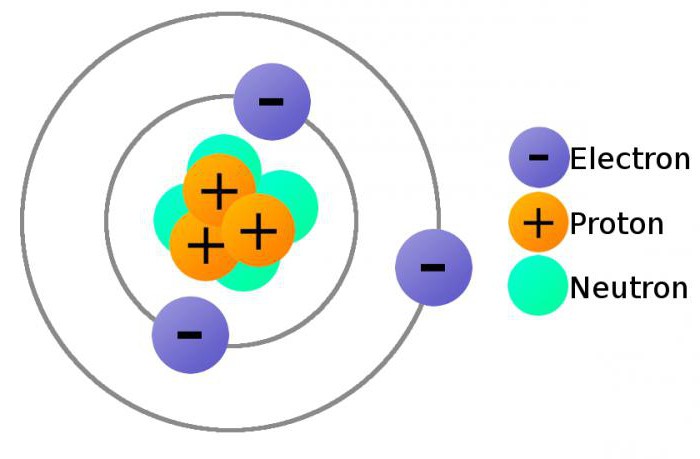
Oddzielne własności elektronów
Elektrony należą do pierwszej generacji leptonów o właściwościach cząstek i fal. Każdy z nich jest obdarzony stanem kwantowym, który określa się mierząc energię, orientację spinu i inne parametry. Przynależność do fermionów ujawnia się przez niemożliwość przebywania w tym samym stanie kwantowym w tym samym czasie, co dwa elektrony (zgodnie z zasadą Pauliego).
Jest on badany w taki sam sposób jak kwazicząstek w okresowym potencjale krystalicznym, w którym efektywna masa może znacznie różnić się od masy w spoczynku.
Poprzez ruch elektronów występuje prąd elektryczny magnetyzm i termoelf. Ładunek elektronu w ruchu tworzy pole magnetyczne. Jednak zewnętrzne pole magnetyczne odchyla cząsteczkę od bezpośredniego kierunku. Podczas przyspieszania elektron nabywa zdolność do absorbowania lub emitowania energii jako fotonu. Jego zestaw składa się z elektronicznych powłok atomowych, których liczba i położenie określa właściwości chemiczne.
Masa atomowa składa się głównie z protonów jądrowych i neutronów, natomiast masa elektronowa Jest rzędu 0,06% całkowitej masy atomowej. Siła elektryczna Coulomba jest jedną z głównych sił zdolnych do trzymania elektronu blisko jądra. Ale kiedy cząsteczki powstają z atomów i powstają wiązania chemiczne elektrony są redystrybuowane w nowo utworzonej przestrzeni.
Pojawienie się elektronów wiązało się z nukleonami i hadronami. Izotopy o właściwościach radioaktywnych mogą emitować elektrony. W warunkach laboratoryjnych cząstki te można badać w specjalnych urządzeniach, na przykład, teleskopy mogą wykrywać promieniowanie z nich w chmurach plazmy.
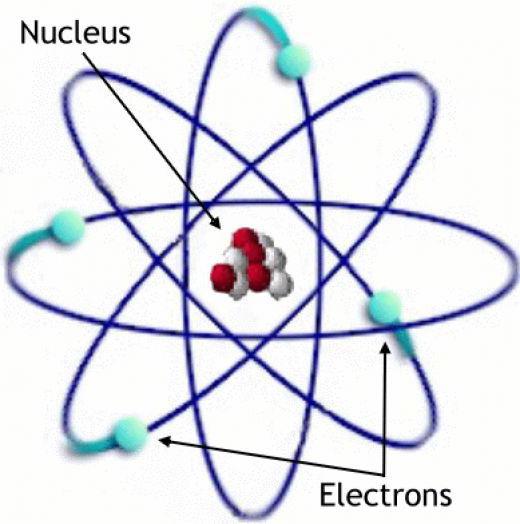
Odkrycie
Elektron został odkryty przez niemieckich fizyków w XIX wieku, kiedy badali właściwości katodowe promieni. Następnie inni naukowcy zaczęli go bardziej szczegółowo badać, dostosowując go do rangi pojedynczej cząstki. Badano promieniowanie i inne powiązane zjawiska fizyczne.
Na przykład grupa kierowana przez Thomsona oszacowała ładunek elektronów i masę promieni katodowych, których związek, jak się dowiedziała, nie zależy od źródła materialnego.
Becquerel odkrył, że minerały same emitują promieniowanie, a ich promienie beta są w stanie odbiegać od działania pola elektrycznego, a masa i ładunek zachowały ten sam stosunek, co promienie katodowe.
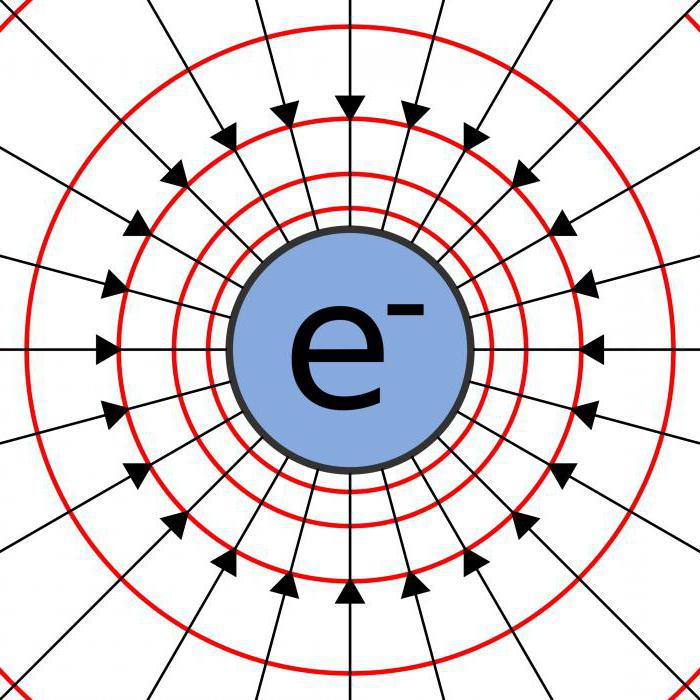
Teoria atomu
Zgodnie z tą teorią atom składa się z jądra i otaczających go elektronów, znajdujących się w jako chmura. Znajdują się one w pewnych skwantowanych stanach energii, których zmianom towarzyszy proces absorpcji lub emisji fotonów.
Mechanika kwantowa
Na początku XX wieku sformułowano hipotezę, zgodnie z którą cząstki materiału mają właściwości zarówno samych cząstek, jak i fal. Światło może również przejawiać się w postaci fali (nazywanej falą de Broglie) i cząstek (fotonów).
W rezultacie sformułowano słynne równanie Schrödingera, w którym opisano propagację fal elektronowych. Takie podejście nazywa się mechaniki kwantowej. Używając jej obliczono stany elektronowe energii w atomie wodoru.
Podstawowe i kwantowe właściwości elektronu
Cząstka wykazuje podstawowe i kwantowe właściwości.
Podstawowe obejmują masę (9 099 * 10-31 kg), elementarny ładunek elektryczny (to znaczy minimalną część ładunku). Zgodnie z dotychczas przeprowadzonymi pomiarami w elektronie nie znaleziono pierwiastków, które mogłyby ujawnić jego podbudowę. Ale niektórzy naukowcy są zdania, że jest to cząstka naładowana punktowo. Jak wskazano na początku artykułu, elektroniczny ładunek elektryczny wynosi -1,602 * 10 -19 Cl.
 Będąc cząstką, elektron może równocześnie być falą. Eksperyment z dwiema szczelinami potwierdza możliwość równoczesnego przejścia przez oba z nich. Jest to w konflikcie z właściwościami cząstki, gdzie za każdym razem możliwe jest przejście tylko przez jedną szczelinę.
Będąc cząstką, elektron może równocześnie być falą. Eksperyment z dwiema szczelinami potwierdza możliwość równoczesnego przejścia przez oba z nich. Jest to w konflikcie z właściwościami cząstki, gdzie za każdym razem możliwe jest przejście tylko przez jedną szczelinę.
Uważa się, że elektrony mają te same właściwości fizyczne. Dlatego ich permutacja, z punktu widzenia mechaniki kwantowej, nie prowadzi do zmiany stanu systemu. Funkcja fal elektronów jest antysymetryczna. Dlatego jego rozwiązania znikają, gdy te same elektrony wpadają w ten sam stan kwantowy (zasada Pauliego).