The Stern Experience - Experimental Confirmation of theory
Zrozumienie, że podstawą struktury jakiejkolwiek substancji jest istnienie najmniejszych cząsteczek - atomów i cząsteczek, które są w ciągłym ruchu i aktywnych interakcji ze sobą - pojawiły się w XIX wieku. Fizyka Rudolf Clausius, Ludwig Boltzmann, a zwłaszcza James Maxwell uczestniczyli w opracowaniu teorii molekularno-kinetycznej na papierze. Wkrótce potem i potwierdzając jej praktyczne badania. Najważniejszym z nich jest doświadczenie Sterna, przeprowadzone w 1920 roku. 
Eksperyment geniuszu
W biografii laureata nagrody Nobla z fizyki (1943) Otto Stern (1888-1969) jest okres, w którym z powodzeniem zaangażował się w teoretyczny rozwój problemów termodynamiki w oparciu o postulaty mechaniki kwantowej. Kierownikiem jego pracy naukowej był kiedyś Albert Einstein. Prawdziwy szacunek ze strony społeczności naukowej przyniósł mu pracę fizyka eksperymentalnego. Opracował unikalne urządzenia, empirycznie potwierdzając i rozwijając teoretyczne obliczenia.
Ad
Oprócz klasycznego eksperymentu do pomiaru prędkości ruchu termicznego cząstek znane jest doświadczenie Sterna-Gerlacha, w wyniku którego udowodniono istnienie spinu - momentu pędu jądra atomowego lub atomu. Eksperyment ten, przeprowadzony w 1922 r. Wraz z Walterem Gerlach (1889-1979), był najważniejszym dowodem podstawowych założeń teorii kwantowej.
Opis urządzenia
Eksperyment z 1920 r., Którego wynikiem był dowód rozkładu prędkości ruchu termicznego cząsteczek, został przeprowadzony przy użyciu technicznie prostego układu. Urządzenie oparte było na dwóch współosiowych (współosiowych) cylindrach o różnych średnicach, wewnątrz których wytworzono obszar niskiego ciśnienia przez pompowanie powietrza. Drut platynowy z cienkim posrebrzeniem znajduje się na wspólnej osi. Kiedy prąd elektryczny jest podłączony do końców przewodu, przewód jest podgrzewany do temperatury powyżej temperatury topnienia srebra. Istnieje parowanie atomów metali, które zaczynają się prostoliniowo jednolity ruch do wewnętrznej powierzchni małego cylindra. 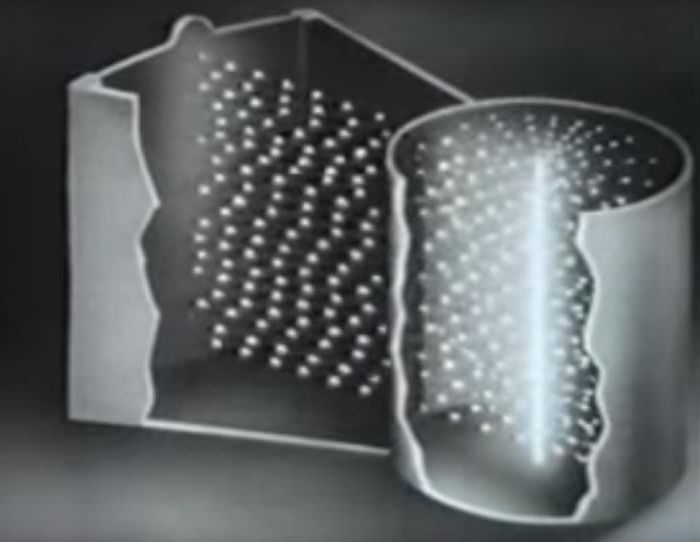
W małym cylindrze przecina się wąska szczelina, przez którą atomy metalu przenikają do dużych. Zewnętrzny cylinder zewnętrzny ma temperaturę pokojową, która zapewnia szybkie chłodzenie ogrzanych cząstek metalu. Jeśli cylindry się nie obracają, atomy "przyklejają się" do ekranu i osiadają przed szczeliną w postaci gładkiego, srebrnego paska. Doświadczenie Sterna było następujące: kiedy oba cylindry zaczęły się obracać z pewnym prędkość kątowa zamazany pasek płytki nazębnej został przesunięty w kierunku przeciwnym do kierunku obrotów.
Ad
Pomiar ruchu molekularnego
Głównym wskaźnikiem, który sprawiał, że doświadczenie Stern jest widoczne, jest prędkość cząsteczek V. Ustalono, że średnia prędkość z którego przemieszczają się atomy srebra podczas odparowywania, gdy spirala jest podgrzewana do 1200 ° C, wynosi od 560 do 650 m / s.
Aby ją zmierzyć, Stern otrzymał wszystkie niezbędne dane:
• S - przesunięcie srebrnego paska podczas obrotu z pozycji zajmowanej w stanie spoczynku;
• L - ścieżka przebyta przez atomy (odległość między wewnętrznymi powierzchniami cylindrów);
• U to prędkość poruszających się punktów na powierzchni zewnętrznego cylindra;
• t jest czasem tranzytu atomów.
Wynik uzyskany doświadczalnie przez niemieckiego fizyka - V = S / U = L / V = UL / S - zbiegł się z wartościami uzyskanymi w wyniku rozważania teorii kinetyki cząsteczkowej. Średnia prędkość ruchu cząsteczek srebra, wyznaczona teoretycznie, wynosiła 584 m / s.  Był to dowód słuszności postulatów sformułowanych przez jej założycieli, w tym znaczące miejsce zajmuje James Maxwell.
Był to dowód słuszności postulatów sformułowanych przez jej założycieli, w tym znaczące miejsce zajmuje James Maxwell.
Prawo dystrybucji Maxwella
Krótko mówiąc, doświadczenie Stern'a można zdefiniować jako wizualizację rozkładu szybkości ruchu termicznego atomów i cząsteczek. Po osadzeniu srebra na ściankach zewnętrznego cylindra, gdy układ jest w spoczynku, otrzymano pasek o wystarczająco ostrych krawędziach. Gdy cylindry się obróciły, wyleciały zamglone. 
Powodem tego jest różnica prędkości ruchu atomów emitowanych podczas odparowywania srebrnej powłoki drutu. Szybsze cząstki zostały osadzone z mniejszym przemieszczeniem ze szczeliny w małym cylindrze, a te, które poruszały się wolniej, pokonały większą odległość. Stosunek prędkości mieści się w proporcji przewidywanej przez obliczenia Maxwella. Krzywa przekroju uzyskanego depozytu pokrywa się w formie z graficzną ekspresją wzorów, które posłużyły za podstawę teorii molekularno-kinetycznej.
Ad
Teoria sprawdzonej praktyki
Ogromne znaczenie fizyki eksperymentalnej, doświadczenie Sterna pokazuje szczególnie wyraźnie. Umiejętność znalezienia sposobu na potwierdzenie poprawności teoretycznych założeń jest szczególnie cenna, gdy przedmioty nierozróżnialne gołym okiem są przedmiotem badań naukowych.
Kolejna historia nauki, kiedy fizyka weszła w fazę badań struktury atomowe w okresie wyszukiwania cząstek elementarnych to udowodnił. Jednym z pionierów nowego trendu był niemiecki fizyk, genialny eksperymentator Otto Stern.