Rodzaje sieci krystalicznych. Rodzaje sieci krystalicznych metali
Podczas przeprowadzania wielu reakcji fizycznych i chemicznych substancja przechodzi w stan skupienia. W tym samym czasie cząsteczki i atomy mają tendencję do osiedlania się w takim porządku przestrzennym, że siły oddziaływania między cząstkami substancji będą możliwie jak najbardziej zbalansowane. Daje to siłę bryły. Atomy, zajmując pewną pozycję, wykonują niewielkie ruchy oscylacyjne, których amplituda zależy od temperatury, ale ich pozycja w przestrzeni pozostaje stała. Siły przyciągania i odpychania równoważą się nawzajem w pewnej odległości.
Współczesne pomysły na temat struktury materii
Współczesna nauka twierdzi, że atom składa się z naładowanego jądra, które przenosi ładunek dodatni, oraz elektronów niosących ładunki ujemne. Przy prędkości kilku tysięcy bilionów obrotów na sekundę elektrony obracają się na swoich orbitach, tworząc obłok elektronu wokół jądra. Dodatni ładunek jądra jest liczbowo równy ładunkowi ujemnemu elektronów. W ten sposób atom materii pozostaje neutralny elektrycznie. Możliwe interakcje z innymi atomami występują, gdy elektrony odrywają się od natywnego atomu, tym samym zakłócając równowagę elektryczną. W jednym przypadku atomy są ułożone w pewnej kolejności, nazywanej siecią krystaliczną. Z drugiej strony, ze względu na złożone oddziaływanie jąder i elektronów, łączą się one w cząsteczki różnego rodzaju i złożoności. 
Definicja sieci krystalicznej
W agregacie różne rodzaje sieci krystalicznych substancji są sieciami o różnej orientacji przestrzennej, w węzłach których znajdują się jony, cząsteczki lub atomy. Ta stabilna geometryczna pozycja przestrzenna nazywana jest krystaliczną siatką materii. Odległość między węzłami pojedynczej komórki krystalicznej nazywana jest okresem tożsamości. Kąty przestrzenne, w których znajdują się węzły komórki, są nazywane parametrami. Zgodnie z metodą budowania ogniw, sieci krystaliczne mogą być proste, skoncentrowane na centrum, skupione na twarzy i skupione na ciele. Jeśli cząstki materii znajdują się tylko w narożnikach równoległościanu, taka siatka nazywana jest prostą. Przykład takiej siatki pokazano poniżej: 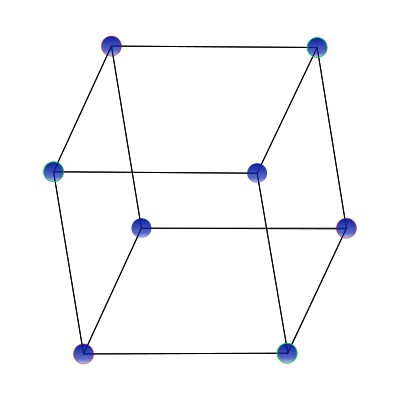
Jeśli oprócz węzłów cząstki substancji znajdują się w środku przestrzennych przekątnych, wówczas taka konstrukcja cząstek w substancji nazywana jest siecią krystaliczną skupioną na ciele. Na rysunku ten typ jest pokazany wizualnie. 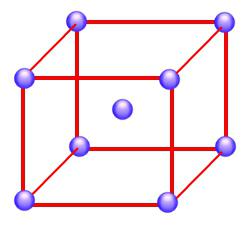
Jeśli oprócz węzłów na wierzchołkach sieci znajduje się węzeł i miejsce, w którym krzyżują się wyimaginowane przekątne równoległościanu, mamy typ siatki kratowej. 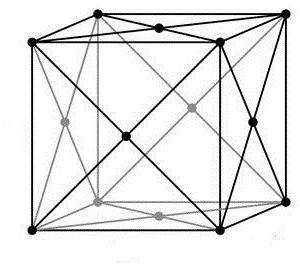
Rodzaje sieci krystalicznych
Różne mikrocząsteczki, które tworzą substancję, określają różne rodzaje sieci krystalicznych. Mogą określić zasadę budowania związku pomiędzy mikrocząstkami wewnątrz kryształu. Fizyczne typy sieci krystalicznych - jonowych, atomowych i molekularnych. Obejmuje to również różne typy siatki krystaliczne metale. Badanie zasad wewnętrznej struktury pierwiastków zaangażowanych w chemię. Rodzaje sieci krystalicznych przedstawiono bardziej szczegółowo poniżej.
Jonowe sieci krystaliczne
Typy danych siatki krystaliczne są obecne w związkach z typem wiązania jonowego. W tym przypadku miejsca sieci zawierają jony o przeciwnym ładunku elektrycznym. Ze względu na pole elektromagnetyczne siły oddziaływania między jonami są dość silne, a to powoduje fizyczne właściwości substancji. Typowymi cechami są ogniotrwałość, gęstość, twardość i zdolność do przewodzenia prądu elektrycznego. Jonowe rodzaje sieci krystalicznych występują w substancjach takich jak sól, azotan potasu i inne. 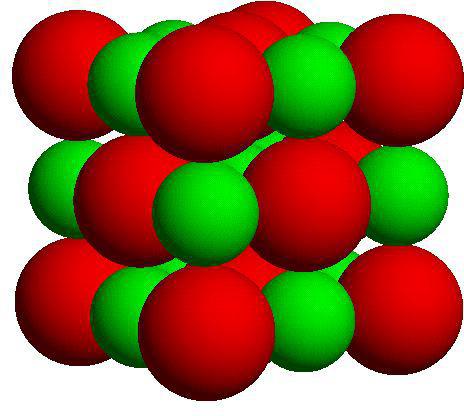
Atomowe krystaliczne kraty
Ten rodzaj struktury substancji jest nieodłączny dla pierwiastków, których struktura jest określona przez kowalencyjne wiązanie chemiczne. Rodzaje sieci krystalicznych tego rodzaju zawierają oddzielne atomy w węzłach, które są ze sobą połączone silnie wiązania kowalencyjne. Podobne wiązanie występuje, gdy dwa identyczne atomy "dzielą się" elektronami, tworząc w ten sposób wspólną parę elektronów dla sąsiednich atomów. Dzięki tej interakcji wiązania kowalencyjne równomiernie i silnie wiążą atomy w określonej kolejności. Pierwiastki chemiczne, które zawierają typy atomowe sieci krystalicznych, mają twardość, wysoką temperaturę topnienia, słabo przewodzą prąd elektryczny i nieaktywne chemicznie. Klasyczne przykłady elementów o podobnej strukturze wewnętrznej to diament, krzem, german i bor.
Sieci molekularne
Substancje o typie molekularnym sieci krystalicznej są układem stabilnych, oddziałujących, blisko upakowanych cząsteczek, które znajdują się w miejscach sieci krystalicznej. W takich związkach cząsteczki zachowują swoje przestrzenne położenie w fazie gazowej, ciekłej i stałej. W węzłach kryształu cząsteczki są utrzymywane przez słabe siły van der Waalsa, które są dziesiątki razy słabsze od sił oddziaływania jonowego. 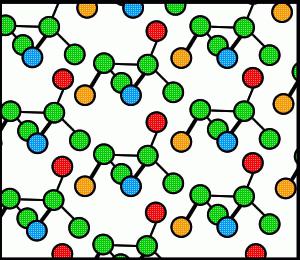
Cząsteczki tworzące kryształ mogą być zarówno polarne, jak i niepolarne. Ze względu na spontaniczny ruch elektronów i oscylacje jąder w cząsteczkach, równowaga elektryczna może się zmieniać - tak powstaje chwilowy elektryczny moment dipolowy. Odpowiednio zorientowane dipole tworzą atrakcyjne siły w sieci. Dwutlenek węgla i parafina są typowymi przykładami pierwiastków o sieci cząsteczkowej.
Metalowe kraty kryształowe
Wiązanie metaliczne jest bardziej elastyczne i plastyczne niż jonowe, chociaż może się wydawać, że oba oparte są na tej samej zasadzie. Rodzaje sieci krystalicznych metali wyjaśniają ich typowe właściwości - takie jak na przykład wytrzymałość mechaniczna, przewodnictwo cieplne i elektryczne oraz topliwość.
Charakterystyczną cechą metalowej sieci krystalicznej jest obecność dodatnio naładowanych jonów metali (kationów) w miejscach tej sieci. Pomiędzy węzłami znajdują się elektrony, które są bezpośrednio zaangażowane w tworzenie pola elektrycznego wokół sieci. Liczba elektronów poruszających się wewnątrz tej sieci krystalicznej nazywana jest gazem elektronowym.  W przypadku braku pola elektrycznego swobodne elektrony wykonują ruch chaotyczny, losowo oddziałując z jonami sieci. Każde takie oddziaływanie zmienia pęd i kierunek ruchu ujemnie naładowanej cząstki. Elektrony w swoim polu elektrycznym przyciągają do siebie kationy, równoważąc wzajemne odpychanie. Chociaż elektrony są uważane za wolne, ich energia nie wystarcza, aby opuścić kratę krystaliczną, więc te naładowane cząstki są zawsze w swoich granicach.
W przypadku braku pola elektrycznego swobodne elektrony wykonują ruch chaotyczny, losowo oddziałując z jonami sieci. Każde takie oddziaływanie zmienia pęd i kierunek ruchu ujemnie naładowanej cząstki. Elektrony w swoim polu elektrycznym przyciągają do siebie kationy, równoważąc wzajemne odpychanie. Chociaż elektrony są uważane za wolne, ich energia nie wystarcza, aby opuścić kratę krystaliczną, więc te naładowane cząstki są zawsze w swoich granicach.
Obecność pola elektrycznego daje dodatkową energię dla gazu elektronowego. Połączenie z jonami w sieci krystalicznej metali nie jest trwałe, więc elektrony łatwo opuszczają swoje granice. Elektrony poruszają się wzdłuż linii energetycznych, pozostawiając za sobą dodatnio naładowane jony.
Wnioski
Chemia przywiązuje dużą wagę do badania wewnętrznej struktury materii. Rodzaje sieci krystalicznych różnych elementów określają prawie całe spektrum ich właściwości. Działając na kryształy i zmieniając ich wewnętrzną strukturę, możliwe jest osiągnięcie poprawy pożądanych właściwości substancji i usunięcie niepożądanych, konwersji pierwiastków chemicznych. Tak więc badanie wewnętrznej struktury otaczającego świata może pomóc poznać istotę i zasady struktury wszechświata.