Jak wygląda formuła aminokwasowa?
Ogólna formuła aminokwasów potwierdza obecność w cząsteczce węgla, wodoru, tlenu, a także zawartość dwóch grup funkcyjnych: grup karboksylowych i aminowych. To oni wyjaśniają amfiteatralny charakter tych związków, dwoistość ich struktury.
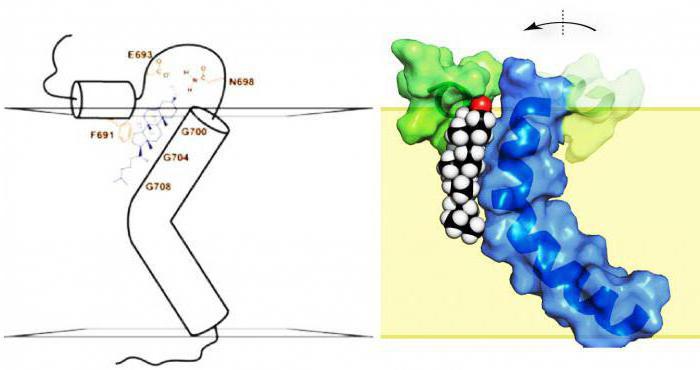
Znaczenie związków
Wszystkie procesy związane z żywotną aktywnością organizmów występują na poziomie molekularnym. Dlatego tak ważne jest pełne zrozumienie cech wszystkich materia organiczna ich właściwości fizyczne i chemiczne.
Rozważmy niektóre aminokwasy, których formuły i imiona są znane nawet współczesnym uczniom.
Przez kilka dziesięcioleci nastąpił gwałtowny rozwój biochemii. Dzięki innowacyjnym metodom badawczym możliwe było wyjaśnienie złożonych przekształceń związanych z syntezą cząsteczek białkowych. Informacje uzyskane w specjalistycznych laboratoriach naukowych są wykorzystywane w przemyśle medycznym, farmaceutycznym.
Ad

Funkcje biochemiczne
Nauka ta bada skład chemiczny organizmów żywych, ich strukturę, transformacje. To właśnie dzięki biochemii uzyskano ogólną formułę aminokwasów, węglowodanów i tłuszczów. Pochodzący z IX wieku, dopiero dziś biochemia stała się sprzymierzeńcem w leczeniu złożonych chorób dziedzicznych.
Właściwości i struktura aminokwasów
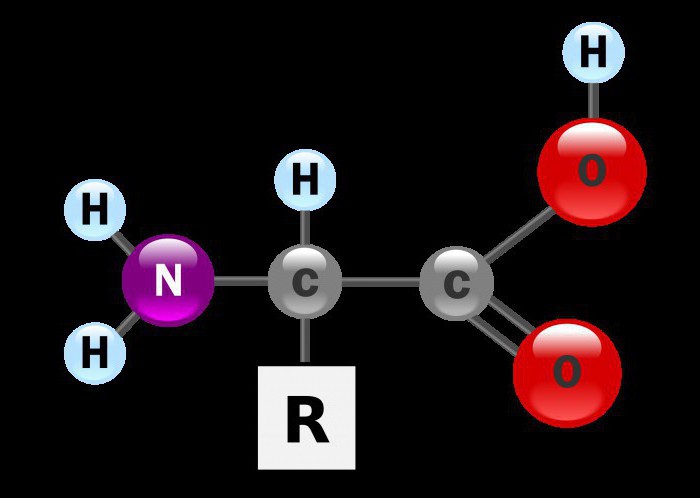
Jakakolwiek formuła aminokwasów jest pochodną amoniaku i kwasu karboksylowego. Obecnie około trzystu przedstawicieli tej klasy znajduje się w dzikiej faunie i florze. Jakakolwiek formuła aminokwasów, niezależnie od charakterystyki łańcucha węglowego, składa się z dwóch grup funkcyjnych. Każdy z nich pozostawia piętno na ogólnych właściwościach chemicznych tych związków. Ogólna formuła aminokwasów to NH2-CH (R) -COOH
Ad
Rodnik, który jest częścią cząsteczki, jest pochodną ograniczającego węglowodoru.
Istnieją wymienialne i niezbędne aminokwasy, ich formuły są rozpatrywane w trakcie chemii organicznej.
Dwadzieścia członków tej klasy jest częścią cząsteczek białek, uważanych za ich zasadniczy składnik strukturalny.
Wśród tych związków, o których powinni wiedzieć absolwenci szkół średnich, są: alanina, prolina, leucyna, glicyna, glutamina, walina, kwas asparaginowy.
Klasyfikacja Amino
W zależności od rodzaju formuły aminokwasowej mogą występować pewne różnice w nazwie. W naszych czasach wyizolowano związki z rodnikami niepolarnymi. Wśród nich należy wybrać alaninę, prolinę, walinę, izoleucynę, tryptofan, fenyloalaninę. Ponadto istnieją aminokwasy, które mają polarne nienaładowane rodniki: serynę, cysteinę, glutaminę, asparaginę.
Standardowe związki są integralnymi składnikami polipeptydowych łańcuchów białkowych, działających jako izomery przestrzenne L. Prawie wszystkie z nich zawierają asymetryczny atom węgla w strukturze, co tłumaczy swobodną przestrzenną rotację aminokwasów.
Te związki są zawarte w komórkach drobnoustrojów, znajdujących się w kompozycji antybiotyków.
Proces wzajemnej transformacji stereoizomerów nazywa się racemizacją. Oprócz standardowych przedstawicieli tej klasy, niestandardowe aminokwasy są również zawarte w cząsteczkach białka.
W zależności od specyfiki cząsteczki białka biorą udział tylko niektóre aminokwasy. Na przykład hydroksyprolina jest obecna w kompozycji kolagenu.
Wszystkie aminokwasy są słabymi elektrolitami, dlatego w roztworze wodnym ulegają tylko częściowej dysocjacji. Zdolność związków do tworzenia jonów polarnych jest używana do analizy obiektów biologicznych w celu zidentyfikowania składu aminokwasów. Odpowiednie do tego są metody, takie jak elektroforeza, chromatografia jonowymienna.
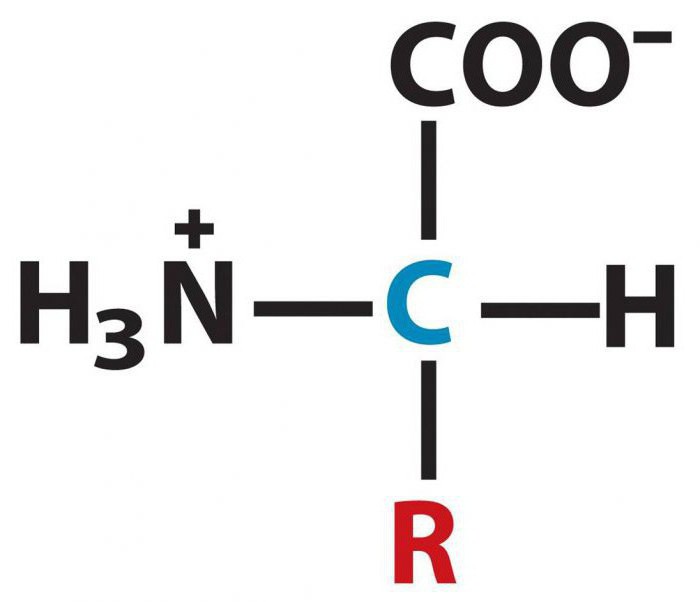
Jest to sekwencja aminokwasowa, która determinuje charakterystykę pierwotnej struktury cząsteczek białka. Wśród głównych obszarów zastosowania tej klasy substancji organicznych można zauważyć zastosowanie w syntezie organicznej, przemyśle farmaceutycznym. Aminokwasy są również stosowane jako pasza dla bydła.