Czym jest atom? Z jakich części składa się i jak mierzy się jego masę?
Współczesny człowiek nieustannie słyszy zwroty, które zawierają pochodne od słowa "atom". To jest energia elektrownia, bomba. Ktoś bierze to za pewnik, a niektórzy zadają pytanie: "Czym jest atom?".
Co oznacza to słowo?
Ma starożytne greckie korzenie. Pochodzi z "atomu", co dosłownie oznacza "niecięte".
Ktoś, już trochę obeznany z fizyką atomu, będzie oburzony: "Jako" niecięty, "Składa się z cząstek!" Chodzi o to, że nazwa pojawiła się, gdy naukowcy wciąż nie wiedzieli, że atomy nie są najmniejszymi cząstkami.
Po doświadczonym dowodzie na to, zdecydowano, aby nie zmieniać zwykłej nazwy. I w 1860 roku "atom" zaczął być nazywany najmniejszą cząstką, która ma wszystkie właściwości pierwiastka chemicznego, do którego należy.
Co jest więcej niż atom i mniej niż to?
Molekuła jest zawsze większa. Powstaje z kilku atomów i jest najmniejszą cząsteczką substancji.
Ale mniej - cząstki elementarne. Na przykład elektrony i protony, neutrony i kwarki. Jest ich dużo.

Wiele rzeczy zostało już powiedziane na jego temat. Ale nadal nie jest jasne, czym jest atom.
Jaki on jest?
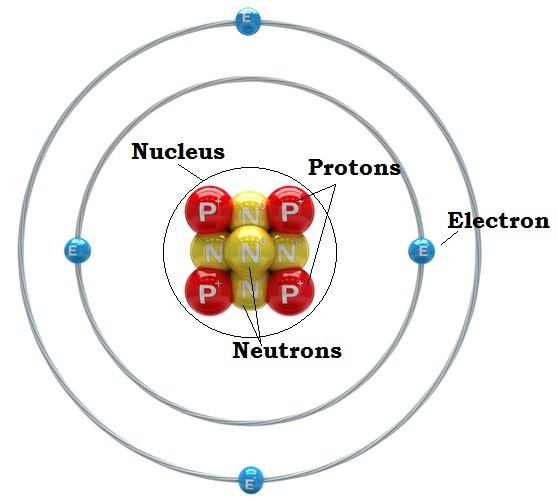
Od dawna naukowcy zajmowali się kwestią tego, jak przedstawić model atomu. Dzisiaj ten, który został zaproponowany E. Rutherford i sfinalizowano N. Bor. Zgodnie z nim atom dzieli się na dwie części: jądro i chmurę elektronową.

Większość masy atomu koncentruje się w środku. Jądro składa się z neutronów i protonów. A elektrony w atomie znajdują się w wystarczająco dużej odległości od środka. Okazuje się, że jest podobny do układu słonecznego. W centrum, podobnie jak słońce, jądro i wokół niego elektrony obracają się w swoich orbitach, podobnie jak planety. Właśnie dlatego model ten jest często nazywany planetarnym.
Co ciekawe, jądro i elektrony zajmują bardzo małą przestrzeń w porównaniu do całkowitej wielkości atomu. Okazuje się, że w centrum małego rdzenia. Następnie pustka. Bardzo duża pustka. A potem wąski pasek małych elektronów.
Do takiego modelu atomów naukowcy nie przybyli od razu. Wcześniej wysunięto wiele założeń, które zostały obalone eksperymentami.
Jednym z tych pomysłów było przedstawienie atomu jako ciała stałego, które ma ładunek dodatni. A elektrony w atomie miały być rozmieszczone na całym ciele. Taki pomysł wysunął J. Thomson. Jego model atomu był również nazywany "Pudding z rodzynkami". Model bardzo przypominał to danie.
Ale było to nie do utrzymania, ponieważ nie potrafił wyjaśnić niektórych właściwości atomu. Dlatego został odrzucony.
Japoński naukowiec, H. Nagaoka, w kwestii tego, czym jest atom, zaproponował taki model. Jego zdaniem, ta cząstka ma dalekie podobieństwo do planety Saturn. W centrum jądra i elektrony krążą wokół niego na orbitach, połączone w pierścień. Pomimo faktu, że model nie został przyjęty, niektóre jego przepisy zostały wykorzystane w systemie planetarnym.
O liczbach powiązanych z atomem
Po pierwsze, o wielkościach fizycznych. Całkowity ładunek atomu jest zawsze zerowy. Wynika to z faktu, że liczba elektronów i protonów w nim jest taka sama. Ich ładunek ma taki sam rozmiar i ma przeciwne znaki.
Często zdarzają się sytuacje, gdy atom traci elektrony lub odwrotnie, przyciąga do siebie zbytecznie. W takich sytuacjach mówi się, że stał się jonem. Jego ładunek zależy od tego, co stało się z elektronami. Jeśli ich liczba zmniejszyła się, ładunek jonów jest dodatni. Kiedy jest więcej elektronów, jon staje się ujemny.

Teraz o chemii. Ta nauka, jak żadna inna, daje najwięcej zrozumienia, czym jest atom. Wszakże nawet główny stół, który jest w nim badany, opiera się na tym, że atomy są ułożone w nim w pewnej kolejności. Mówimy o układzie okresowym.
W nim każdemu elementowi przypisana jest określona liczba, która jest związana z liczbą protonów w jądrze. Zazwyczaj jest to oznaczone literą z.
Kolejną wartością jest liczba masowa. Jest równa sumie protonów i neutronów znajdujących się w jądrze atomu. Jego oznaczenie jest akceptowane literą A.
Te dwie liczby są powiązane ze sobą przez następującą równość:
A = z + N.
Tutaj N to liczba neutronów w jądrze atomowym.
Kolejną ważną ilością jest masa atomu. Do jego pomiaru wprowadzono specjalną wartość. Kurczy się : a.e.m. I czyta się jak atomową jednostkę masy. Przechodząc z tej jednostki, trzy cząsteczki, które składają się na wszystkie atomy wszechświata, mają masy:
| cząstka elementarna | masa w amu |
| proton | 1,0073 |
| neutron | 1,0087 |
| elektron | 0,0005 |
Wartości te są często potrzebne przy rozwiązywaniu problemów chemicznych.