Alkenes: nomenklatura i struktura
Dowiedz się, czym są alkeny. Nomenklatura tej klasy ma pewne charakterystyczne cechy, które należy wymienić bardziej szczegółowo.
Cechy klasy
Przedstawiciele pewnej liczby etylenu mają ustaloną historycznie nazwę - olefiny. Wynika to z faktu, że uważano ich za przodków suszenia oleju (suszenie naturalnych olejów). Ogólną formułą wszystkich przedstawicieli tej serii jest SpN2p. Wśród parametrów wyróżniających wybieramy obecność wiązania podwójnego (nienasyconego).

Specyfikacja nazwy
Międzynarodowy nomenklatur alkenów wymaga użycia specjalnego algorytmu dla nazw olefin. Jaka jest sekwencja działań? Najpierw musisz wybrać najdłuższy łańcuch węglowy w szkielecie węglowym, który obejmuje podwójne wiązanie. Następnie atomy węgla są ponumerowane, począwszy od strony, do której podwójne wiązanie jest najbliższe.
Ad
Algorytm Alkenes
Jeśli są gałęzie (radykały), musisz je określić. Jak to zrobić dobrze? Systematyczna nomenklatura alkenów wskazuje na liczbę, w której znajdują się te cząsteczki. Ponadto należy wziąć pod uwagę strukturę i liczbę rodników. Jeśli w formule występuje kilka identycznych cząsteczek, stosowane są dodatkowe przedrostki: di-, tri-, tetra-, penta-, heksa-.
W obecności różnych rodników ich nazwa jest przeprowadzana z uwzględnieniem alfabetu rosyjskiego. Kiedy nazwiesz łańcuch węglowy, zostanie użyty sufiks -eng. Jakie inne cechy oznacza nomenklatura alkenów? Przykłady homologów etylenu pokazują znaczenie wskazania pozycji podwójnego wiązania w tytule.
Ad
Na przykład dla olefiny kompozycji С4H18 możliwe są dwie formy: buten-1 i buten-2.
Izomeria olefinowa
Jakie izomery mają alkeny? Nomenklatura tych związków jest szczegółowo omawiana w ramach szkolnego kursu chemii organicznej. Biorąc pod uwagę, że cykloalkany i olefiny mają taki sam ogólny wzór (SpN2p), możemy śmiało powiedzieć, że przedstawiciele tych klas węglowodorów są Izomery międzyklasowe. Na przykład, przy składzie jakościowym i ilościowym, wyrażonym wzorem C3H6, może występować cyklopropan i propen. Oprócz tego typu można również uwzględnić strukturę przestrzenną. Isomerism, nomenklatura alkenów w tym przypadku ma pewne cechy. Zakłada się istnienie dwóch konfiguracyjnych izomerów: cis i transview.
W pierwszym przypadku te same podstawniki powinny znajdować się w tym samym regionie symetrii pierwotnej cząsteczki. Transformacja zakłada ich położenie w przeciwległych płaszczyznach. Dla olefin o długich łańcuchach węglowych charakteryzuje się izomerią łańcucha głównego.
Produkcja alkenu
Izomeryzm i nazewnictwo alkenów omówiono powyżej. Teraz dowiedzmy się, jak uzyskać tę klasę nienasyconych węglowodorów. Jako główną metodę przemysłową wytwarzania pierwszych czterech przedstawicieli klasy olefin rozważa się pirolizę i pękanie produktów ropopochodnych. Na przykład pękanie C4H10 przeprowadza się w temperaturze 600 stopni Celsjusza. Mieszanina produktów reakcji zawiera etan, metan, etylen, wodór, propen.
Ad
Wśród innowacyjnych opcji do produkcji olefin, wyróżnimy katalityczne odwodornienie nasyconych węglowodorów, przeprowadzone w podwyższonych temperaturach.

Metody laboratoryjne
W laboratorium najczęstszym sposobem uzyskania przedstawicieli homologicznej serii alkenów jest eliminacja wody z cząsteczek jednowodorotlenowe alkohole. Proces ten prowadzi się ogrzewając alkanol stężonym kwasem fosforowym lub siarkowym.
Specyficzność odwadniania trzeciorzędowych i drugorzędowych końcowych alkoholi można określić za pomocą reguły Zaitseva. Aby utworzyć cząsteczkę wody, wodór jest usuwany z węgla, który jest mniej uwodorniony.
Ponadto olefiny można uzyskać podczas reakcji dehydrohalogenacji. Rozszczepienie cząsteczki fluorowcowodoru następuje, gdy odpowiednia cząsteczka fluorowcopochodna jest eksponowana na alkoholowy roztwór alkaliczny.

Właściwości fizyczne
Jakie są fizyczne właściwości alkenów? Nomenklatura i izomeria zostały rozpatrzone powyżej, teraz skupimy się na cechach fizycznych. Olefiny o składzie C2-C4 w normalnych warunkach są substancjami gazowymi, od pięciu do siedemnastu atomów węgla są cieczami, a następnie są substancjami stałymi.
Wraz ze wzrostem względnego masa cząsteczkowa substancji występuje wzrost temperatury topnienia. Olefiny charakteryzują się minimalną rozpuszczalnością w wodzie. Zwróć uwagę, że w rozpuszczalnikach organicznych znacznie się zwiększa.
Ad
Właściwości chemiczne
Co jeszcze charakteryzuje się alkenami? Nomenklatura klasy pokazuje nieadekwatność ich natury. Dlatego też, jako pierwsza właściwość chemiczna, rozważ uwodornienie (nasycenie wodorem). W trakcie tej reakcji alken przekształca się w odpowiedni nasycony węglowodór. Na przykład, propan powstaje podczas uwodorniania propenu. Jakie są warunki wdrożenia tego procesu? Przystąpienie wodoru przeprowadza się w podwyższonej temperaturze z użyciem katalizatora.
Olefiny, podobnie jak wszystkie inne klasy substancji organicznych, charakteryzują się reakcjami utleniania. W zależności od warunków, w których przeprowadzany jest proces, można uzyskać różne produkty: alkohole, aldehydy, kwasy karboksylowe.
W powietrzu alkeny palą się z uwolnieniem pary wodnej i dwutlenku węgla, a procesowi temu towarzyszy wydzielanie znacznej ilości ciepła.
Wśród specyficznych reakcji, które odróżniają przedstawicieli tej klasy od innych węglowodorów, zauważamy interakcję z roztworem nadmanganian potasu. Produktem tej interakcji są dwuwodorotlenowe alkohole, zwane glikolami.
Twarde utlenianie tej substancji w kwaśnym środowisku w podwyższonej temperaturze prowadzi do całkowitego rozerwania podwójnego wiązania, wytwarzania ketonów lub kwasów.
Zastosowanie alkenów
Przyjrzeliśmy się podstawowym właściwościom, które posiadają alkeny. Nomenklatura, liczba izomerów w przedstawicielach olefin wskazuje na szerokie możliwości ich praktycznego zastosowania.
Są one stosowane w dużych ilościach jako materiały wyjściowe do produkcji organicznych rozpuszczalników: dichloroetanu, alkoholi. Ponadto, poprzez syntezę olefin, wytwarza się związki polimeryczne: poliizobutylen, polichlorek winylu, polietylen.
Ad
Ze względu na zwiększoną aktywność chemiczną ze względu na obecność wiązania podwójnego w cząsteczkach, etylen jest stosowany do wytwarzania alkoholu dwuwodorotlenowego glikolu etylenowego. Jest to produkt niezbędny do wytworzenia syntetycznego lavsanu, produkcji materiałów wybuchowych, produkcji środków przeciw zamarzaniu.
Szczególne miejsce w nowoczesnej produkcji chemicznej zajmuje synteza polietylenu. W procesie polimeryzacji powstaje substancja, która jest podstawą do produkcji paliwa, kauczuku syntetycznego, a także różnych materiałów polimerowych.
Podobny proces zachodzi w podwyższonej temperaturze, stosuje się katalizator. Jeżeli makrocząsteczki polietylenu mają niewielki rozmiar, jest on stosowany jako płynny środek poślizgowy. Gdy liczba jednostek strukturalnych w zakresie od jednego do trzech tysięcy sztuk polietylenu na żądanie w produkcji plastikowych naczyń.
Przynosząc łańcuch o długości do sześciu tysięcy powtarzających się jednostek konstrukcyjnych, wykonuje się rury i różne części. Podczas polimeryzacji propenu powstaje włókno syntetyczne. Chemicznemu procesowi interakcji z chlorkiem etylenu towarzyszy tworzenie chloroetanu, który jest stosowany we współczesnej medycynie jako znieczulenie.
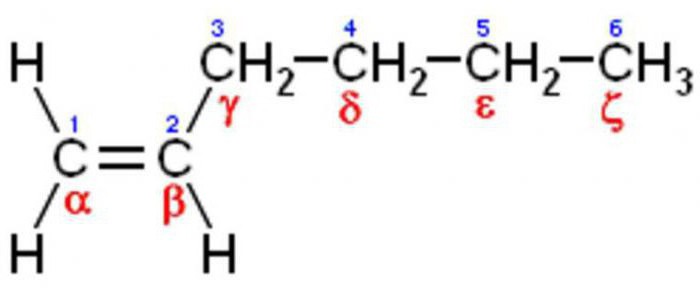
Zdolność olefin do interakcji z cząsteczkami wody znalazła również zastosowanie w przemyśle. W podobny sposób etanol otrzymuje się z etylenu, który jest nie tylko głównym surowcem do produkcji napojów alkoholowych, ale ma również doskonałe właściwości rozpuszczające.
Olefiny są pożądane w przemyśle kosmetycznym, wytwarzanie farb i lakierów, produkcja materiałów wybuchowych, są surowcami do kwasu octowego, aromatyczne węglowodory.