Tlenek azotu: wzór, właściwości, zastosowanie
Tlenki są nazywane dwuskładnikowymi związkami pierwiastków chemicznych z atomem tlenu, w którym stopień utlenienia wynosi 2. Azot, który ma niższą wartość elektroujemną, tworzy różne kombinacje z tlenem. Związki te należą do różnych klas substancji. Tlenek azotu zawiera tlen w ilości, która decyduje o wartościowości pierwiastka N. Jest w zakresie od 1 do 5.
Jakie są tlenki
Istnieje około dwunastu związków azotowych zawierających element O. Spośród nich najczęściej spotykane są: monowalentny tlenek, dwuwartościowy tlenek, trójwartościowy tlenek, czterowartościowy tlenek i pięciowartościowy tlenek. 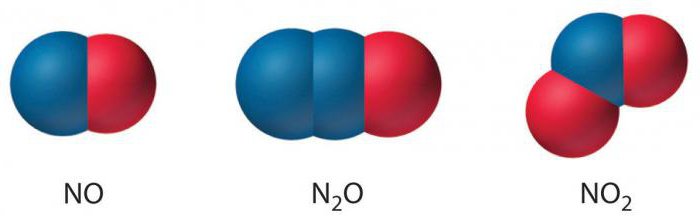
Pozostałe związki uważane są za mniej powszechne. Należą do nich czterowartościowy tlenek azotu w postaci dimeru, niestabilne cząsteczki nitrylozydu, azydku nitrozylu, trinitramidu i rodnik azotanowy.
Wzory tlenków azotu
Poniżej znajdują się oznaczenia najbardziej znaczących związków pierwiastka N.
Jest to przede wszystkim podtlenek azotu, którego formuła składa się z dwóch znaków chemicznych - N i O. Indeksy są umieszczane za nimi, w zależności od stany utleniania atomy.
- Monowalentny tlenek azotu ma wzór N 2 O. W nim atom N jest naładowany +1.
- Tlenek azotu ma wzór NO. W nim atom N jest naładowany +2.
- Azotowy tlenek żelaza ma wzór N 2 O 3 . W nim atom N jest naładowany +3.
- Czterowartościowy tlenek azotu, którego wzór to NO 2 , ma ładunek atomu N + 4.
- Pentawententowy związek tlenu oznaczono jako N2O5. W nim atom N jest naładowany +5.
Opis monowalentnego tlenku azotu
Jest również określany jako diaz, tlenek azotu i gaz rozweselający. Nazwisko pochodzi od działania związanego z odurzaniem. 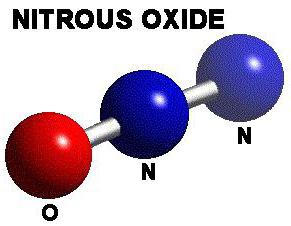
Tlenek azotu o wartościowości I w normalnych warunkach temperaturowych występuje w postaci niepalnego gazu, bezbarwnego, który wykazuje przyjemny słodkawy smak i zapach. Powietrze jest lżejsze niż ten związek. Tlenek jest rozpuszczalny w środowisku wodnym, etanolu, eterze i kwasie siarkowym.
Ad
Roztwory wodne, zasadowe i kwaśne nie są w stanie z nim reagować, nie tworzą soli. Nie podlega zapłonowi, ale jest w stanie wspierać proces spalania.
Amoniak-tlenek azotu przekształca się w azydek (N3NH4).
W połączeniu z cząsteczkami eterów, chloroetanu i cyklopropanu tworzy się mieszanina wybuchowa.
Normalne warunki przyczyniają się do jego bezwładności. Pod działaniem ogrzewania substancja zostaje przywrócona.
Opis tlenku dwuwartościowego azotu
Jest również nazywany rodnikiem monotlenkowym, tlenkowym lub nitrozylowym. W normalnych warunkach temperaturowych jest to bezbarwny, niepalny gaz, słabo rozpuszczalny w środowisku wodnym. Powietrze jest utlenione, okazuje się NIE 2. Jego ciekła i stała postać staje się niebieska. 
Tlenek azotu może być czynnikiem redukującym w reakcjach interakcji z halogenami. Produkt ich addycji jest halogenkiem nitrozylu, który ma wzór NOBr.
Dwutlenek siarki i inne silne czynniki redukujące utleniają NO, tworząc cząsteczki N2.
Opis tlenku żelaza
Są one określane jako bezwodnik nitrowy. W stanie normalnym może to być ciecz o niebieskim zabarwieniu, a standardowe parametry medium przekształcają tlenek w postać gazu, który nie ma koloru. Ma stabilność tylko w niskich temperaturach.
Ad
Cząsteczki N 2 O 3 dysocjują podczas ogrzewania z wydzielaniem mono- i biwalentnego tlenku.
Jako bezwodnik dodaje wodę do wytwarzania kwasu azotowego, az alkaliami tworzy sole w postaci azotynów.
Opis tlenku czterowartościowego azotu
Inaczej nazywa się to dwutlenkiem. Występuje w postaci brązowo-czerwonego gazu, który ma ostry zapach i może być również żółtawym płynem. 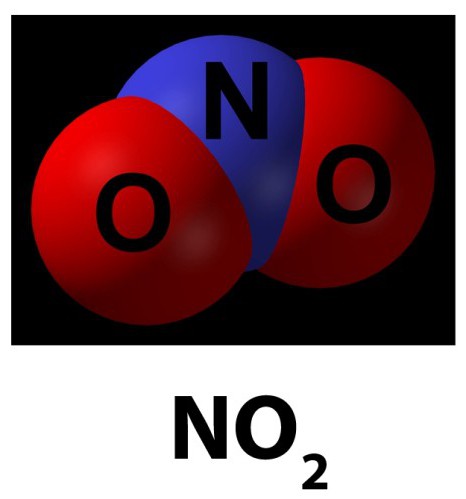
Odnosi się do kwaśnych tlenków, które mają dobrze rozwiniętą aktywność chemiczną.
Jego cząsteczki utleniają niemetale z tworzeniem związków zawierających tlen i wolnego azotu.
Dwutlenek reaguje z czterowartościowym i sześciowartościowym tlenkiem siarki. Okazuje się kwas siarkowy. Metoda jego syntezy nosi nazwę azotawy.
Tlenek azotu można rozpuszczać w środowisku wodnym. Kwas azotowy jest wynikiem tej reakcji. Proces ten nazywa się dysproporcjonowaniem. Za składnik pośredni uważany jest kwas azotowy, który szybko ulega rozkładowi.
Ad
Jeśli rozpuścisz czterowartościowy tlenek azotu w alkaliach, wówczas powstanie roztworów azotanów i azotynów. Możesz użyć jego ciekłej formy do interakcji z metalem, a następnie uzyskujesz bezwodną sól.
Opis pięciowartościowego tlenku azotu
Jest również określany jako pięciotlenek diazotyczny, azotan nitronowy, azotan nitrylu lub bezwodnik nitrowy. 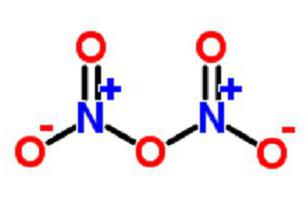
Ma postać bezbarwnych kryształów, które są lotne i niestabilne. Ich stabilność obserwuje się w niskich temperaturach. Struktura ta składa się z jonów azotanów i azotynów.
W postaci gazowej substancja ma postać bezwodnika NO 2- O - NO 2 .
Pentawalentowy tlenek azotu ma właściwości kwasowe. Łatwo ulega rozkładowi wraz z uwolnieniem tlenu.
Substancja reaguje z wodą, w wyniku czego powstaje kwas azotowy.
Alkalia rozpuszczają bezwodnik uwalniając sole azotanów.
Jak zdobyć tlenki azotu
Tlenki azotu powstają, gdy suchy azotan amonu jest stosowany w stanie ostrym, ale tej metodzie może towarzyszyć wybuch.
Korzystnym sposobem otrzymywania monowalentnego tlenku jest działanie kwasu azotowego w stężonej postaci na kwas amidosulfonowy. Głównym warunkiem jest ogrzewanie.
Nitrosyl, czyli NO, to specjalny tlenek azotu, który otrzymuje się w wyniku interakcji cząsteczek N 2 i O 2 . Ważnym warunkiem tego procesu jest silne nagrzanie powyżej 1000 ° C.
Naturalna metoda otrzymywania związana z wyładowaniami atmosferycznymi w powietrzu atmosferycznym. Taki tlenek szybko łączy się z cząsteczkami tlenu i tworzy się dwutlenek.
Laboratoryjna metoda syntezy NO związana jest z reakcją metali i nieskoncentrowanego kwasu azotowego. Przykładem takiej reakcji jest oddziaływanie miedzi z HNO 3 .
Inną metodą wytwarzania tlenku azotu jest reakcja chlorku żelazawego z azotynem sodu i kwasem chlorowodorowym. W wyniku tego procesu powstaje żelazo żelazowe i chlorki sodu, woda i sam tlenek.
Ad
W skali przemysłowej wytwarza się go przez utlenianie cząsteczek amoniaku podczas ogrzewania i pod wysokim ciśnieniem. Akceleratorem procesu jest triwalentny tlenek platyny lub chromu. 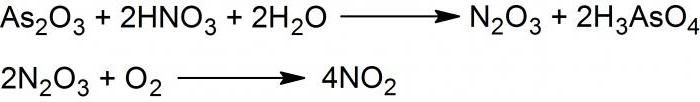
Dwutlenek lub NO2 otrzymuje się w reakcji arsenu z trójwartościowego tlenku z 50% kwasem azotowym, który nanosi się kroplami na powierzchnię stałego odczynnika. Powstaje mieszanina tlenków dwuwartościowego i czterowartościowego azotu.
Jeśli zostanie schłodzony do temperatury -30 ° C, syntezuje się bezwodnik nitrowy lub N203.
W postaci proszku otrzymuje się go w przypadku przepuszczania prądu elektrycznego przez jego gazową postać.
Jeśli proszek skrobiowy zostanie podany za pomocą kwasu azotowego o stężeniu 50%, uwalniany jest tlenek dwuwartościowego i czterowartościowego azotu, dwutlenku węgla i wody. Następnie z dwóch pierwszych otrzymanych związków tworzy się cząsteczka N2O3.
W wyniku rozkładu termicznego ołowiu nitro, dwutlenek azotu, wolny tlen i tlenek ołowiu.
Bezwodnik lub N205 powstaje w wyniku eliminacji cząsteczki wody z kwasu przez działanie azotowe tlenek fosforu pentavalent.
Innym sposobem jego syntezy jest przekazywanie suchego chloru przez bezwodny azotan srebra.
Jeżeli cząsteczki ozonu działają na dwutlenek azotu, powstaje N 2 O 5 .