Ciśnienie osmotyczne w przyrodzie i życiu człowieka
Materiał dostarczony do przeglądu dostarczy informacji na temat ciśnienia osmotycznego (g). Poniżej zostaną rozważone: sformułowanie terminu, cechy i właściwości, metody pomiaru ciśnienia, związek z biologią i związek z rozwiązaniami (pp) różnych typów.
Zapoznanie się z ciśnieniem osmotycznym
Ciśnienie osmotyczne to nadwyżka ciśnienia hydrostatycznego wywieranego na roztwory. Jednocześnie same roztwory powinny być oddzielone półprzepuszczalną membraną z czystych rozpuszczalników. Proces rozpadu dyfuzji przez membranę w takich warunkach nie występuje. Celem tego ciśnienia jest dążenie do uzyskania równomiernej równowagi pomiędzy stężeniami dowolnych roztworów, a środkiem jest spotkanie dyfuzji cząsteczkowej pomiędzy solą i rozpuszczalnikiem. Ciśnienie osmotyczne oznaczone jest literą "π" (pi).
Informacje o właściwościach
Ciśnienie osmotyczne ma zjawisko toniczności, które jest gradientową miarą ciśnienia osmotycznego. Innymi słowy, jest to potencjał różnicy wody w parze rowu oddzielonego półprzepuszczalną membraną. Hipertoniczny roztwór nazwę substancji, która ma w porównaniu z innym roztworem wyższe ciśnienie osmotyczne. Natomiast roztwór hipotoniczny ma niższy wskaźnik osmotyczny.
Jeśli taki roztwór zostanie umieszczony w zamkniętej przestrzeni, na przykład w komórce krwi, wtedy zobaczymy, że ciśnienie osmotyczne może się zepsuć błona komórkowa. Leki wprowadzone do krwi najpierw miesza się z izotonicznym p-rumem, doprowadzając je do rozwiązania właśnie z tego powodu. Dzięki temu chlorek sodu w roztworze powinna być zawarta w ilości zdolnej do równoważenia efektu osmotycznego płynu komórkowego.
Gdyby leki o podanym typie były podawane na bazie wody lub roztworów o wysokim stężeniu, rozkład osmotyczny rozbijałby komórki krwi, zmuszając wodę do wnikania w nie. Tworzenie roztworów przy użyciu zbyt dużych stężeń substancji spowoduje, że woda opuści komórki, w wyniku czego ulegną one skurczeniu. Do tego wystarcza od trzech do dziesięciu procent chlorku sodu w p-re.
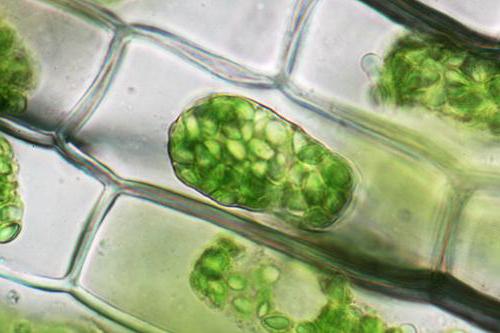
Komórki roślinne, w przeciwieństwie do zwierząt, będą poddane oddzieleniu od ściany komórkowej, całej jej zawartości, za wyjątkiem zewnętrznej ściany komórkowej, ale razem z błoną. Zjawisko to nazywa się plazmolizą. Deplazmolizom z kolei jest procesem obserwowanym podczas przesuwania skurczonych komórek w pp bardziej rozcieńczonego typu.
Związek ciśnienia i rozwiązania
Chemiczny charakter substancji rozpuszczonych w związku nie wpływa na wielkość efektu osmotycznego. Jego szybkość zależy od ilości tych substancji w p-re. Dlatego widzimy, że ciśnienie osmotyczne jest koligatywną właściwością roztworu. Ciśnienie wzrośnie wraz ze wzrostem stężenia substancji czynnych w p-re. Wskazuje na to prawo ciśnienia osmotycznego. Formuła jest dość prosta:
π = i · C · R · T ,
gdzie współczynnik izotoniczny jest oznaczone literą i , molowy poziom stężenia p-ra jest wyrażany przez C (mol / m3), uniwersalny indeks gazu jego stałej jest oznaczony literą R, a T jest poziomem termodynamicznym temperatury p-ra.
Formuła jest podobna do idealnego prawa gazu. Cząsteczki w powietrzu doskonały gaz w środowisku rozpuszczalnika typu lepkiego podobieństwa w ich właściwościach wskazują również na ich wspólne cechy. To stwierdzenie potwierdza szereg eksperymentów przeprowadzonych przez J.B. Perrin w 1906 roku. Obserwował proces rozkładu cząstek emulsji żywicy gummigovoy w słupie wody, która ogólnie była zgodna z prawem Boltzmanna.
Istnieje pojęcie onkotycznego ciśnienia osmotycznego, które zależy od ilości białek w roztworze. W wyniku głodu lub choroby nerek stężenie białek będzie się zmniejszać. Z tego powodu ciśnienie onkotyczne spadnie, a zaczną pojawiać się obrzęki o charakterze onkotycznym. Nastąpi przeniesienie wody z tkanek do naczyń, do miejsc, gdzie π onc więcej Ropne procesy powodują wzrost π onc dwa do trzech razy. Jest to spowodowane zniszczeniem białek, co prowadzi do wzrostu liczby cząstek.
Stabilny wskaźnik osmotyczny powinien wynosić około 7,7 atm. Z tego powodu izotoniczne roztwory zazwyczaj zawierają około π plazmy = 7,7 atm. Rozwiązania z π przekracza π osocza , służy do usuwania ropy z ran lub eliminowania obrzęków o charakterze alergicznym. Są również lekami przeczyszczającymi.
Termodynamiczny widok ciśnienia osmotycznego
Formuła Vant-Hoffa stosowana do leczenia osmotycznego może być uzasadniona z termodynamicznego punktu widzenia.

Energia swobodna , będąc w roztworze, będzie odpowiadała G = G 0 + RTlnx A + π V C. Molowa część roztworu będzie oznaczona jako x A , V C - jest to wskaźnik objętości molowej. Termin πV C jest równoważny wprowadzeniu darmowej energii ciśnienia zewnętrznego. Czysty rozpuszczalnik ma G = G0 . Jeżeli indeks równowagi G rozpuszczalnika odpowiada wskaźnikowi 0, otrzymujemy:
0 = ∇ G = G 0 + RTlnx A + π V C - G 0 = RT lnx A + π V C.
Wynikowy rekord można przekształcić na formułę van't Hoffa.
O roztworach koloidalnych
Ciśnienie osmotyczne roztworu może wystąpić, jeśli występują dwa warunki:
- Wymagana jest półprzepuszczalna przegroda (membrana).
- Obecność dwóch roztworów po obu stronach membrany, podczas gdy roztwory muszą mieć różne stężenia.
Błona komórkowa może przepuszczać cząstki o określonej wielkości, na przykład, przyjmować i uwalniać cząsteczkę wody, ale ma przeciwny wpływ na C 2 H 6 O. Zatem, stosując specjalne materiały, które również mają taką możliwość rozdzielania, możliwe jest oddzielenie różnych składników mieszaniny.
Roztwory osmotyczne są obliczane przy użyciu π = cRT. Ta formuła została wyprowadzona przez Vanta-Hoffa w 1885 roku, a eksperymenty Pfeffera z porowatą porcelaną posłużyły jako podstawa do jej odkrycia.
Turgor w klatce
Zarówno osmoza, jak i osmoza są bardzo ważnymi składnikami wielu systemów biologicznych. Jeśli struktura zawiera półprzepuszczalną przegrodę (specyficzną tkankę lub ścianę komórkową), wówczas stała szybkość osmotyczna wody spowoduje nadmierne ciśnienie hydrostatyczne, w wyniku czego powstanie turgor, który zapewni wytrzymałość i sprężystość tkanek.
Być może zjawisko hemolizy, które jest pęknięciem błony komórkowej, takim jak erytrocyt w wyniku nadmiernego pęcznienia po umieszczeniu w oczyszczonej wodzie.
Plazmoliza
Procesy przeciwne pojawią się, gdy komórka zostanie umieszczona w roztworach soli typu skoncentrowanego: woda zawarta w komórce będzie dyfundować do roztworów soli przez membranę. W wyniku tego komórka kurczy się, tracąc turgor stabilnego stanu. Zjawisko to nazywa się plazmolizą. Jednak turgor można przywrócić, umieszczając komórkę plazmolizowaną w wodzie protoplazmatycznej. Objętość komórek będzie utrzymywana tylko w izotonicznym p-re z tym samym stężeniem (stały osmotyczny).
Podsumowując
Materiał ten pozwolił czytelnikowi zapoznać się z koncepcją leczenia osmotycznego, sformułować ogólną koncepcję i nauczyć się wielu interesujących rzeczy. Na przykład podobieństwo obliczania wzoru z formułą Van't Hoffa, podobieństwo do gazu doskonałego, rola w procesach biologicznych i konsekwencje, które mogą powodować, a mianowicie turgor, plazmoliza, hemoliza i wiele innych.