Kwantowo-mechaniczny model atomu i jego struktura
Planetarny model kwantowy atomu Bohra jest często pamiętany ze względu na schludny i znajomy obraz elektronów. Obracają się wokół centralnego rdzenia, podobnie jak planety wokół Słońca. Z tego powodu może być trudno zastąpić obraz tego, który dokładniej reprezentuje kwantowo-mechaniczny model atomu wykorzystywany przez współczesnych fizyków.
Jak porusza się i porusza atom?
Atom ma małe jądro i fale ostrych orbit. Lokalizacja i ruch elektronów opisuje fale ich materii. Struktury te przewidują prawdopodobieństwo znalezienia elektronu w danym regionie atomu. Ale skąd się wziął kwantowy model atomu Bohra?
Model planetarny zainicjował proces wprowadzania teorii kwantowej do struktury atomu. Bohr przedstawił ideę stanów stacjonarnych, w których atom był stabilny. Przejścia między tymi stanami wyjaśniały istnienie linii widmowych. W przypadku wodoru był w stanie uzyskać poziomy energii:
Ad
- Przejścia między jej poziomami energii odpowiadały liniom widma wodoru.
- Jego model nie był w stanie przewidzieć poziomu energii dla jakichkolwiek innych atomów (chociaż poziomy wodorowopodobnych metali alkalicznych można zbliżyć do prawdy).
Odrębnie, praca Heisenberga i Schrödingera została przeprowadzona w celu wymyślenia sposobów pełniejszego opisu skwantyzowanych poziomów energii atomów.
Analogie Heisenberga i Schrödingera: jak doprowadzili równanie do dowodu fali
Kwantowo-mechaniczny model struktury atomu ma unikalny zestaw właściwości. Heisenberg używał matryc, a Schrödinger opracował równanie falowe, aby udowodnić absolutność różnicy w zachowaniu kwantu. Dualizm cząstek jest bardziej szczegółowo przedstawiony na filmie.
Ad

Równania Schrödingera przedstawiają gęstość prawdopodobieństwa elektronów wokół jądra atomu. Większość definicji teorii kwantowej i mechaniki kwantowej oferuje ten sam opis dla obu. Zasadniczo opisują teorię kwantową, w której zarówno energia, jak i materia mają charakterystykę fal w pewnych warunkach i charakterystykę cząstek w innych.
Aby pomysł stał się jaśniejszy, ludzie zaczęli przeprowadzać eksperymenty w kategoriach obietnicy umysłu.

- Teoria kwantowa sugeruje, że energia przychodzi w osobnych pakietach zwanych kwantami (lub, w przypadku promieniowania elektromagnetycznego, fotonami).
- Teoria kwantowa ma pewien rozwój matematyczny, często nazywany mechaniką kwantową, która oferuje wyjaśnienie zachowania elektronów wewnątrz chmur elektronowych atomów.
Głównymi postanowieniami kwantowo-mechanicznego modelu struktury atomu jest dwoistość fal elektronowych w obłoku elektronowym, która ogranicza naszą zdolność do jednoczesnego pomiaru energii i położenia elektronu.
Ukryte cechy elektronów
Im dokładniej mierzymy energię lub pozycję elektronu, tym mniej wiemy o drugim. Nie możemy dokładnie oznaczyć pozycji i pędu elektronu w tym samym czasie. To uniemożliwia przewidywanie trajektorii cząstki. W związku z tym zachowanie elektronu jest opisane inaczej niż zachowanie cząstek o normalnej wielkości. Musisz wiedzieć:
- Najpowszechniejszym sposobem opisywania elektronów w atomach zgodnie z mechaniką kwantową jest rozwiązanie równania Schrödingera dla stanów energetycznych elektronów w tej chmurze.
- Kiedy elektron znajduje się w tych stanach, jego energia jest jasno określona, a pozycja nie.
- Pozycja jest opisana przez mapę rozkładu prawdopodobieństwa, zwaną orbitą.
Trajektoria, którą zwykle kojarzymy z obiektami makroskopowymi, zastępowana jest przez elektrony w chmurach elektronów, a opisy statystyczne wskazują nie ścieżkę, ale obszar, w którym się znajduje. Ponieważ elektron w chmurze elektronów atomowych determinuje jego zachowanie chemiczne, aby zrozumieć chemię, konieczne jest opisanie konfiguracji elektronów w kluczu kwantowego modelu atomu.
Zasada nieoznaczoności Heisenberga: obszar wewnątrz atomu
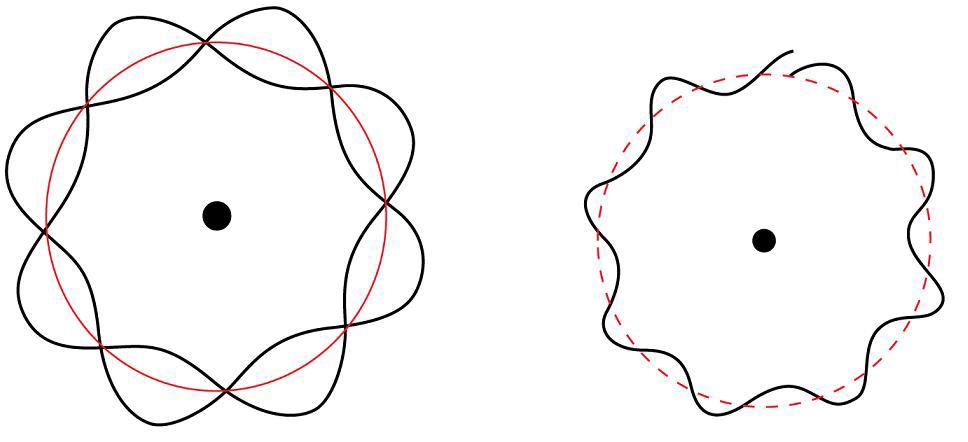
Louis de Broglie zaproponował, że wszystkie cząstki można uznać za fale materialne o długości fali - lambda, zdefiniowanej następującym równaniem:
Lambda = aktualny czas (godzina) + millivolt godzina
Erwin Schrödinger zaproponował kwantowo-mechaniczny model atomu. W skrócie: traktuje elektrony jako fale materii.
Kwadrat funkcji falowej reprezentuje prawdopodobieństwo znalezienia elektronu w danym regionie w obrębie atomu. Orbita atomowa jest określona jako obszar wewnątrz atomu, w którym znajduje się elektron.
Zasada nieoznaczoności Heisenberga stwierdza, że nie możemy znać ani energii, ani pozycji elektronu. Dlatego, kiedy dowiadujemy się więcej o pozycji elektronu, wiemy mniej o jego energii i vice versa. Elektrony mają swoistą własność zwaną spin. Jakiekolwiek dwa elektrony zajmujące tę samą orbitę muszą mieć przeciwne spiny.
Ad
Eter Luminiferous w świecie kwantowym
Natura światła była przedmiotem badań od czasów starożytnych. W XVII wieku Isaac Newton przeprowadzał eksperymenty z soczewkami i pryzmatami. Udowodnił, że białe światło składa się z poszczególnych kolorów tęczy, połączonych ze sobą. Newton wyjaśnił wyniki swojej optyki "korpuskularnym" widokiem światła, w którym światło składało się z strumieni niezwykle małych cząstek poruszających się z dużą prędkością zgodnie z prawami ruchu Newtona. Warto zauważyć:
Christian Huygens wykazał, że zjawiska optyczne, takie jak odbicie i załamanie, mogą być równie dobrze wyjaśnione z punktu widzenia światła, jak fale poruszające się z dużą prędkością przez medium zwane "eterem świetlnym". Przenika całą przestrzeń.
Ad
Na początku XIX wieku Thomas Young wykazał, że światło przechodzące przez wąskie, ściśle rozstawione szczeliny tworzy wzorce interferencji, których nie można wyjaśnić z punktu widzenia cząstek newtonowskich, ale można je łatwo zinterpretować z punktu widzenia fal.
- Później, w XIX wieku, po tym, jak James Clerk Maxwell rozwinął swoją teorię promieniowania elektromagnetycznego i pokazał, że światło jest widoczną częścią ogromnego spektrum fal elektromagnetycznych, widok cząstki światła został całkowicie zdyskredytowany.
Dziś obszary te nazywane są mechaniką klasyczną i klasyczną elektrodynamiką (lub klasycznym elektromagnetyzmem).
Jak postępował pomysł wprowadzania nowych koncepcji w fizyce

Pod koniec dziewiętnastego wieku naukowcy postrzegali świat fizyczny jako złożony z dwóch oddzielnych obszarów:
- materia uformowana z cząstek poruszających się zgodnie z prawami ruchu Newtona;
- promieniowanie elektromagnetyczne składające się z fal kontrolowanych równaniami Maxwella.
Paradoksy doprowadziły do nowoczesnej struktury kwantowo-mechanicznego modelu atomu Schrödingera, który ściśle łączy cząstki i fale na poziomie podstawowym, zwanym dwoistością cząstki falowej, która zastąpiła klasyczny pogląd.
Dyskretna fala Bohra: jak zachowują się widma emisyjne wodoru
Zgodnie z modelem Bohra widma emisyjne różnych pierwiastków zawierają linie dyskretne. Widoczny region widm emisyjnych wodoru można przedstawić za pomocą tabeli.
Ad
| Podstawowa liczba kwantowa | Liczba podpoziomów | Liczba elektronów |
| 1 | 1 | 2 |
| 2 | 2 | 8 |
| 3 | 3 | 18 |
| 4 | 4 | 32 |
Jest to schematyczna reprezentacja kwantów, gdzie znana jest liczba elektronów i poziomów. W życiu w warunkach próżni nie można powiedzieć na pewno, że istnieje granica na podpoziomie, ale nie może być więcej niż 7. Spektrogramy z kwantyfikacją emisji wskazywały Bohra, że elektrony mogą istnieć wewnątrz atomu tylko przy pewnych promieniach atomowych i energiach.

Konstruując model, Bohr wyprowadził równanie, które poprawnie przewidywało różne poziomy energii w atomie wodoru. Model kwantowo-mechaniczny był odpowiedni tylko do reprezentowania tego konkretnego przypadku. Poziomy odpowiadały liniom emisyjnym w widmie substancji.
Model Bohra, który udowodnił jednolektronowy układ wodorowy
Prędkość elektronu na poziomie energetycznym stanu podstawowego wodoru wynosi 2,2 × 10 6 s ÷ m, gdzie s jest długością, m jest masą. Możemy zastąpić stałą, jak również masę elektronową i prędkość w równaniu de Broglie. Ale jednocześnie nie potrafił wyjaśnić struktury elektronowej w atomach, które zawierały więcej niż jeden elektron.
Jeśli przejdziemy do chemii, model kwantowo-mechaniczny atomu wodoru powinien składać się tylko z protonów. Podczas spotkania z elektronami lub neutronami cząstka zaczyna zachowywać się jak fala. W innych przypadkach atomy innej substancji mogą, niezależnie od struktury, zachowywać się jak fale lub cząstki. W skrócie, kwantowo-mechaniczny model atomu wodoru jest materialnym dualizmem fali, ale nie cząstką.
Nakładanie się fal jeden na drugi: w jaki sposób ścieżki przecięcia atomów nie mieszają się
Fale radiowe z telefonu komórkowego, promieniowanie rentgenowskie używane przez dentystów, energia używana do gotowania w kuchence mikrofalowej, promieniowanie cieplne z gorących przedmiotów i światło z ekranu telewizora to wszelkie formy promieniowania elektromagnetycznego, które wykazują falę. Należy pamiętać:
- Fala to oscylacja lub okresowy ruch, który może przenosić energię z jednego punktu przestrzeni do drugiego.
- Potrząsanie końcówką liny przenosi energię z ręki na drugi koniec liny; kamyki wpadające do stawu prowadzą do fal rozchodzących się po powierzchni wody; ekspansja powietrza towarzysząca piorunowi generuje fale dźwiękowe (grzmoty), które mogą płynąć przez kilka mil.
- W każdym z tych przypadków energia kinetyczna jest przenoszona przez substancję (lina, woda lub powietrze), podczas gdy substancja pozostaje na swoim miejscu.
Fale nie powinny ograniczać się do podróży przez materię. Jak pokazał Maxwell, fale elektromagnetyczne składają się z pola elektrycznego, oscylującego w czasie z prostopadłym polem magnetycznym. Są prostopadłe do kierunku ruchu. Fale te mogą przechodzić przez próżnię ze stałą prędkością 2.998 × 108 m / s, gdzie c jest prędkością światła.