Zasada uprzedzenia w rozpadzie promieniotwórczym
Zasada polaryzacji dla rozpadu promieniotwórczego w radiochemii i fizyce jądrowej, która jest również znana jako prawo Soddy-Faience, jest regułą, która determinuje przekształcenie jednego elementu w inny podczas rozpadu radioaktywnego. Wyjaśniono go w 1913 r. Niezależnie przez dwóch naukowców: angielskiego radiochemika Fredericka Soddy'ego i amerykańskiego fizyka-chemika z polskimi korzeniami Casimira Fayansa.
Osiągnięcia Fredericka Soddy'ego w dziedzinie radioaktywności

Soddy, wraz z Rutherfordem, znajduje się w czołówce odkryć radioaktywnych transformacji atomowych. W 1903 r. Soddy odkrył, że rad emituje jądra helu podczas jego rozpadu. Naukowiec ten wykazał również, że atomy tego samego pierwiastka chemicznego mogą mieć różne masy, co doprowadziło go do opracowania koncepcji izotopów. Soddy ustalił zasady usuwania pierwiastków chemicznych podczas rozpadów promieniotwórczych alfa i beta, co było ważnym krokiem w zrozumieniu związku między rodzinami pierwiastków promieniotwórczych.
W 1921 roku otrzymał nagrodę Frederick Soddy Nagroda Nobla w dziedzinie chemii do ważnych odkryć w dziedzinie fizyki pierwiastków promieniotwórczych i do badania natury izotopów.
Dzieła Kazimierza Fayana

Naukowiec przeprowadził ważne badania nad radioaktywnością różnych izotopów i opracował kwantową teorię elektronowej struktury cząsteczek. W roku 1913 Fayans, niezależnie od niego, odkrył zasady przemieszczania, które regulują przekształcanie niektórych pierwiastków w inne w procesie rozpadu promieniotwórczego. Fayans odkrył również nowy pierwiastek chemiczny, protaktinium.
Pojęcie radioaktywności

Przed rozważeniem praw rozpadu promieniotwórczego i zasad przemieszczania, konieczne jest zrozumienie pojęcia radioaktywności. W fizyce słowo to oznacza zdolność jądra niektórych pierwiastków chemicznych do emitowania promieniowania, które ma następujące właściwości:
- zdolność przenikania do tkanek ludzkich, mająca niszczący wpływ;
- zdolność do jonizacji gazów;
- stymulacja procesu fluorescencji;
- przejście przez różne ciała stałe i płynne.
Z powodu tych zdolności to promieniowanie nazywane jest zwykle jonizacją. Charakter promieniowania może być na przykład elektromagnetyczny, Zdjęcia rentgenowskie lub promieniowanie gamma, lub mieć charakter korpuskularny, emisję jąder helowych, protonów, elektronów, pozytonów i innych cząstek elementarnych.
Tak więc radioaktywność jest zjawiskiem obserwowanym w niestabilnych jądrach atomowych, które są spontanicznie zdolne przekształcić się w jądra bardziej stabilnych pierwiastków. Mówiąc prosto, niestabilny atom emituje promieniowanie radioaktywne, aby stać się stabilnym.
Ad
Niestabilne izotopy atomowe
Niestabilne izotopy, czyli atomy tego samego pierwiastka chemicznego, które mają różne masy atomowe, są w stanie wzbudzonym. Sugeruje to, że mają zwiększoną energię, którą starają się dać, aby przejść do stanu równowagi. Biorąc pod uwagę, że wszystkie energie atomu są skwantowane, to znaczy mają dyskretne wartości, to sam rozpad radioaktywny zachodzi z powodu utraty specyficznej energii kinetycznej.

Niestabilny izotop w procesie rozpadu radioaktywnego staje się bardziej stabilny, ale to nie znaczy, że nowo powstałe jądro nie będzie miało radioaktywności, może również ulec rozkładowi. Uderzającym przykładem tego procesu jest jądro uranu-238, które przez kilka stuleci doświadczyło serii rozpadów, przekształcając się ostatecznie w atom ołowiu. Zauważmy, że w zależności od rodzaju izotopu może on ulegać spontanicznemu rozkładowi, na przykład w milionach sekundy i na miliardach lat, na przykład, ten sam uran - 238 ma okres półtrwania (czas, w którym połowa zarodków jąder) wynosi 4,468 miliarda lat, w tym samym czasie dla izotopu potasu-35 okres ten wynosi 178 milisekund.
Różne rodzaje radioaktywności
Zastosowanie konkretnej reguły odchyleń promieniotwórczych zależy od rodzaju rozpadu promieniotwórczego, który występuje w danym elemencie. Ogólnie rozróżnia się następujące rodzaje radioaktywności:
Ad
- rozpad alfa;
- rozpad beta;
- rozpad gamma;
- rozpad z emisją wolnych neutronów.
Wszystkie te typy rozpadu promieniotwórczego (z wyjątkiem emisji wolnych neutronów) zostały ustalone przez fizyka nowozelandzkiego. Ernest Rutherford z powrotem na początku XX wieku.
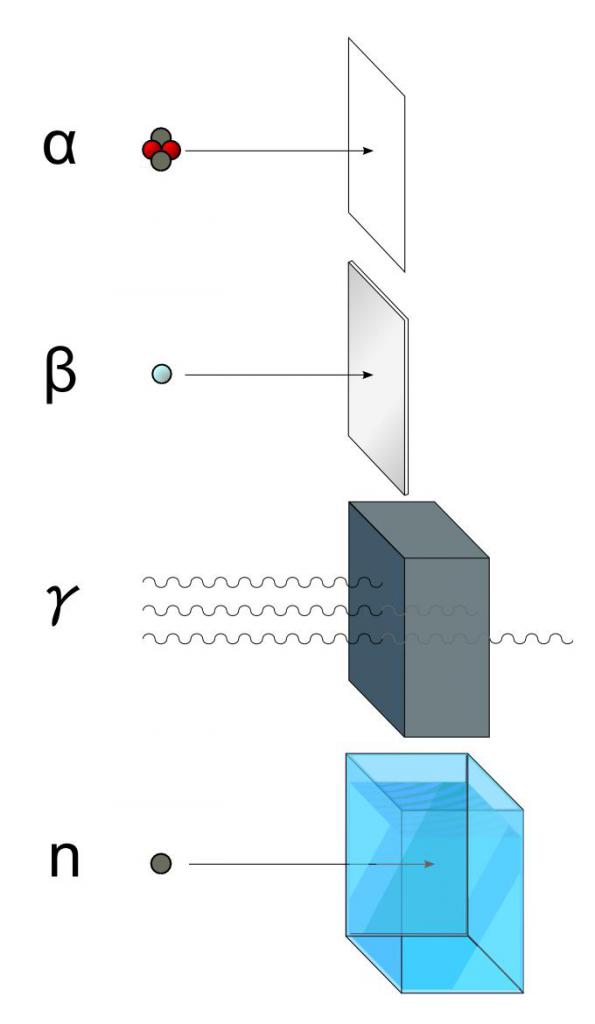
Korpusowe rodzaje rozpadu
Rozpad Alfa wiąże się z emisją jąder helu-4, czyli jest to materia promieniowania korpuskularnego, którego cząsteczki składają się z dwóch protonów i dwóch neutronów. Oznacza to, że masa tych cząstek wynosi 4 w jednostkach masy atomowej (AEM), a ładunek elektryczny wynosi +2 w jednostkach elementarnego ładunku elektrycznego (1 ładunek elementarny w układzie SI jest równy 1,602 * 10-19 C). Emitowane jądro helu przed rozpadem było częścią niestabilnego rdzenia izotopowego.
Naturą rozpadu beta jest emisja elektronów o masie 1/1800 AEM i ładunku -1. Z powodu negatywnego ładunek elektronów ten rozpad nazwano beta-ujemnym. W przeciwieństwie do cząstki alfa, elektron nie istniał przed rozpadem w jądrze atomowym, ale powstał w wyniku przekształcenia neutronu w proton. Ten ostatni pozostał w jądrze po rozpadzie, a elektron opuścił jądro atomowe.
Ad
Następnie odkryto rozpad beta-dodatni, który polega na emitowaniu pozytonu-antycząstki elektronu. Radioaktywny pozyton powstaje w wyniku reakcji odwrotnej niż elektron, to znaczy proton w jądrze zamienia się w neutron, tracąc swój ładunek dodatni.
W serii promieniotwórczych transformacji jednego jądra w drugi emitowane są neutrony o różnych energiach. Podobnie jak proton, neutron ma masę 1 AEM (dokładniej, neutron jest o 0.137% cięższy niż proton) i ma zerowy ładunek elektryczny. Tak więc przy tego typu rozpadzie rdzeń macierzysty traci tylko 1 jednostkę swojej masy.
Zaniki gamma
Zaniki gamma, w przeciwieństwie do poprzednich typów zaniku, mają naturę elektromagnetyczną, tj. Promieniowanie to jest podobne do promieniowania rentgenowskiego lub widzialnego, jednak długość fali promieniowania gamma jest znacznie mniejsza niż w przypadku każdej innej fali elektromagnetycznej. Promienie gamma nie mają masy spoczynkowej i ładunku. W rzeczywistości promieniowanie gamma - to dodatkowa energia, która istniała przed zawaleniem w jądrze atomu, powodując jego niestabilność. Element chemiczny utrzymuje swoją pozycję w układzie okresowym. D.I. Mendelejew z rozpadem gamma.
Ad
Zasady zmiany radia
Korzystając z tych reguł, można łatwo określić, który pierwiastek chemiczny powinien zostać uzyskany z danego macierzystego izotopu o określonym typie rozpadu radioaktywnego. Wyjaśniamy te zasady stronniczości w fizyce:
- W przypadku rozpadu alfa, ponieważ jądro traci 4 masy AEM i +2 jednostki ładunku, powstaje pierwiastek chemiczny, który jest 2 pozycją po lewej stronie w układzie okresowym DI Mendelejewa. Na przykład 92 U 238 = 90 Th 234 , tutaj indeks dolny jest ładunkiem, górny jest masą jądra.
- W przypadku rozpadu beta-ujemnego ładunek jądra macierzystego wzrasta o 1 jednostkę, podczas gdy masa pozostaje niezmieniona (masa elektronu emitowanego podczas tego rozpadu wynosi tylko 0,06% masy protonu). W tym przypadku reguła przesunięcia równowagi określa, że należy utworzyć izotop pierwiastka chemicznego, stojąc po jednej komórce na prawo od macierzyńskiego elementu w tabeli DI Mendelejewa. Na przykład 82 Pb 212 = 83 Bi 212 .
- Zasada wypierania podczas rozpadu beta-pozytywnego (promieniowanie pozytonu) stwierdza, że w wyniku tego procesu powstaje pierwiastek chemiczny, który jest 1 po lewej stronie elementu macierzystego i ma taką samą masę jądra, jak on. Na przykład 7 N 13 = 6 C 13 .