Względna masa atomowa pierwiastka w chemii i historia jego definicji
W procesie rozwoju nauki chemia stanęła przed problemem obliczenia ilości substancji do przeprowadzenia reakcji i substancji uzyskanych w ich przebiegu.
Dzisiaj, dla takich obliczeń reakcji chemicznych między substancjami i mieszaninami, stosuje się wartość względnej masy atomowej wymienionej w układzie okresowym pierwiastków chemicznych DI Mendelejewa.
Procesy chemiczne i wpływ udziału pierwiastka w substancjach w przebiegu reakcji
Współczesna nauka pod definicją "względnej masy atomowej pierwiastka chemicznego" oznacza ile razy masa atomu danego pierwiastka chemicznego jest większa niż jedna dwunasta atomu węgla.
Wraz z narodzinami epoki chemii wzrosło zapotrzebowanie na precyzyjne określenie przebiegu reakcji chemicznej i jej wyników. 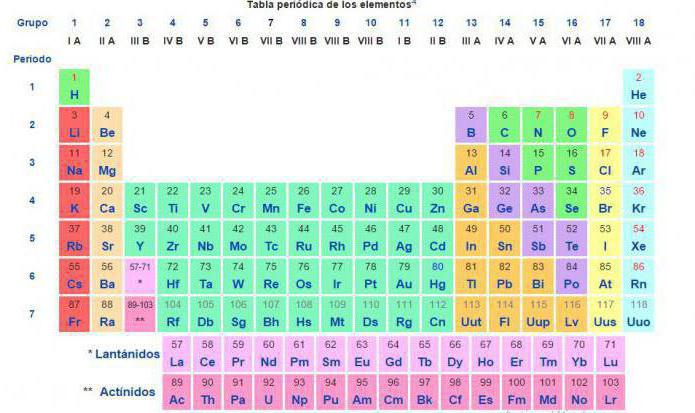 Dlatego chemicy nieustannie próbowali rozwiązać problem dokładnych mas oddziałujących elementów w substancji. Jedna z najlepszych decyzji w tamtym czasie wiązała się z najlżejszym elementem. A waga jego atomu została przyjęta jako jednostka.
Dlatego chemicy nieustannie próbowali rozwiązać problem dokładnych mas oddziałujących elementów w substancji. Jedna z najlepszych decyzji w tamtym czasie wiązała się z najlżejszym elementem. A waga jego atomu została przyjęta jako jednostka.
Historyczny przebieg liczenia substancji
Początkowo używano wodoru, następnie tlenu. Ale ta metoda obliczania była niedokładna. Przyczyną tego była obecność izotopów o masie 17 i 18 w tlenie.
 Dlatego też, mając mieszaninę izotopów, otrzymała technicznie liczbę inną niż szesnaście. Obecnie względna masa atomowa pierwiastka jest obliczana na podstawie wagi atomu węgla przyjętego jako podstawa w stosunku 1/12.
Dlatego też, mając mieszaninę izotopów, otrzymała technicznie liczbę inną niż szesnaście. Obecnie względna masa atomowa pierwiastka jest obliczana na podstawie wagi atomu węgla przyjętego jako podstawa w stosunku 1/12.
Dalton położył fundamenty pod względną masę atomową pierwiastka
Dopiero jakiś czas później, w XIX wieku, Dalton zasugerował obliczenie najlżejszego pierwiastka chemicznego, wodoru. Na wykładach dla swoich uczniów pokazał na figurach wyrzeźbionych z drewna, jak połączone są atomy. W przypadku innych elementów wykorzystał dane wcześniej uzyskane przez innych naukowców.
Według eksperymentów Lavoisiera woda zawiera piętnaście procent wodoru i osiemdziesiąt pięć procent tlenu. Dzięki tym danym Dalton obliczył, że względna masa atomowa pierwiastka, który jest częścią wody, w tym przypadku tlenu, wynosi 5,67. Błąd jego obliczeń wynika z faktu, że błędnie ocenił liczbę atomów wodoru w cząsteczce wody.
Jego zdaniem na jeden atom tlenu przypada jeden atom wodoru. Korzystając z danych chemik Austina, że 20 procent wodoru i 80 procent azotu znajduje się w kompozycji amoniaku, obliczył, jaka jest względna masa atomowa azotu. Z tym wynikiem doszedł do ciekawego wniosku. Okazało się, że względna masa atomowa (formuła amoniaku została błędnie przyjęta z jedną cząsteczką wodoru i azotu) wynosi cztery. W swoich obliczeniach naukowiec polegał na układzie okresowym Mendelejewa. Według analizy obliczył on, że względna masa atomowa węgla wynosi 4,4, zamiast poprzednio przyjętej dwunastki.
 Pomimo poważnych porażek, to właśnie Daltona stworzył stół z pewnymi elementami. Przeszła wiele zmian w życiu naukowca.
Pomimo poważnych porażek, to właśnie Daltona stworzył stół z pewnymi elementami. Przeszła wiele zmian w życiu naukowca.
Składnik izotopowy substancji wpływa na dokładność względnej masy atomowej
Rozważając masy atomowe pierwiastków, można zauważyć, że dokładność każdego elementu jest różna. Na przykład w przypadku litu jest czterocyfrowym, a w przypadku fluoru ośmiocyfrowym. 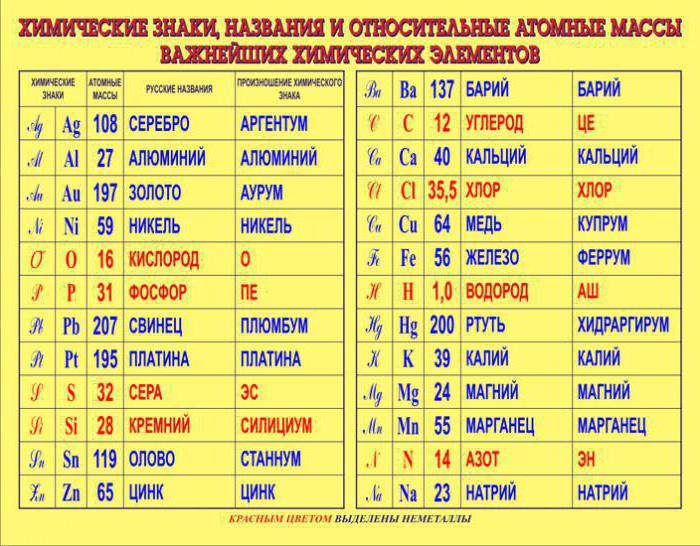 Problem polega na tym, że składnik izotopowy każdego elementu jest jego własnym i niestałym. Na przykład w zwykłej wodzie występują trzy rodzaje izotopów wodoru. Te, oprócz zwykłego wodoru, obejmują deuter i tryt.
Problem polega na tym, że składnik izotopowy każdego elementu jest jego własnym i niestałym. Na przykład w zwykłej wodzie występują trzy rodzaje izotopów wodoru. Te, oprócz zwykłego wodoru, obejmują deuter i tryt.
Względna masa atomowa izotopów wodoru wynosi odpowiednio dwa i trzy. "Ciężka" woda (utworzona przez deuter i tryt) paruje gorzej. Dlatego w stanie parowym izotopy wody są mniejsze niż w stanie ciekłym.
Selektywność żywych organizmów na różne izotopy
Organizmy żywe mają selektywną właściwość w odniesieniu do węgla. Aby zbudować cząsteczki organiczne, stosuje się węgiel o względnej masie atomowej równej dwanaście. Dlatego substancje pochodzenia organicznego, a także pewna liczba minerałów, takich jak węgiel i ropa, zawierają mniej składnika izotopowego niż materiały nieorganiczne.
Mikroorganizmy, które przetwarzają i gromadzą siarkę, pozostawiają izotop siarki 32. W obszarach, gdzie bakterie nie przetwarzają, proporcja izotopu siarki wynosi 34, to jest znacznie więcej. Właśnie na podstawie stosunku siarki w skałach gleby geolodzy dochodzą do wniosku o naturze pochodzenia warstwy - czy to natury magmatycznej, czy sedymentacyjnej.
Ze wszystkich pierwiastków chemicznych tylko jeden nie zawiera izotopów - fluoru. Dlatego jego względna masa atomowa jest dokładniejsza niż inne elementy.
Istnienie w przyrodzie niestabilnych substancji
Niektóre elementy mają względną masę w nawiasach kwadratowych. Jak widać, są to elementy położone po uranie. Faktem jest, że nie mają one stabilnych izotopów i rozpadają się wraz z uwolnieniem promieniowania radioaktywnego. Dlatego najbardziej stabilny izotop jest wskazany w nawiasach. 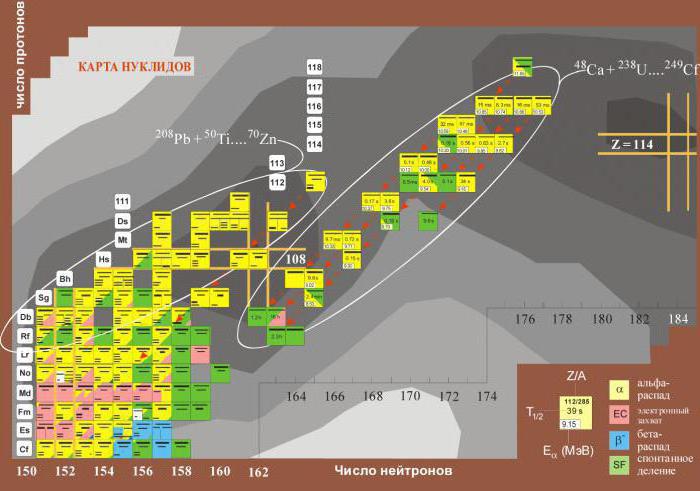 Z czasem okazało się, że niektóre z nich mogą mieć stabilny izotop w sztucznych warunkach. Konieczna była zmiana masy atomowej niektórych pierwiastków transuranowych w układzie okresowym Mendelejewa.
Z czasem okazało się, że niektóre z nich mogą mieć stabilny izotop w sztucznych warunkach. Konieczna była zmiana masy atomowej niektórych pierwiastków transuranowych w układzie okresowym Mendelejewa.
W procesie syntezy nowych izotopów i pomiaru długości życia czasami można było wykryć nuklidy o okresie półtrwania wynoszącym miliony razy dłużej.
Nauka nie stoi w miejscu, nowe elementy, prawa, wzajemne relacje różnych procesów w chemii i przyrodzie są ciągle odkrywane. Dlatego w jakiej formie chemia i okresowy układ pierwiastków chemicznych Mendelejewa pojawią się w przyszłości, za sto lat, jest niejasna i niepewna. Ale chcę wierzyć, że dzieła chemików zgromadzone w ciągu ostatnich stuleci będą służyć nowej, doskonalszej znajomości naszych potomków.