Jaką formułę ma kwas jabłkowy i jak ją zdobywasz?
Drugim nazwiskiem kwasu jabłkowego jest hydroksyntar. Jest członkiem grupy kwasów hydroksykarboksylowych. Związek ten najpierw uzyskał Karl Scheele (szwedzki chemik) z niedojrzałych jabłek (które określiło jego nazwę) w 1785 roku. Również w przyrodzie występuje w winogronach, berberysach, jarzębach, malinach itp. W postaci soli, zwanych jabłkami, substancja jest zawarta w tytoniu. Maksymalna zawartość kwasu hydroksycyklowego razem z kwasem cytrynowym w niedojrzałych zielonych jabłkach osiąga 1,2%.

Kwas jabłkowy: Formuła
Ten związek chemiczny ma następującą formułę:
HOOC-CH 2 -CH (OH) - COOH lub C 4H 3O 2 (OH) 3
W normalnych warunkach kwas jabłkowy jest bezbarwnym krystalicznym proszkiem, który dobrze rozpuszcza się w alkoholu (w 100 ml - 35,9 g) iw wodzie (w 100 ml - 144 g). Masa cząsteczkowa związki równe 134,1 g / mol.
Ad
Poniższy rysunek pokazuje przestrzenną strukturę cząsteczki kwasu jabłkowego. Atomy węgla są zaznaczone na czarno, tlen na czerwono, wodór na biel.
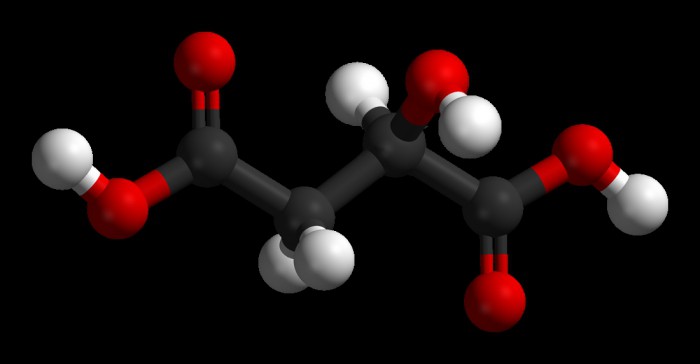
Kwas jabłkowy istnieje w postaci racematu (optycznie nieaktywnego związku) i dwóch stereoizomerów. Te ostatnie są takimi związkami w cząsteczkach, których między atomami występuje ta sama sekwencja wiązań chemicznych, ale istnieją różnice w ich rozmieszczeniu w przestrzeni względem siebie. Szczegółowo ten problem dotyczy stereochemii. W kwasie jabłkowym są dwa stereoizomery, na ich przykładzie P. Walden jako pierwszy pokazał w 1896 r., Że możliwe są interkonwersje enancjomerów. Badanie tego zjawiska posłużyło za podstawę do późniejszego stworzenia teorii reakcji tzw. Substytucji nukleofilowej na atomie węgla (nasyconym).
Ad
Pierwsze
Substancja jest otrzymywana na dwa sposoby: naturalny i chemiczny. Pierwsza oferuje ekstrakcję z owoców i jagód. Syntetyczny kwas jabłkowy otrzymuje się w kilku reakcjach:
1. Hydratacja kwasu maleinowego lub fumarowego. Warunkiem jest temperatura 100-150 ° C. Równanie reakcji wygląda następująco:
HOOCCH = CHCOOH + H2O → NOEP-CH 2 -CH (OH) - COOH
2. Hydroliza kwasu bromo- lub chloro-bursztynowego. Kwas jabłkowy ekstrahuje się za pomocą eteru. Wykorzystuje materiał roślinny.
Kwas jabłkowy. Reakcje interakcji

1. Utlenianie kwasu siarkowego stężonego (H2SO4) z utworzeniem kwasu kumalinowego. Reakcja przebiega w dwóch etapach:
HOOC-CH 2 -CH (OH) - COOH + H 2 SO 4 → HOOC-CH 2- CHO + HCOOH
Rezultatem jest malonowy aldehyd i kwas mrówkowy. Ten ostatni związek rozkłada się tworząc tlenek węgla i woda:
HCOOH → CO + H2O
Aldehyd kwasu malonowego natychmiast przekształca się w kwas kumalinowy.
2. Interakcja z kwas chlorowodorowy :
HOOC-CH 2 -CH (OH) - COOH + HCI → HOOC-CH2-CHCl-COOH
Otrzymana substancja nosi nazwę 2-chloroantynę.
3. Kwas jabłkowy jest podatny na utlenianie (w szczególności, gdy stosuje się KMnO4):
HOOC-CH2-CH (OH) - COOH + KMnO4 → HOOC-CH2-CO-COOH
Powstały kwas nazywany jest 2-okso-bursztynowym (oksylooctowym).
4. Interakcje z chlorkiem acetylu z wytworzeniem kwasu 2-acetoksybursztynowego:
HOOC-CH 2 -CH (OH) - COOH + CH3COCl → HOOC-CH2-CH (OCOCH3) -COOH
Przy stopniowym ogrzewaniu kwas jabłkowy rozkłada się, tworząc serię produktów pośrednich. W temperaturze 100 ° C dochodzi do powstawania bezwodników (są one podobne do laktydów). Przy wzroście do 140-150 ° C przekształca się w kwas fumarowy. Przy gwałtownym wzroście temperatury do 180 ° C otrzymuje się bezwodnik maleinowy.
Ad
Podsumowując wszystkie dane, można powiedzieć, że właściwości chemiczne kwasu jabłkowego są takie same jak innych kwasów hydroksylowych.
Rola biologiczna
Kwas jabłkowy uczestniczy w cyklu Krebsa. Reprezentuje on główny etap oddychania wszystkich komórek, które zużywają tlen i jest pośrednim ogniwem między glikolizą a elektrycznym łańcuchem transportowym. Główną rolą cyklu kwasu trójkarboksylowego (Krebsa) jest synteza zredukowanych koenzymów FAD * H 2 i NAD * H. Są one następnie wykorzystywane do produkcji ATP, ADP i fosforanów. Kwas hydroksykwasowy powstaje w wyniku hydratacji fumarami. Jego późniejsze utlenianie za pomocą NAD + kończy cykl Krebsa. Katalizatorem enzymu jest dehydrogenaza jabłczanowa.

Kule użytkowania
Uzyskany komercyjnie kwas jabłkowy jest dość szeroko stosowany:
- W przemyśle spożywczym znany jest pod kodem E296. Substancja stosowana jako środek konserwujący. wzmacniacz smaku i regulator kwasowości. Główne zastosowanie: napoje gazowane, soki owocowe, wyroby cukiernicze, wino, żywność w puszkach. Warto podkreślić, że w niewielkich ilościach kwas jabłkowy ma pozytywny wpływ na organizm.
- W kosmetologii. Kwas Oxycytic ma właściwości przeciwutleniające, wybielające, złuszczające i nawilżające, dzięki czemu może być stosowany jako część antycellulitowych i wybielających, peelingów. Ponadto dodaje się go do past do zębów i produktów do pielęgnacji jamy ustnej.
- W farmakologii kwas jabłkowy (wzór podany powyżej) jest stosowany w kompozycji wykrztuśnych i przeczyszczających.