Co oznacza topnienie w fizyce? Definicja, wzór
Cała materia obserwowana w naturze istnieje w 3 stanach: gazowym, płynnym i stałym. Obecność substancji w określonym stanie zależy od jej właściwości fizykochemicznych, a także od warunków zewnętrznych. W artykule szczegółowo omówiono proces przejścia materii ze stanu stałego do ciekłego, to znaczy, że zawiera on szczegółową odpowiedź na pytanie: "Co to jest topnienie?".
Cechy struktury ciał stałych i cieczy

Przed udzieleniem odpowiedzi na pytanie, czym jest topnienie, należy wziąć pod uwagę cechy strukturalne ciał stałych i cieczy.
Te pierwsze charakteryzują się obecnością stałej formy, której oporność opiera się. Ciała stałe mają elastyczność, brak płynności. Odległości między cząstkami tworzącymi ciało stałe są małe, a siły wiążące pomiędzy tymi cząsteczkami są znaczące w porównaniu do tych dla cieczy i gazów. Siły wiążące w ciałach stałych mogą mieć inną naturę chemiczną (van der Waals, metaliczny, kowalencyjny, jonowy). Istnieją dwa sposoby organizowania brył:
- struktury krystaliczne, gdy atomy lub cząsteczki ciała znajdują się w określonych pozycjach w przestrzeni, na przykład metale;
- bezpostaciowe struktury, w których atomy lub cząsteczki są rozmieszczone chaotycznie, na przykład szkło.
W cieczach atomy i cząsteczki znajdują się dalej od siebie niż w ciałach stałych, więc są słabiej związane. Płyn zachowuje swoją objętość w danych warunkach, ale nie zachowuje swojego kształtu i ma dobrą płynność. Cząstki płynu są rozmieszczone losowo względem siebie.
Ważnym punktem, na który należy zwrócić uwagę, jest to, że atomy lub cząsteczki w ciele stałym znajdują się w pewnych pozycjach, które bardzo wolno się zmieniają (na przykład w procesach dyfuzji), ale cząsteczki płynów nieustannie przeskakują z jednej pozycji do drugiej.
Energia kinetyczna i potencjalna
Aby zrozumieć, czym jest topnienie w fizyce, konieczne jest jasne zrozumienie proporcji energii kinetycznej i potencjalnej w ciałach stałych i cieczach.
Energia potencjalna charakteryzuje pracę, którą należy poświęcić na rozpylenie danego ciała w przestrzeni na jej cząstki składowe. Aby opisać tę ilość, wprowadza się pojęcie energii wiążącej, co oznacza pracę niezbędną do oderwania jednego atomu lub cząsteczki od ciała i usunięcia go / nieskończoności. Na przykład, typowe wartości energii wiążącej dla ciał stałych to kilka woltów elektronowych, te same wartości dla cieczy są o rząd wielkości mniejsze.
Energia kinetyczna charakteryzuje intensywność ruchu atomów i cząsteczek. W przypadku mediów skondensowanych ta energia jest wprost proporcjonalna do temperatury.
W ciałach stałych energia kinetyczna w temperaturze pokojowej wynosi kilka setnych części napięcia elektronowego, czyli jest 100 razy mniejsza niż potencjał. Atomy i cząsteczki w ciałach stałych znajdują się w studni potencjału i oscylują wokół stabilnych określonych pozycji. Mogą wydostać się z tych pozycji, jeśli fluktuacje energii kinetycznej okażą się znaczące, lub jeśli sama studnia potencjału jest mała, na przykład, gdy w pobliżu jest jakaś wada.
Energia kinetyczna atomów i cząsteczek w cieczy jest w przybliżeniu równa ich potencjalnej energii, to jest jest to kilka dziesiątych woltów elektronowych w temperaturze pokojowej. Oznacza to, że każda cząstka tworząca płyn stale przeskakuje z jednego miejsca do drugiego. Dobrym tego dowodem jest ruch Browna.
Oznaczanie procesu topienia

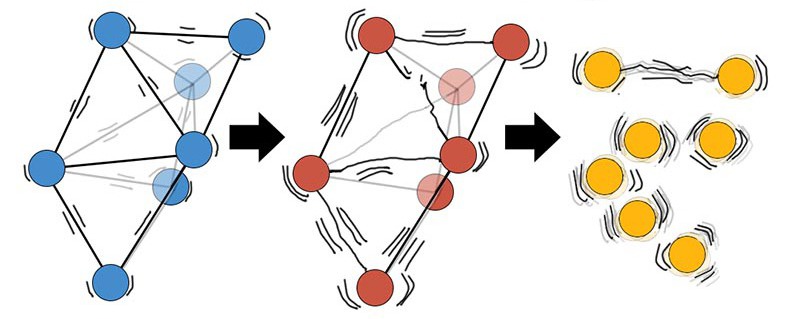
Co oznacza topnienie w fizyce? Definicję tego zjawiska można podać w następujący sposób: topienie to przejście ze stanu stałego do ciekłego substancji w wyniku wzrostu jej temperatury. Oznacza to, że jeśli ciało stałe jest stale podgrzewane, wówczas cząsteczki lub atomy, które go tworzą, zaczynają zwiększać swoją energię kinetyczną. I tak się dzieje do ta energia nie równa się energii wiązania, po której częstotliwość skoków atomów (cząsteczek) znacznie wzrasta, a stały materiał zaczyna się topić.
Żywymi przykładami topienia są procesy topienia lodu lub przejścia do stanu stopionego metalu lub stopu.
Topienie - przejście fazowe pierwszego rodzaju

Zgodnie z definicją topienie jest przejściem pierwszego rodzaju, ponieważ pochłania ciepło. W tym przypadku temperatura całego układu nie zmienia się podczas procesu topienia i jest wartością stałą. Fakt ten tłumaczy się tym, że ciepło dostarczane do ciała nie jest wydawane na zwiększanie energii kinetycznej atomów i cząsteczek, ale na przełamywanie silnych wiązań chemicznych między nimi. Dopiero po zniszczeniu wszystkich wiązań w ciele dalsze doprowadzanie ciepła do już ciekłej substancji prowadzi do wzrostu jej temperatury.
Sam proces topienia nie pojawia się spontanicznie, ale rozwija się w pewnym okresie czasu, gdy fazy ciekłe i stałe współistnieją w równowadze ze sobą.
Tak więc topienie jest procesem endotermicznym, co oznacza, że pochodzi z absorpcji ciepła. Odwrotny proces, w którym ciecz zestala się, nazywa się krystalizacją.
Temperatura topnienia
Jak wspomniano powyżej, topienie zachodzi w określonej temperaturze, która jest nazywana temperaturą topnienia. Od czego zależy ta fizyczna ilość? Po pierwsze, od energii wiążącej cząstek tworzących ciało stałe, im wyższa energia, tym wyższa temperatura topnienia. Na przykład ogniotrwały metal niobowy topi się w temperaturze 2742 K, a energia wiązania na atom tego metalu wynosi 7,6 eV, inny ogniotrwały metal jest wolframem, ma energię wiązania 8,9 eV i topi się w znacznie wyższej temperaturze 3695 K.
Po drugie, temperatura topnienia zależy od warunków zewnętrznych. W szczególności wraz ze wzrostem ciśnienia wzrasta również.
Po trzecie, ta wartość dla tej substancji jest silnie uzależniona od zanieczyszczeń. Z reguły zanieczyszczenia prowadzą do niższej temperatury topnienia.
Ciepło fuzji
Przejdujemy teraz od definicji topnienia do formuły opisującej ilościowo ten proces. Kiedy następuje topienie, zewnętrzne źródło ciepła zużywa się na rozerwanie wiązań w ciele stałym i przeniesienie go do stanu ciekłego. Energia, która musi zostać wydatkowana, aby pewna ilość ciała stałego w punkcie topnienia zmieniła się w stan ciekły zwany ciepłem termojądrowym. Wzór w tym przypadku jest zapisany w następujący sposób: λ = Q / m, gdzie Q to ilość ciepła, m to masa ciała.
Wartość ciepła topnienia λ zależy od właściwości fizykochemicznych materiału. Na przykład dla lodu wartość ta wynosi 333,55 J / g lub 6,02 kJ / mol, a dla żelaza 13,81 kJ / mol. Wartości podaje się pod ciśnieniem 1 atmosfery.
Topienie kryształów
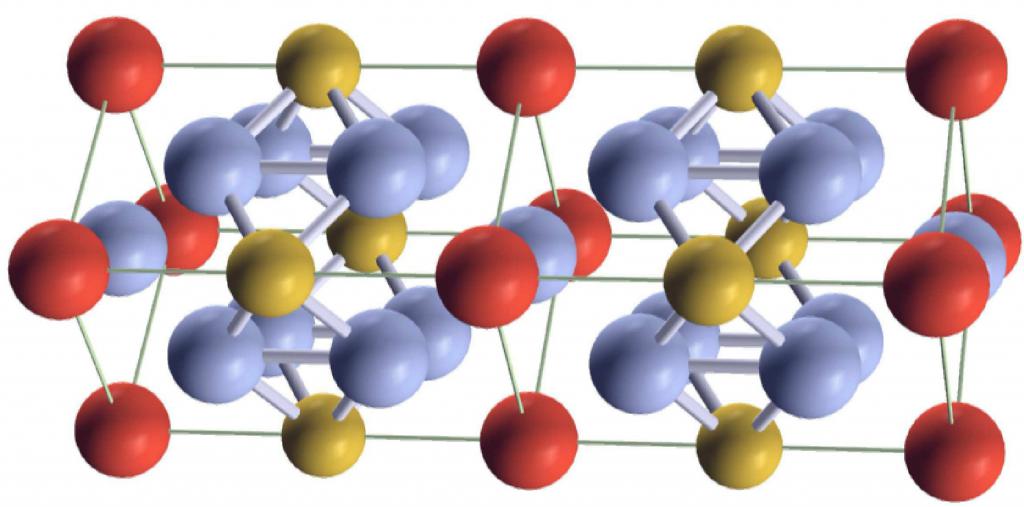
Te ciała stałe reprezentują specyficzne przestrzenne ułożenie cząstek, które je tworzą. Jest znany jako sieć krystaliczna. Istnieje wiele różnych sieci krystalicznych, z których każda jest realizowana w pewnej klasie substancji. Na przykład, metale istnieją z reguły w postaci bcc (sześciennych) i fcc (sześciennych). Pojęcie temperatury topnienia obowiązuje tylko dla kryształów.
Topienie bezpostaciowych ciał

Ponieważ atomy (cząsteczki) są losowo ułożone w amorficzne materiały, energie wiązania między nimi będą różne. Fakt ten tłumaczy, dlaczego nie ma określonego punktu topienia dla materiałów amorficznych, a sam proces topnienia zachodzi w zakresie temperatur, który z reguły wynosi kilkadziesiąt stopni.