Kryształowe i amorficzne ciała: struktura i właściwości
Istnieje kilka stanów skupienia, w których znajdują się wszystkie ciała i substancje. To jest:
- gaz;
- płynny;
- osocze;
- solidny.
Jeśli weźmiemy pod uwagę całkowitą populację planety i kosmosu, większość substancji i ciał nadal znajduje się w stanie gazowym i plazmowym. Jednak na samej Ziemi istotna jest również zawartość cząstek stałych. Tutaj porozmawiamy o nich, sprawdzając, jakie są krystaliczne i amorficzne ciała stałe.
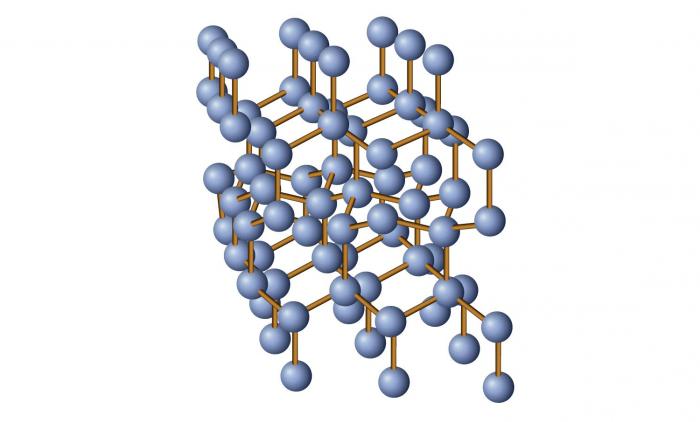
Krystaliczny i ciała amorficzne: ogólna koncepcja
Wszystkie ciała stałe, ciała, obiekty są warunkowo podzielone na:
- krystaliczny;
- bezpostaciowy.
Różnica między nimi jest ogromna, ponieważ podstawą jednostki są oznaki struktury i przejawione właściwości. Krótko mówiąc, stałe kryształy to te substancje i ciała, które mają określony rodzaj przestrzeni sieć krystaliczna to znaczy, że mają możliwość zmiany w określonym kierunku, ale nie we wszystkich (anizotropia).
Jeśli jednak scharakteryzowane zostaną związki amorficzne, ich pierwszym znakiem jest zdolność do zmiany właściwości fizycznych we wszystkich kierunkach jednocześnie. Nazywa się to izotropią.
Struktura, właściwości krystalicznych i amorficznych ciał są całkowicie różne. Jeśli te pierwsze mają wyraźnie ograniczoną strukturę składającą się z uporządkowanych cząstek w przestrzeni, to ta ostatnia nie ma porządku.

Właściwości ciał stałych
Krystaliczne i amorficzne ciała należą jednak do jednej grupy ciał stałych, a zatem mają wszystkie cechy tego stanu skupienia. To znaczy, ogólne właściwości dla nich będą następujące:
- Mechaniczny - elastyczność, twardość, zdolność odkształcania.
- Ciepło - temperatury wrzenia i topnienia, współczynnik rozszerzalności cieplnej.
- Elektryczne i magnetyczne - przewodnictwo cieplne i elektryczne.
Tak więc rozpatrywane państwa posiadają wszystkie te cechy. Pojawiają się tylko w amorficznych ciałach, będą nieco inne niż w krystalicznych.
Ważnymi właściwościami do celów przemysłowych są mechaniczne i elektryczne. Zdolność do wyzdrowienia z deformacji lub, przeciwnie, kruszenia i mielenia jest ważną cechą. Dużą rolę odgrywa również fakt, że substancja może przewodzić prąd elektryczny lub nie jest do niej zdolna.

Struktura krystaliczna
Jeśli opisujemy strukturę krystalicznych i amorficznych ciał, to przede wszystkim należy wskazać rodzaj cząstek, które je tworzą. W przypadku krystalizuje to mogą być jony atomy, atomy, jony (w metalach) cząsteczki (rzadko).
Ogólnie rzecz biorąc, struktury te charakteryzują się obecnością ściśle uporządkowanej sieci przestrzennej, która powstaje w wyniku ułożenia cząstek tworzących substancję. Jeśli wyobrażasz sobie strukturę kryształu w przenośni, otrzymujesz coś takiego: atomy (lub inne cząsteczki) są oddalone od siebie w pewnych odległościach, tak że uzyskuje się idealną komórkę elementarną przyszłej sieci krystalicznej. Następnie ta komórka powtarza się wiele razy, a więc tworzy się ogólna struktura.
Główną cechą jest to, że właściwości fizyczne w takich strukturach zmieniają się równolegle, ale nie we wszystkich kierunkach. Zjawisko to nosi nazwę anizotropii. Oznacza to, że jeśli działasz na jedną część kryształu, druga strona może na nią nie reagować. Więc możesz zmielić połowę soli, ale druga pozostanie nietknięta.
Typy kryształów
Zwyczajowo oznacza się dwa warianty kryształów. Pierwszym z nich są struktury monokryształowe, to znaczy, gdy sama siatka jest równa 1. Ciała krystaliczne i amorficzne mają w tym przypadku zupełnie inne właściwości. Ostatecznie pojedynczy kryształ charakteryzuje się anizotropią w czystej postaci. Jest to najmniejsza elementarna struktura.
Jeśli monokryształy powtarza się wiele razy i są połączone w jedno, to mówimy o polikryształu. Wtedy nie ma mowy o anizotropii, ponieważ orientacja komórek elementarnych narusza ogólną uporządkowaną strukturę. Pod tym względem polikryształy i ciała amorficzne są blisko siebie pod względem ich właściwości fizycznych.

Metale i stopy
Krystaliczne i amorficzne ciała są bardzo blisko siebie. Łatwo jest o tym przekonać, biorąc za przykład metale i ich stopy. Same w sobie są w normalnych warunkach stałych. Jednakże w określonej temperaturze zaczynają się topić i dopóki nie dojdzie do całkowitej krystalizacji, pozostaną one w stanie rozciągania, gęstej, lepkiej masie. I to już jest bezpostaciowy stan ciała.
Dlatego ściśle rzecz biorąc, niemal każda substancja krystaliczna może w pewnych warunkach stać się bezpostaciowa. Tak jak ten drugi podczas krzepnięcia, staje się bryłą o uporządkowanej strukturze przestrzennej.
Metale mogą mieć różne typy struktur przestrzennych, z których najbardziej znane i badane są:
- Prosty sześcienny.
- Granularny.
- Objętościowo.
Struktura kryształu może być oparta na pryzmacie lub piramidzie, a jej główna część jest reprezentowana przez:
- trójkąt;
- równoległobok;
- kwadratem;
- sześciokąt.
Substancja o prostej regularnej siatce kratowej ma idealne właściwości izotropowe.

Pojęcie amorficzne
Krystaliczne i bezpostaciowe ciała są na tyle proste, by je odróżnić. W końcu ten drugi często można pomylić z lepkimi cieczami. Struktura amorficznej substancji opiera się również na jonach, atomach, cząsteczkach. Nie tworzą jednak uporządkowanej ścisłej struktury, a zatem ich właściwości zmieniają się we wszystkich kierunkach. Oznacza to, że są izotropowe.
Cząsteczki są rozmieszczone losowo, losowo. Czasem tylko mogą tworzyć małe loci, co nadal nie ma wpływu na ogólne przedstawione właściwości.
Właściwości podobnych ciał
Są identyczne z kryształami. Różnice są jedynie wskaźnikami dla poszczególnych organów. Tak więc, na przykład, możemy rozróżnić takie charakterystyczne parametry ciał bezpostaciowych:
- elastyczność;
- gęstość;
- lepkość;
- wytrzymałość;
- przewodnictwo i półprzewodnictwo.
Często można spełnić warunki brzegowe związków. Krystaliczne i amorficzne ciała mogą stać się pół-amorficzne.
Również interesująca jest cecha danego państwa, która przejawia się ostrym wpływem zewnętrznym. Tak więc, jeśli ciało amorficzne jest poddawane gwałtownemu uderzeniu lub deformacji, wówczas może zachowywać się jak polikrystal i dzielić na małe kawałki. Jednakże, jeśli czas poświęcony tym częściom, wkrótce połączą się ponownie i staną się lepkim płynnym stanem.

Ten stan związków nie ma określonej temperatury, w której zachodzi przemiana fazowa. Proces ten jest znacznie wydłużony, czasem nawet przez dziesięciolecia (na przykład, dekompozycja niskociśnieniowego polietylenu).
Przykłady substancji amorficznych
Istnieje wiele przykładów takich substancji. Wyznaczmy najbardziej oczywiste i często spotykane.
- Czekolada jest typową substancją amorficzną.
- Żywice, w tym fenol-formaldehyd, wszystkie tworzywa sztuczne.
- Bursztynowy
- Szkło o dowolnym składzie.
- Bitum
- Tar
- Wosk i inne.
Ciało bezpostaciowe powstaje w wyniku bardzo powolnej krystalizacji, to znaczy wzrostu lepkości roztworu w miarę obniżania temperatury. Często trudno jest nazwać takie substancje substancjami stałymi, a raczej są one określane jako lepkie, gęste ciecze.
Związki, które w ogóle nie krystalizują podczas krzepnięcia, mają szczególny stan. Nazywa się je szklankami, a państwo szklistym.
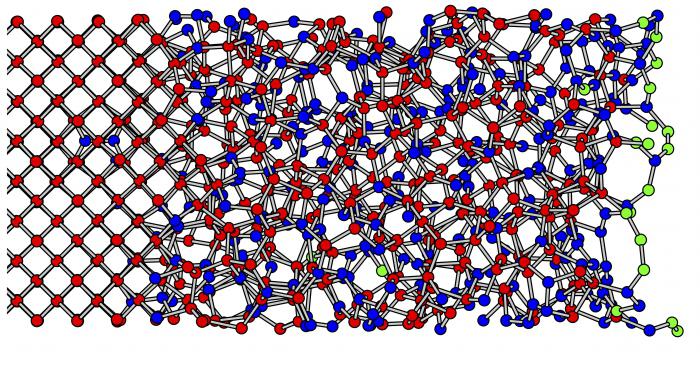
Substancje szkliste
Właściwości krystalicznych i amorficznych ciał są podobne, jak się dowiedzieliśmy, ze względu na ich wspólne pochodzenie i jedną wewnętrzną naturę. Ale czasami są one oddzielnie traktowane jako szczególny stan substancji, zwany szklistem. Jest to homogeniczny roztwór mineralny, który krystalizuje i utwardza się bez tworzenia siatek przestrzennych. Oznacza to, że pozostaje on izotropowy pod względem zmieniających się właściwości zawsze.
Na przykład konwencjonalne szkło okienne nie ma dokładnej wartości temperatury topnienia. To właśnie wraz ze wzrostem tego wskaźnika powoli topi się, zmiękcza i przechodzi w stan ciekły. Jeśli efekt zostanie zatrzymany, nastąpi odwrotny proces i rozpocznie się krzepnięcie, ale bez krystalizacji.
Takie substancje są wysoko cenione, szkło jest dziś jednym z najbardziej powszechnych i poszukiwanych materiałów budowlanych na całym świecie.