Cechy struktury atomu wodoru
Najbardziej rozpowszechnionym elementem w przestrzeni, składającym się z najlżejszych atomów, jest wodór. Został odkryty w XIV wieku przez wielkiego alchemika Paracelsusa. Naukowcy są słusznie uważani za twórców nie tylko medycyny, ale także chemii. Struktura atomu wodoru została dokładniej przeanalizowana przez Nielsa Bohra. Element został następnie odkryty przez astronomów jako część Słońca i innych planet, a także w mgławicach gwiazd gazowych. Procesy przemiany atomów wodoru w atomy helu występują w nich, innymi słowy, obserwuje się reakcję jądrową. W naszym artykule przyjrzymy się nie tylko strukturze atomu wodoru, ale także uwzględnimy charakterystyczne cechy właściwości tego pierwiastka.
Miejsce elementu w układzie okresowym
Wodór jest jedynym pierwiastkiem chemicznym, który jest jednocześnie w dwóch grupach układu okresowego: 1 i 7. Można wytłumaczyć następujący fakt: wykazuje on podwójne właściwości chemiczne. Specjalna struktura atomu wodoru pozwala przekazać swój jedyny elektron do atomów, na przykład elementów aktywnych - niemetali. Są to przede wszystkim halogeny: agresywne pod względem właściwości fluoru, chloru, bromu i jodu. H 2 łatwo wchodzi w interakcję z chalkogenami: siarką, tlenem, selenem. W tym przypadku atomy wodoru są przekształcane w kationy - dodatnio naładowane cząstki.
Ad
Dzięki tej funkcji element ma swoje miejsce w pierwszej grupie układu okresowego. Mechanizm reakcji między metalami i wodorem wygląda inaczej. Zgodnie z teorią struktury atomu wodoru według N. Bohra element ma jeden niesparowany elektron. Atom H akceptuje elektrony z aktywnych atomów metali alkalicznych lub metali ziem alkalicznych. W ten sposób jego konfiguracja elektronowa staje się podobna do cząstki gazu obojętnego helu. Jedyna warstwa energii jest teraz całkowicie ukończona. W tych procesach zmienia się struktura atomu wodoru i przechodzi w postać anionową. Z tego powodu element znajduje się jednocześnie w układzie okresowym także w jego siódmej grupie.

Wszystko w porównaniu
Kontynuując badanie cech strukturalnych cząstek wodoru, zobaczmy, jak ich struktura wewnętrzna wpływa na zachowanie elementu w reakcjach. Aby to zrobić, zwróć uwagę na najbliższych sąsiadów w układzie okresowym i określ, jaka jest struktura atomów wodoru, helu i litu. Przy cząstkach gazu obojętnego wodór łączy w sobie taką samą ilość energii z litem, podobną strukturę zewnętrznej warstwy energetycznej, na której znajduje się jeden elektron. Jednak właściwości wodoru są bardzo różne od zarówno gazu obojętnego, jak i metalu alkalicznego. Fakt ten dowodzi, że wszystkie cechy pierwiastka chemicznego są określone przez strukturę wnęki atomu i cząsteczkę wodoru, to znaczy liczbę poziomów energii i rozmieszczenie na nich elektronów.
Zapewnienie wody
Nazwa elementu wskazuje, że połączenie jego atomów z cząsteczkami tlenu prowadzi do powstania tak wyjątkowej i ważnej substancji dla Ziemi, jak woda. W normalnych warunkach ta reakcja nie występuje, temperatura spalania mieszaniny gazowej sięga 2800 ° C. W laboratorium interakcja między H2 i O2 w stosunku 2: 1 prowadzi do eksplozji. Sama mieszanka nazywana jest gazem detonującym, a proces zachodzący w niej zachodzi przez mechanizm wolnorodnikowy. Jeśli nie jest kontrolowany, reakcja kończy się poważnym problemem - potężną eksplozją. Z tego powodu, pomimo swojej wyjątkowej lekkości, wodór został porzucony jako wypełniacz do samolotów powietrznych. Smutną przyczyną była katastrofa statku powietrznego Hindenburg zmierzającego do Ameryki w 1937 roku. Zobaczmy teraz, jak struktura atomu wodoru wpływa na fizyczne właściwości gazu.
Ad

Wodór, Deuter, Tryt
Nie bądź zaskoczony powyższą listą warunków. Chodzi o ten sam pierwiastek chemiczny, atom wodoru, ładunek atomowy atomu wynosi +1. Drugie i trzecie nazwy to nazwy izotopów. Przyczyną ich różnic jest liczba neutronów w jądrze, podczas gdy liczba protonów wszystkich trzech rodzajów cząstek jest taka sama. Deuter ma dwa neutrony, tryt ma 3, a sam wodór ma 1 neutron w swoim jądrze. Woda zawierająca deuter w swoich cząsteczkach nazywana jest ciężką. Można go znaleźć w stacjach chłodniczych elektrowni jądrowych, a także w składzie cytoplazmy komórek, które mają zaburzony prawidłowy metabolizm.
Struktura elektronowa atomu wodoru
Poniższy schemat pomoże nam zrozumieć specyficzne zachowanie prostej substancji H2 w różnych interakcjach chemicznych.
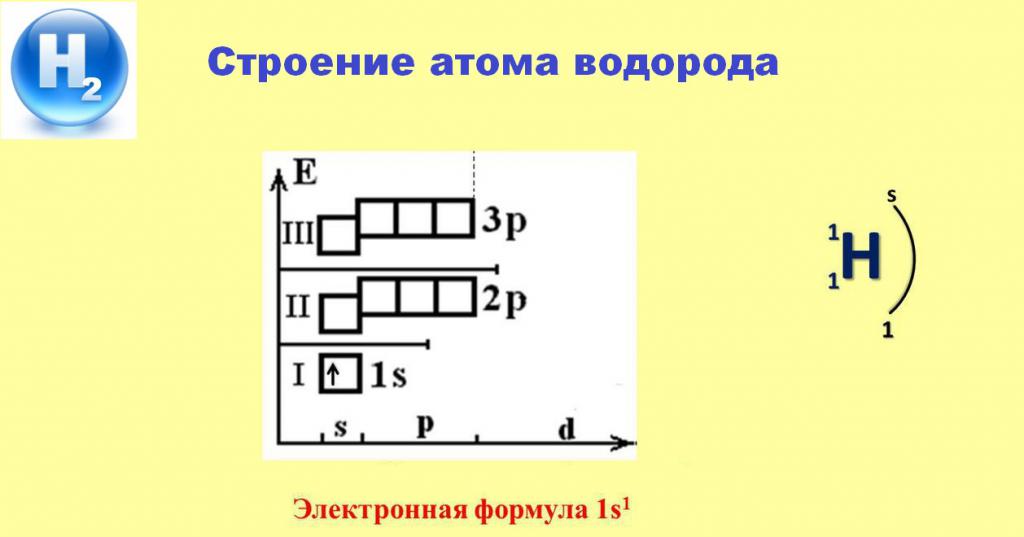
Obecność pojedynczego elektronu zajmującego s-orbitę pierwszego poziomu energii zapewnia stałą wartośćowości wodoru równą 1. W większości przypadków ten elektron opuszcza przestrzeń atomu i przejmuje więcej elementów elektroujemnych. Tylko reakcje z metalami pozwalają wodór narysować elektrony z atomów aktywnych pierwiastków alkalicznych lub ziem alkalicznych do sfery oddziaływania własnego jądra, tworząc białe krystaliczne związki - ich wodorki.
Aktywny i agresywny
Można powiedzieć, że atom wodoru jest łatwy do uniesienia. Inne czynniki redukujące, takie jak węgiel lub jego tlenki, mogą zazdrościć jego szybkości redukcji metali z ich tlenków. Atomy H są również aktywnie łączone z cząsteczkami siarki, tlenu i fosforu. Palnik z atomowym wodorem daje temperaturę powyżej 4000 ° C. Z tego powodu takie urządzenia są łatwe w obróbce powierzchni metalowych: można je ciąć lub spawać.
Ad

Atomowy wodór jest dobrze ugruntowany jako czynnik redukujący czyste metale - wolfram, molibden - z ich rud, reprezentowanych głównie przez tlenki. Podczas spotkania z tymi samymi atomami co on sam, wodór tworzy stabilną i pasywną strukturę - cząsteczkę. Oba atomy H przyklejają się do siebie za pomocą wspólnej pary elektronów, będącej modelem stabilnego kowalencyjnego niepolarnego wiązania. Jest trwały i zapewnia stabilność cząsteczek H2 zarówno w warunkach ziemskich, jak iw kosmosie. Przemysł spożywczy, w którym jest używany do uwodorniania olejów i produkcji niskokalorycznych środków do smarowania, które są modne w nowoczesnej diecie, nie był wolny od wodoru.

W naszym artykule zbadaliśmy strukturę atomu wodoru i dowiedzieliśmy się, jak wpływa on na właściwości prostej substancji.