Okresowe prawa pierwiastków chemicznych Dmitrija Iwanowicza Mendelejewa
Tutaj czytelnik znajdzie informacje o jednym z najważniejszych praw, jakie kiedykolwiek odkrył człowiek na polu naukowym - okresowym prawie Mendelejewa Dmitrija Iwanowicza. Zapoznasz się z jego wartością i wpływem na chemię, przepisy ogólne, cechy i szczegóły dotyczące prawa okresowego, historię odkrycia i podstawowe postanowienia.
Co to jest prawo okresowe?
Prawo okresowe jest prawem naturalnym o charakterze fundamentalnym, odkrytym po raz pierwszy przez D Mendelejewa w 1869 roku, a samo odkrycie było wynikiem porównania właściwości niektórych pierwiastków chemicznych i znanych w tym czasie wartości masy atomowej.

Mendeleev dowodził, że zgodnie z jego prawem, proste i złożone ciała i różne związki pierwiastków zależą od zależności typu okresowego od ciężaru atomu.
Prawo okresowe jest na swój sposób wyjątkowe i wynika to z faktu, że nie wyraża się go w równaniach matematycznych, w przeciwieństwie do innych podstawowych praw natury i wszechświata. Graficznie znajduje swoje odbicie w układzie okresowym pierwiastków chemicznych.
Historia odnajdywania
Odkrycie prawa okresowego miało miejsce w 1869 roku, ale próby usystematyzowania wszystkich znanych elementów X zaczęły się na długo przedtem.
Pierwszą próbę stworzenia takiego systemu podjęła I. V. Debereiner w 1829 r. Sklasyfikował wszystkie znane mu pierwiastki chemiczne w triadę spokrewnioną ze sobą przez bliskość połowy sumy mas atomowych należących do tej grupy trzech składników. Po debereinerum podjęto próbę stworzenia unikalnej tabeli klasyfikacji elementów A. de Chancourtois, nazwał on swój system "spiralą ziemi", a po jej skomponowaniu oktawę Newlands John Newlands. W 1864 roku, niemal równocześnie, William Alding i Lothar Meyer opublikowali tabele stworzone niezależnie od siebie.

Okresowe prawo zostało przedstawione społeczności naukowej 8 marca 1869 r. I stało się to podczas spotkania rosyjskiego społeczeństwa. Mendelejew Dmitrij Iwanowicz ogłosił odkrycie, aw tym samym roku ukazał się podręcznik Mendelejewa "Podstawy chemii", w którym po raz pierwszy pokazano jego układ okresowy. Rok później, w 1870 r., Napisał artykuł i umieścił go na wystawie w RCW, gdzie po raz pierwszy zastosowano pojęcie prawa okresowego. W 1871 r. Mendelejew wyczerpująco opisał swoje z-in w słynnym artykule na temat okresowej legalności pierwiastków chemicznych.

Nieoceniony wkład w rozwój chemii
Znaczenie prawa okresowego jest niezwykle duże dla społeczności naukowej całego świata. Wynika to z faktu, że jego odkrycie dało potężny impuls do rozwoju zarówno chemii, jak i innych nauki przyrodnicze, na przykład fizyka i biologia. Wzajemne powiązanie pierwiastków z ich jakościowymi cechami chemicznymi i fizycznymi było otwarte, pozwoliło także zrozumieć istotę budowy wszystkich elementów według jednej zasady i dało początek nowoczesnemu sformułowaniu pojęć dotyczących pierwiastków chemicznych, aby określić wiedzę o substancjach o złożonej i prostej strukturze.
Zastosowanie okresowego prawa pozwoliło rozwiązać problem przewidywania chemicznego, aby określić przyczynę zachowania znanych pierwiastków chemicznych. Fizyka atomowa, w tym energia jądrowa, stała się możliwa dzięki temu samemu prawu. Z kolei dane naukowe pozwoliły rozszerzyć horyzonty istoty tego prawa i głębiej wejść w jego rozumienie.
Właściwości chemiczne pierwiastków układu okresowego
Zasadniczo pierwiastki chemiczne są ze sobą powiązane charakterystycznymi dla nich właściwościami w wolnym stanie zarówno atomu, jak i jonu, solwatowanego lub uwodnionego, w prostej substancji i formie, którą mogą tworzyć liczne związki. Jednak właściwości x-cue zwykle składają się z dwóch zjawisk: właściwości charakterystycznych dla atomu w stanie swobodnym i prostej substancji. Wiele rodzajów właściwości należy do tego rodzaju właściwości, ale najważniejsze są:
- Jonizacja atomowa i jej energia, w zależności od pozycji elementu w tabeli, liczby porządkowej.
- Relacja energetyczna między atomem a elektronem, która podobnie jak jonizacja atomowa, zależy od umiejscowienia pierwiastka w układzie okresowym.
- Elektroujemność atomu nie ma stałej wartości, ale może się zmieniać w zależności od różnych czynników.
- Promienie atomów i jonów - tu z reguły wykorzystuje się dane empiryczne, które związane są z naturą falową elektronów w stanie ruchu.
- Atomizacja substancji prostych - opis reaktywności pierwiastka.
- Stopień utlenienia jest formalną cechą, ale wydaje się jedną z najważniejszych cech tego pierwiastka.
- Potencjał utleniania prostych substancji to pomiar i wskazanie potencjału substancji do jej działania w roztworach wodnych, a także poziom przejawów właściwości natury redoks.
Częstotliwość elementów typu wewnętrznego i wtórnego
Prawo okresowe daje zrozumienie innej ważnej złożonej cząstki natury - okresowości wewnętrznej i wtórnej. Powyższe obszary badań właściwości atomowych, w rzeczywistości, znacznie trudniejsze niż mogłoby się wydawać. Wynika to z faktu, że elementy s, p, d tabeli zmieniają ich cechy jakościowe w zależności od pozycji w okresie (okresowość charakteru wewnętrznego) i grupy (okresowość charakteru drugorzędnego). Na przykład, wewnętrznemu procesowi przejścia elementu s z pierwszej grupy do ósmej na element p towarzyszą punkty minimum i maksimum na krzywej energii zjonizowanego atomu. Zjawisko to pokazuje wewnętrzną niestałość okresowości zmian właściwości atomu w zależności od jego pozycji w okresie.
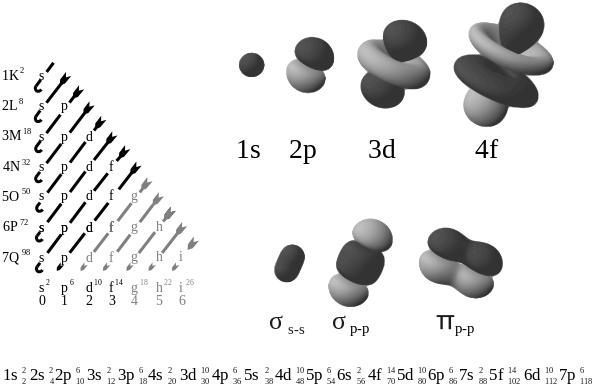
Wyniki
Teraz czytelnik ma jasne zrozumienie i definicję tego, czym jest okresowe prawo Mendelejewa, zdaje sobie sprawę z jego znaczenia dla człowieka i rozwoju różnych nauk oraz ma wyobrażenie o jego aktualnych pozycjach i historii odkryć.