Metoda obligacji walencyjnych i jej główne postanowienia
Metoda wiązania walencyjnego jest uważana za jedną z podstawowych zasad chemia nieorganiczna. Zidentyfikuj jego funkcje, opcje użycia.
Pozycja teoretyczna
Wiązanie chemiczne uważa się za wiązanie między atomami, po którym następuje uwolnienie energii cieplnej.
Spójrzmy na główne punkty metody wiązania walencyjnego.
Kowalencyjna forma jest tworzona za pomocą dwóch elektronów o przeciwnych kierunkach z tyłu.
Utworzona para elektronów jest powszechna, powstaje przez parowanie wolnych elektronów, które należą do dwóch różnych atomów, i powstaje wiązanie kowalencyjne.
Metoda wiązań walencyjnych wyjaśnia także mechanizm wiązania, w którym pojedynczy atom ma parę wolnych elektronów. Drugi element ma wolną orbitę atomową i jest akceptorem.
Charakterystyka wiązania kowalencyjnego
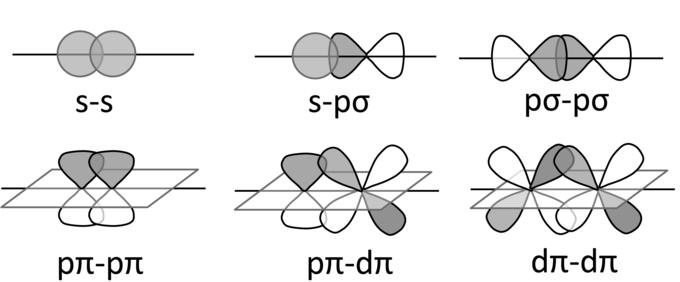
Jaka siła ma wiązanie chemiczne? Metoda wiązań walencyjnych wyjaśnia związek między siłą wiązanie kowalencyjne oraz stopień nakładania się chmur elektronowych oddziałujących ze sobą. Formacja tego rodzaju komunikacji zachodzi w kierunku, w którym następuje całkowita interakcja chmur elektronowych.
Ad
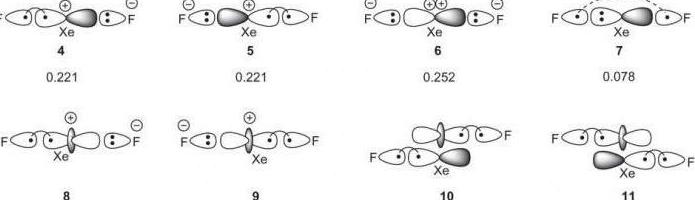
Metoda wiązań walencyjnych wykorzystuje hybrydyzację orbitali głównego pierwiastka chemicznego. Tworzenie wiązań często występuje po zmianie stanu orbitali wartościowości.
Cechy edukacji
Nierówne początkowe orbitale atomowe "mieszają się", tworząc hybrydowe orbitale, które mają ten sam zapas energii. Procesowi hybrydyzacji towarzyszy ciągnięcie chmury w kierunku oddziałującego elektronu, co prowadzi do zachodzenia na siebie chmury hybrydowej ze zwykłym elektronem sąsiedniego atomu.
Metoda wiązań walencyjnych charakteryzuje się tworzeniem silnego wiązania. Procesowi towarzyszy wydzielanie energii, kompensowane kosztami procesu hybrydyzacji.
Główne zasady metody wiązania walencyjnego, przedstawione powyżej w artykule, w pełni wyjaśniają strukturę cząsteczek mających wiązanie kowalencyjne. Jest skierowany na największe nakładanie się orbitali.
Ad
Możliwości walentynkowe
Metoda wiązań walencyjnych pozwala nam zrozumieć, jakie wartościowości może posiadać dany pierwiastek chemiczny. W stanie nieokreślonym możliwości walencyjne są ograniczone przez liczbę niesparowanych elektronów znajdujących się na końcu poziom energii. Po ogrzaniu obserwuje się przejście atomu ze stanu normalnego do postaci wzbudzonej. Procesowi temu towarzyszy wzrost liczby niesparowanych elektronów.
Energia wzbudzenia w chemii nazywa się wartością niezbędną do pełnego przejścia atomu z magazynem o niskiej energii do wyższej formy. Wielość wiązania jest rozumiana jako liczba par elektronów, które są uspołecznione przez najbliższe atomy w wyniku tworzenia kowalencyjnego wiązania chemicznego.
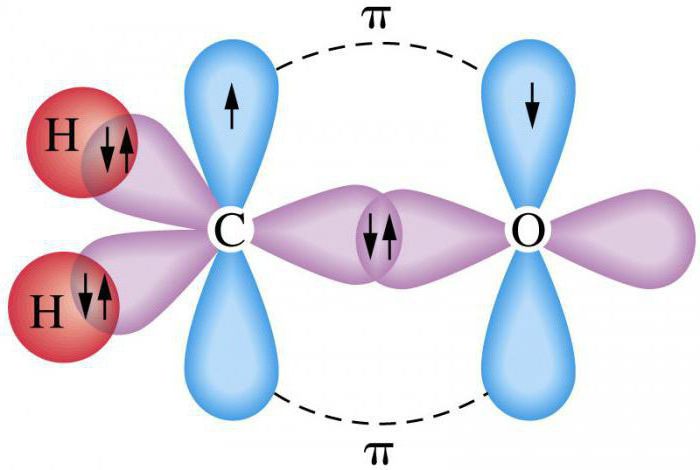
Wiązania Ϭ i π są przybliżonym opisem różnych typów wiązań kowalencyjnych w cząsteczkach. Proste (Ϭ wiązanie) powstaje między chmurami hybrydowymi. Charakteryzuje się on maksymalnym rozkładem gęstości chmury elektronowej wzdłuż osi, wzdłuż której są połączone jądra atomowe.
Ad
Kompleks (sprzężenie π) implikuje boczne nakładanie się niehybrydowych chmur elektronowych. Podczas formowania gęstość chmury elektronowej ma maksymalną wartość we wszystkich kierunkach.
Charakterystyka procesu
Hybrydyzacja komunikacji odnosi się do procesu przemieszczania różnych typów orbitali w cząsteczce wieloatomowej, w wyniku czego powstają chmury o takich samych właściwościach termodynamicznych.
Jakie jest zastosowanie metody wiązania walencyjnego? Przykłady substancji organicznych i nieorganicznych wskazują na jego znaczenie dla wyjaśnienia struktury, a także charakterystyczne właściwości chemiczne związków.
Rodzaje hybrydyzacji
W zależności od tego, ile niesparowanych elektronów jest zmieszanych ze sobą, istnieje kilka głównych typów hybrydyzacji.
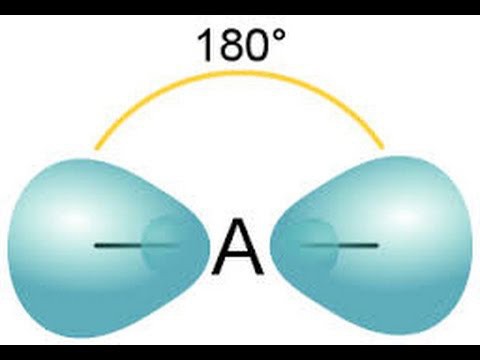
Wariant typu sp zakłada mieszanie pomiędzy orbitaliami s i p. W wyniku tego procesu powstają dwa identyczne orbitale hybrydowe, które zachodzą na siebie pod kątem 180 stopni. W ten sposób są kierowane z jądra atomowego w różnych kierunkach.
Hybrydyzację Sp2 obserwuje się, gdy dwa p-orbitale miesza się z jednym s. W wyniku tego powstają trzy identyczne hybrydowe orbitale, które są skierowane do wierzchołków trójkąta pod tym samym kątem (jego wartość wynosi 120 stopni).
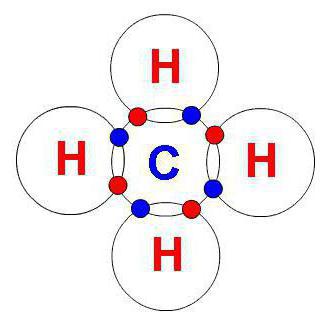
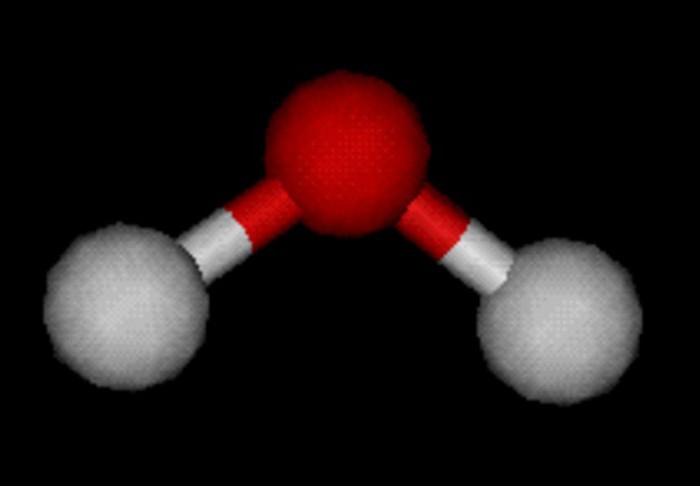
Przy hybrydyzacji sp3 miesza się 3p i jeden s-orbitale. W wyniku tego procesu powstają cztery identyczne chmury hybrydowe, które tworzą czworościan. Kąt wartościowości w tym przypadku wynosi 109 stopni i 28 minut.
Ważne aspekty metody
Wyróżniamy kilka ważnych punktów charakteryzujących metodę wiązania walencyjnego. Do tworzenia kowalencyjnego wiązania chemicznego potrzebne są dwa elektrony, które mają przeciwne spiny. Na przykład, jeśli weźmiemy pod uwagę tworzenie się cząsteczki wodoru, wiąże się ona z nakładaniem się na siebie pojedynczych orbitali elektronowych dwóch atomów, pojawieniem się jednej wspólnej pary elektronów między nimi.
Ad
Analizując wiązanie kowalencyjne utworzone przez typ akceptora-dawcy, podajemy jako przykład tworzenie kationu amonowego. W tym przypadku dawcą jest azot, który ma swoją własną parę elektronów, a akceptor jest protonem wodoru zawartym w kwasach. W utworzonym kationie amonowym tworzą się trzy wiązania przez chmury hybrydowe, a jeden tworzy się przez nakładanie się wzdłuż typu donor-akceptor. Gęstość elektronowa jest rozkładana równomiernie, więc wszystkie wiązania są uważane za kowalencyjne.
Wniosek
W procesie tworzenia wiązania między atomami niemetali obserwuje się nakładanie się funkcji falowych elektronów. Siła wiązania zależy od kompletności interakcji chmur elektronowych. W stanie normalnym walencja atomu charakteryzuje się liczbą niesparowanych elektronów uczestniczących w tworzeniu wspólnych par elektronów z innymi atomami.
Dla atomu w stanie rozgrzanym (wzbudzonym) jest on związany z liczbą wolnych (niesparowanych) elektronów, a także liczbą nie zajmowanych orbitali.
Podsumowując, zauważamy, że metoda wiązań walencyjnych pozwala nam wytłumaczyć powstawanie cząsteczek substancji nieorganicznych i organicznych. Jako miarę wiązań walencyjnych należy stosować liczbę wiązań chemicznych, które łączy z innymi pierwiastkami.
Ad
Elektrony walencyjne są uważane za te, które znajdują się na poziomie zewnętrznym. To stwierdzenie odnosi się do elementów głównych podgrup. Jeśli weźmiemy pod uwagę elementy, które znajdują się w układzie okresowym w podgrupie wtórnej, to walencyjność zostanie określona przez elektrony znajdujące się na poziomie energii przed zewnętrznym.
Rozważając dowolną cząsteczkę, można zastosować metodę wiązania walencyjnego, aby skomponować elektroniczną formułę, a także przyjąć aktywność chemiczną i właściwości związku. W zależności od tego, ile chmur bierze udział w procesie, powstaje różna liczba orbitali hybrydowych. Prowadzi to do pojawienia się pojedynczych, podwójnych, potrójnych wiązań w cząsteczkach substancji nieorganicznych i organicznych.
Tutaj krótko przejrzeliśmy metodę wiązania walencyjnego, jego pozycję.